Tính biến thiên enthalpy chuẩn của phản ứng:
Biết Eb (H-H) = 436 kJ/mol, Eb (C-H) = 418 kJ/mol, Eb (C-C) = 346 kJ/mol, Eb (C=C) = 612 kJ/mol.
 Giải bởi qa.haylamdo.com
Giải bởi qa.haylamdo.com
Đáp án đúng là: B
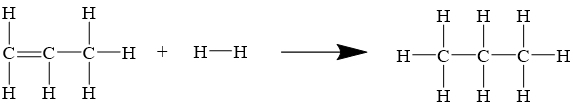
Tính biến thiên enthalpy của phản ứng theo năng lượng liên kết khi các chất ở trạng thái nào?
Nhiệt lượng tỏa ra hay thu vào của một phản ứng ở một điều kiện xác định được gọi là gì?
Công thức tính biến thiên enthalpy của phản ứng theo năng lượng liên kết đúng là?
Xác định biến thiên enthalpy của phản ứng sau ở điều kiện chuẩn:
biết nhiệt tạo thành của CH4(g) là -74,9 kJ/mol, của CO2(g) là - 393,5 kJ/mol, của H2O(l) là -285,8 kJ/mol.