Cho 5 gam bột Mg vào dung dịch hỗn hợp KNO3 và H2SO4, đun nhẹ, trong điều kiện thích hợp, đến khi phản ứng xảy ra hoàn toàn thu được dung dịch X chứa m gam muối; 1,792 lít hỗn hợp khí Y (đktc) gồm hai khí không màu, trong đó có một khí hóa nâu ngoài không khí và còn lại 0,44 gam chất rắn không tan. Biết tỉ khối hơi của Y đối với H2 là 11,5. Tính m?
 Giải bởi qa.haylamdo.com
Giải bởi qa.haylamdo.com
Phương pháp giải:
Kết luận các khí có trong Y và tính số mol mỗi khí trong Y
Áp dụng bảo toàn electron, chứng minh sau phản ứng thu được muối amoni, tính số mol muối amoni.
Tìm số mol các ion K+ và SO42- thông qua H+và NO3-
Áp dụng bảo toàn khối lượng cho dung dịch X và tìm m.
Giải chi tiết:
Hỗn hợp khí Y gồm NO (x mol) và H2 (y mol)
(1)
(2)
Từ (1) và (2)
Ta có mMg phản ứng = 5 – 0,44 = 4,56 gam
Quá trình trao đổi electron:
Mg0 → Mg+2 + 2e 4H+ + NO3- + 3e → NO + 2H2O
0,19 → 0,38 0,24 ← 0,06 ← 0,18 ← 0,06
10H+ + NO3- + 8e → NH4+ + 3H2O
0,2 ← 0,02 ← 0,16 → 0,02
2H+ + 2e → H2
0,04 ← 0,04 ← 0,02
Ta thấy: ne nhường = 2nMg phản ứng = 0,38 mol ≠ ne nhận = 3nNO + 2nH2 = 3.0,06 + 2.0,02 = 0,22
→ Phản ứng có tạo muối amoni
Dung dịch X chứa Mg2+(0,19 mol), K+ (0,08 mol), SO42- (0,24 mol), NH4+ 0,02 mol
Cho khí CO dư đi vào ống sứ nung nóng đựng hỗn hợp gồm Al2O3, Fe2O3 và CuO. Sau khi phản ứng hoàn toàn, thu được chất rắn X và khí Y. Dẫn Y vào nước vôi trong dư thu được kết tủa trắng. Viết các phương trình hóa học và xác định các chất trong X và Y.
Từ ơgenol (trong tinh dầu hương nhu) điều chế được metylơgenol (M = 178 g/mol) là chất dẫn dụ côn trùng. Kết quả phân tích nguyên tố của metylơgenol cho thấy % khối lượng của các nguyên tố như sau: %C = 74,16%; %H = 7,86%, còn lại là oxi. Xác định CTPT của metylơgenol.
Đặt P trắng và P đỏ trên lá sắt và đốt bằng đèn cồn theo sơ đồ thí nghiệm dưới đây:
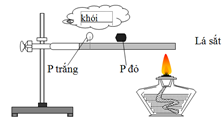
Sau một thời gian, người ta thấy P trắng bốc cháy trong không khí. Thí nghiệm này chứng tỏ
Hoà tan hoàn toàn 8,4 gam Fe vào dung dịch HNO3 đặc nóng, dư thu được V lít (đktc) khí NO2 duy nhất. Tính V.