Đề số 3
-
1219 lượt thi
-
30 câu hỏi
-
45 phút
Danh sách câu hỏi
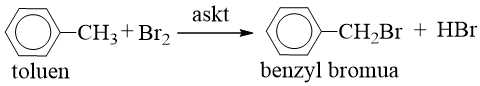
Câu 1:
Đáp án D
Các ancol no, đơn chức tác dụng được với CuO nung nóng tạo anđehit là ancol bậc I.
Câu 3:
Đốt cháy hoàn toàn hỗn hợp 3 ankin A, B, C thu được 3,36 lít CO2 (đktc) và 1,8 gam nước. Số mol hỗn hợp ankin bị đốt cháy là
Đáp án B
Ta có: \({n_{C{O_2}}} = \frac{{3,36}}{{22,4}} = 0,15\,mol\); \({n_{{H_2}O}} = \frac{{1,8}}{{18}} = 0,1\,mol\)
⇒ \({n_{hh\,\,ankin}} = {n_{C{O_2}}} - {n_{{H_2}O}} = 0,15 - 0,1 = 0,05\,mol\)
Câu 4:
Khi hiđrat hóa etin có xúc tác, nhiệt độ thì thu được sản phẩm cuối cùng là
Đáp án B
CH ≡ CH + H2O CH3CHO
Câu 5:
Đáp án C
Gọi công thức của ancol X là CnH2n + 2O.
⇒ 14n + 18 = 37.2
⇒ n = 4
⇒ Công thức phân tử của X là C4H10O.
Cho X tác dụng với H2SO4 đặc đun nóng đến 180oC thấy tạo thành một anken có nhánh duy nhất ⇒ Công thức cấu tạo của X là CH3 – CH(CH3) – CH2OH
Câu 6:
Hỗn hợp X gồm C2H2 và H2 có cùng số mol. Lấy một lượng hỗn hợp X cho đi qua chất xúc tác thích hợp, đun nóng được hỗn hợp Y. Dẫn Y qua bình đựng nước brom thấy khối lượng bình tăng 10,8 gam và thoát ra 4,48 lít khí Z (đktc) có tỉ khối so với H2 là 8. Thể tích O2 (đktc) cần để đốt cháy hoàn toàn hỗn hợp Y là
Đáp án C
Hỗn hợp X
Bảo toàn khối lượng ta có:
mX = \[{m_ \uparrow } + {m_Z}\] = 10,8 + 0,2.16 = 14 (g)
⇒ 26a + 2a = 14
⇒ a = 0,5 (mol)
Đốt hỗn hợp Y giống như đốt hỗn hợp X nên ta có:
\[\begin{array}{*{20}{l}}{2{C_2}{H_2}\; + {\rm{ }}5{O_2}\; \to \;4C{O_2}\; + {\rm{ 2}}{H_2}O}\\{0,5\;\;\;\; \to 1,25\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;{\rm{ }}\left( {mol} \right)}\\{2{H_2}\; + \;{\rm{ }}{O_2}\; \to \;2{H_2}O}\\{0,5\;\; \to 0,25\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;{\rm{ }}\left( {mol} \right)}\end{array}\]
⇒ \(\sum {{n_{{O_2}}}} \)= 1,25 + 0,25 = 1,5 (mol)
⇒ \({V_{{O_2}}}\)= 1,5.22,4 = 33,6 (lít)
Câu 7:
Nhận xét nào sau đây đúng?
Đáp án A
Loại C vì: Phenol ít tan trong nước
Loại D vì: Do ảnh hưởng của vòng benzen đến OH dẫn tới phenol có tính axit.
Loại B vì: Vòng benzen hút e của nhóm OH làm mật độ điện tích trên OH giảm, liên kết O-H phân cực mạnh hơn. Nguyên tử H của nhóm OH linh động hơn so với ancol nên phenol có tính axit mạnh hơn etanol
Câu 8:
Đáp án B
Phản ứng hóa học giữa axit cacboxylic với ancol (có axit H2SO4 đặc làm xúc tác) là phản ứng este hóa.
Câu 9:
Thuốc thử dùng để nhận biết các dung dịch axit acrylic, ancol etylic, axit axetic đựng trong các lọ mất nhãn là
Đáp án D
Câu 10:
Đáp án C
Khi được chiếu sáng, pentan tham gia phản ứng thế với clo theo tỉ lệ mol 1:1, thu được ba dẫn xuất monoclo là đồng phân cấu tạo của nhau.
Câu 11:
Cho các chất sau:
(X) HO-CH2-CH2-OH; (Y) CH3-CH2-CH2OH;
(Z) CH3-CH2-O-CH3; (T) HO-CH2-CH(OH)-CH2-OH.
Số lượng chất hòa tan được Cu(OH)2 ở nhiệt độ phòng là
Đáp án C
X và T hòa tan được Cu(OH)2 ở nhiệt độ phòng vì có 2 nhóm -OH liên kề (tính chất của poli ancol).
Câu 12:
Đáp án B
Anđehit có thể tham gia phản ứng tráng gương và phản ứng với H2 (Ni, to). Qua hai phản ứng này chứng tỏ anđehit có cả tính khử và tính oxi hóa.
Câu 13:
1 mol buta-1,3-đien có thể phản ứng tối đa với bao nhiêu mol brom?
Đáp án A
Buta-1,3-đien có 2 liên kết π kém bền⇒ 1 mol buta-1,3-đien có thể cộng tối đa với 2 mol Br2.
Câu 14:
Trung hòa 3,88 gam hỗn hợp X gồm hai axit cacboxylic no, đơn chức, mạch hở bằng dung dịch NaOH, cô cạn toàn bộ dung dịch sau phản ứng thu được 5,2 gam muối khan. Nếu đốt cháy hoàn toàn 3,88 gam X thì thể tích oxi (đktc) cần dùng là
Đáp án A
\(\begin{array}{l}{C_{\overline n }}{H_{2\overline n + 1}}COOH + NaOH \to {C_{\overline n }}{H_{2\overline n + 1}}COONa + {H_2}O\\3,88\,gam\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,5,2\,gam\\ \Rightarrow \frac{{3,88}}{{14\overline n + 46}} = \frac{{5,2}}{{14\overline n + 68}}\\ \Rightarrow \overline n = \frac{4}{3} \Rightarrow {M_X} = \frac{{194}}{3}\end{array}\)
⇒ nX = \(\frac{{3,88}}{{\frac{{194}}{3}}} = 0,06\,\,mol\)
⇒ \({V_{{O_2}}} = 0,15.22,4 = 3,36\)lít
Câu 15:
Khi tách nước từ rượu (ancol) 3-metylbutanol-2 (hay 3-metylbutan-2-ol), sản phẩm chính thu được là
Đáp án B
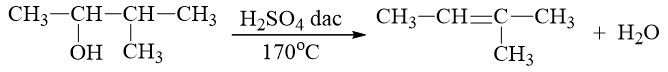
⇒ Sản phẩm chính là 2-metylbut-2-en.
Câu 16:
Cho m gam hỗn hợp X gồm phenol và rượu etylic tác dụng với Na dư thu được 25,2 hỗn hợp muối. Cho \(\frac{m}{{10}}\) gam lượng hỗn hợp X phản ứng vừa đủ với 10ml dung dịch NaOH 1M. Số mol của rượu và phenol là
Đáp án C
\[\begin{array}{*{20}{l}}{{C_6}{H_5}OH{\rm{ }} + {\rm{ }}Na{\rm{ }} \to {\rm{ }}{C_6}{H_5}ONa\;\; + {\rm{ }}0,5{\rm{ }}{H_2}}\\{x\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;x\;\;\;\;\;\;\;\;\;\;\;mol}\\{{C_2}{H_5}OH{\rm{ }} + {\rm{ }}Na{\rm{ }} \to {\rm{ }}{C_2}{H_5}ONa\;\; + {\rm{ }}0,5{\rm{ }}{H_2}}\\{y\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;y\;\;\;\;\;\;\;\;\;mol}\end{array}\]
\[\begin{array}{*{20}{l}}{{C_6}{H_5}OH{\rm{ }} + {\rm{ }}NaOH{\rm{ }} \to {\rm{ }}{C_6}{H_5}ONa\;\; + \;{H_2}O}\\{0,01\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;0,01\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;mol}\end{array}\]
Ta có hệ phương trình:
\[\left\{ \begin{array}{l}116x + 68y = 25,2\\x = 0,01.10\end{array} \right. \Leftrightarrow \left\{ \begin{array}{l}x = 0,1\\y = 0,2\end{array} \right.\]
Câu 17:
Cho 1,52 gam hỗn hợp gồm hai ancol no, đơn chức, mạch hở là đồng đẳng kế tiếp nhau tác dụng hết với một lượng vừa đủ Na kim loại được 2,18 gam chất rắn. Công thức của hai ancol là công thức nào sau đây?
Đáp án A
\(\begin{array}{l}2\overline R OH + 2Na \to 2\overline R ONa + {H_2}\\1,52g\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,2,18g\end{array}\)
⇒ \(\frac{{1,52}}{{\overline R + 17}} = \frac{{2,18}}{{\overline R + 39}}\)
⇒ \(\overline R = 33,6\)
⇒ Công thức của hai ancol là C2H5OH và C3H7OH.
Câu 18:
Dãy gồm các chất đều tác dụng với ancol etylic là
Đáp án A
Ancol etylic phản ứng được với HBr (to), Na, CuO (to), CH3COOH (xúc tác).
C2H5OH + HBr C2H5 – Br + H2O
2C2H5OH + 2Na ⟶ 2C2H5ONa + H2↑
C2H5OH + CuO CH3CHO + Cu + H2O
C2H5OH + CH3COOH CH3COOC2H5 + H2O
Câu 19:
Cho các hợp chất thơm: C6H5OH (1), CH3-C6H3(OH)2 (2), C6H5-CH2OH (3). Chất thuộc loại phenol là
Đáp án A
Các hợp chất (1) và (2) thuộc loại phenol.
Hợp chất (3) thuộc loại ancol thơm.
Câu 20:
Cho các phát biểu sau:
(a) Anđehit vừa có tính oxi hoá vừa có tính khử.
(b) Phenol tham gia phản ứng thế brom khó hơn benzen.
(c) Anđehit tác dụng với H2 (dư) có xúc tác Ni đun nóng, thu được ancol bậc một.
(d) Dung dịch axit axetic tác dụng được với Cu(OH)2.
(e) Dung dịch phenol trong nước làm quỳ tím hoá đỏ.
(g) Trong công nghiệp, axeton được sản xuất từ cumen.
Số phát biểu đúng là
Đáp án A
a) Đúng.
b) Sai. Phenol có nhóm OH hoạt hóa nhân thơm làm cho phản ứng thế dễ hơn benzen.
c) Đúng.
d) Đúng.
e) Sai. Dung dịch phenol có tính axit nhưng rất yếu, không làm đổi màu quỳ tím.
g) Đúng.
Câu 21:
Hỗn hợp X gồm hai axit cacboxylic no, mạch hở Y và Z (phân tử khối của Y nhỏ hơn của Z). Đốt cháy hoàn toàn a mol X, sau phản ứng thu được a mol H2O. Mặt khác, nếu cho a mol X tác dụng với lượng dư dung dịch NaHCO3, thì thu được 1,6a mol CO2. Thành phần % theo khối lượng của Y trong X là
Đáp án C
Gọi công thức chung của X là CnH2n+2-2xO2x
Có a mol CnH2n+2-2xO2x đốt cháy thu được a mol H2O
Áp dụng định luật bảo toàn nguyên tố cho H: a.(2n + 2 – 2x) = 2a
⇒ x = n
⇒ X có số nguyên tử C bằng số nhóm chức.
Số nguyên tử \(\overline H = \frac{{2a}}{a} = 2\)
⇒ X gồm HCOOH (m mol) và HOOC-COOH (n mol)
Chọn a = 1 \( \Rightarrow \left\{ \begin{array}{l}m + n = 1\\m + 2n = 1,6\end{array} \right. \Rightarrow \left\{ \begin{array}{l}m = 0,4\\n = 0,6\end{array} \right.(mol)\)
⇒ \(\% {m_{HCOOH}} = \frac{{0,4.46}}{{0,4.46 + 0,6.90}}.100\% = 25,41\% \)
Câu 22:
Cho m gam hỗn hợp etanal và propanal phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, thu được 43,2 gam kết tủa và dung dịch chứa 17,5 gam muối amoni của hai axit hữu cơ. Giá trị của m là
Đáp án B
RCHO + 2AgNO3 + 3NH3 + H2O RCOONH4 + 2NH4NO3 + 2Ag↓
Ta có: \({n_{Ag}} = \frac{{43,2}}{{108}} = 0,4\,\,mol\)
⇒ \({n_{an{\rm{d}}ehit}} = \frac{{{n_{Ag}}}}{2} = 0,2\,\,mol\)
⇒ manđehit = 17,5 – 0,2.(62 – 29) = 10,9 gam
Câu 23:
Chất X (có M = 60 và chứa C, H, O). Chất X phản ứng được với Na, NaOH, NaHCO3, tên gọi của X là
Đáp án C
X phản ứng được với Na, NaOH, NaHCO3 nên X là axit.
Lại có MX = 60. Vậy X là axit axetic (CH3COOH).
Câu 24:
Dùng H2SO4 đặc, 170oC tách nước 12 gam một ancol no, đơn chức, mạch hở thu được 8,4 gam một anken. Công thức phân tử của ancol đó là
Đáp án D
Bảo toàn khối lượng ta có:
\({m_{ancol}} = {m_{anken}} + {m_{{H_2}O}}\)⇒ \({m_{{H_2}O}} = 12 - 8,4 = 3,6\,\,gam\)
⇒ \({n_{anken}} = {n_{{H_2}O}} = \frac{{3,6}}{{18}} = 0,2\,\,mol\)
⇒ \({M_{anken}} = \frac{{8,4}}{{0,2}} = 42\)
⇒ Anken là C3H6.
⇒ Ancol là C3H7OH.
Câu 25:
Để làm sạch etilen có lẫn axetilen ta cho hỗn hợp đi qua dung dịch nào sau đây?
Đáp án A
Để làm sạch etilen có lẫn axetilen ta cho hỗn hợp đi qua dung dịch AgNO3/NH3 dư vì axetilen phản ứng bị giữ lại, còn etilen không phản ứng thoát ra ngoài.
CH ≡ CH + 2AgNO3 + 2NH3 ⟶ Ag – C ≡ C – Ag + 2NH4NO3
Câu 26:
X là hỗn hợp gồm C6H5OH (phenol) và ancol đơn chức A. Cho 25,4 gam X tác dụng với Na dư thu được 6,72 lít H2 (đktc). Công thức phân tử của A là?
Đáp án D
Gọi công thức phân tử chung của phenol và ancol A là \[\overline R \]OH
\[{n_{{H_2}}} = \frac{{6,72}}{{22,4}} = 0,3\,mol\]
\[\begin{array}{l}\overline {2R} OH{\rm{ }} + {\rm{2}}Na{\rm{ }} \to 2\overline R ONa\;\; + {\rm{ }}{H_2}\\0,6\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\; \leftarrow \;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\,\,\,\,0,3\;mol\end{array}\]
\[{M_{\overline R OH}} = \overline R + 17 = \frac{{25,4}}{{0,6}} = 42,33 \Rightarrow \overline R = 25,333\]
Vậy ancol A là CH3OH.
Câu 27:
Chất nào trong 4 chất dưới đây có thể tham gia cả 4 phản ứng: Phản ứng cháy trong oxi, phản ứng cộng brom, phản ứng cộng hiđro (xúc tác Ni, to), phản ứng thế với dung dịch AgNO3/NH3?
Đáp án B
Axetilen có thể tham gia cả 4 phản ứng: Phản ứng cháy trong oxi, phản ứng cộng brom, phản ứng cộng hiđro (xúc tác Ni, to), phản ứng thế với dung dịch AgNO3 /NH3.
Câu 28:
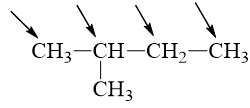
Cho isopentan tác dụng với Cl2 theo tỉ lệ số mol 1: 1, số sản phẩm monoclo tối đa thu được là
Đáp án A
Cho isopentan tác dụng với Cl2 theo tỉ lệ số mol 1: 1, thu được tối đa 4 sản phẩm monoclo.
Câu 29:
Tính thơm của ankylbenzen biểu hiện ở đặc điểm nào?
Đáp án A
Các ankylbenzen dễ tham gia phản ứng thế nguyên tử H của vòng benzen hơn benzen và sự thế ưu tiên ở vị trí ortho và para so với nhóm ankyl.
Các ankylbenzen khó tham gia phản ứng cộng và bền vững với các chất oxi hóa.
⇒ A đúng.
Câu 30:
Đốt cháy hoàn toàn 1 mol hợp chất hữu cơ X, thu được 4 mol CO2. Chất X tác dụng được với Na, tham gia phản ứng tráng bạc với phản ứng cộng Br2 theo tỉ lệ mol 1:1. Công thức cấu tạo của X là
Đáp án C
Số C = \(\frac{{{n_{C{O_2}}}}}{{{n_X}}} = \frac{4}{1} = 4\)
Chất X tác dụng được với Na ⇒ X là chứa nhóm ancol hoặc – COOH
Và X tham gia phản ứng tráng bạc ⇒ X chứa nhóm -CHO
X tham gia cộng Br2 theo tỉ lệ 1:1 ⇒ X có 1 liên kết π.
⇒ Công thức cấu tạo của X là HO – CH2 – CH = CH – CHO.