Đề số 6
-
1457 lượt thi
-
30 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Ở điều kiện thường, chất nào sau đây tồn tại trạng thái lỏng?
Đáp án C
Ở nhiệt độ thường, các ankan có số C từ 18 trở lên sẽ ở thể lỏng.
Câu 2:
Ankan nào sau đây có đồng phân mạch cacbon?
Đáp án A
Các ankan từ C1 đến C3 không có đồng phân. Từ C4 trở đi có đồng phân mạch cacbon.
Câu 4:
Anken có công thức tổng quát là
Đáp án B
Công thức tổng quát của anken là CnH2n với n ≥ 2.
Câu 5:
Đáp án D
Quy tắc Mac-côp-nhi-côp được áp dụng trong phản ứng cộng HX vào anken bất đối xứng.
Câu 7:
Số đồng phân cấu tạo mạch hở của C4H8 là
Đáp án A
Ta có: \(k = \frac{{4.2 - 8 + 2}}{2} = 1\)
⇒ Đồng phân anken
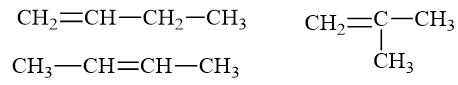
Câu 8:
Số nguyên tử hiđro trong phân tử vinyl axetilen là
Đáp án A
Công thức cấu tạo của vinyl axetilen là CH ≡ C – CH = CH2.
⇒ Có 4 nguyên tử H.
Câu 9:
Đáp án D
Chất có khả năng tác dụng với dung dịch AgNO3/NH3 tạo kết tủa vàng nhạt.
⇒ Chất này có dạng là ank-1-in.
⇒ Axetilen thỏa mãn.
Phương trình hóa học:
CH ≡ CH + 2AgNO3 + 2NH3 → Ag – C ≡ C – Ag↓ + 2NH4NO3
Câu 10:
X có tỉ khối hơi so với H2 bằng 29. Công thức phân tử của X là
Đáp án D
Ta có: MX = 29.2 = 58 đvC
⇒ X là C4H10.
Câu 11:
Khi thực hiện phản ứng đun nóng CH3COONa với vôi tôi xút thu được
Đáp án A
Phương trình hóa học:
CH3COONa (r) + NaOH CH4 + Na2CO3
⟹ X là khí CH4.
Câu 12:
2,8 gam anken X làm mất màu vừa đủ dung dịch chứa 8 gam Br2. Công thức phân tử của X là
Đáp án D
Gọi công thức của anken có dạng CnH2n với n ≥ 2.
\({n_{anken}} = {n_{B{r_2}}} = \frac{8}{{160}} = 0,05\,mol\)
⇒ 14n = \(\frac{{2,8}}{{0,05}} = 56\)
⇒ n = 4
⇒ Công thức phân tử của anken là C4H8.
Câu 13:
Dãy gồm các anken được sắp xếp theo nhiệt độ sôi tăng dần là:
Đáp án B
Nhiệt độ sôi của các anken tăng dần khi số C tăng dần.
⇒ Dãy gồm các anken được sắp xếp theo nhiệt độ sôi tăng dần là C2H4, C3H6, C4H8, C5H10.
Câu 14:
1 mol buta-1,3-đien phản ứng tối đa với bao nhiêu mol Br2?
Đáp án C
Công thức cấu tạo của buta-1,3-đien là: CH2 = CH – CH = CH2.
⇒ có 2 liên kết π.
⇒ 1 mol buta-1,3-đien phản ứng tối đa với 2 mol Br2.
Câu 15:
Đốt cháy 6,72 lít (đktc) hỗn hợp gồm hai hiđrocacbon X và Y (MY > MX) thu được 11,2 lít CO2 (đktc) vào 10,8 gam H2O. Công thức của X là
Đáp án C
Ta có: \({n_{hh}} = \frac{{6,72}}{{22,4}} = 0,3\,mol\)
\({n_{C{O_2}}} = \frac{{11,2}}{{22,4}} = 0,5\,mol\); \({n_{{H_2}O}} = \frac{{10,8}}{{18}} = 0,6\,mol\)
Số \(\overline C \)của hỗn hợp khí là: \(\overline C = \frac{{{n_{C{O_2}}}}}{{{n_{hh}}}} = \frac{{0,5}}{{0,3}} = 1,67 < 2\)
⇒ Khí X là CH4.
Câu 16:
Đáp án D
Gọi công thức tổng quát của ankan và ankin lần lượt là CnH2n +2 (với n ≥ 1) và CmH2m – 2 (với n ≥ 2).
Khi đốt ankan: \({n_{ankan}} = {n_{{H_2}O}} - {n_{C{O_2}}}\)(1)
Khi đốt cháy ankin: \({n_{ankin}} = {n_{C{O_2}}} - {n_{{H_2}O}}\)(2)
(1) – (2) ⇒ nankan – nankin = \(\sum {{n_{{H_2}O}}} - \sum {{n_{C{O_2}}}} \)
Khi đốt cháy hoàn toàn hỗn hợp M gồm một ankan X và một ankin Y, thu được số mol CO2 bằng số mol H2O.
⇒ nankin = nankan
⇒ %nankin = %nankan = 50%
Câu 17:
Hỗn hợp khí X gồm 0,1 mol C2H2 ; 0,2 mol C2H4 và 0,3 mol H2. Đun nóng X với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 11. Hỗn hợp Y phản ứng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
Đáp án B
Áp dụng bảo toàn khối lượng: mY = mX = 0,1.26. + 0,2.28 + 0,3.2 = 8,8 (gam)
Mà MY = 11.2 = 22 ⇒ nY = \(\frac{{8,8}}{{22}}\) = 0,4 mol
Số mol H2 tham gia phản ứng là: nX – nY = (0,1 + 0,2 + 0,3) – 0,4 = 0,2 mol
Ta có:\({n_{{H_2}}}\)phản ứng + \({n_{B{r_2}}}\)= \(2{n_{{C_2}{H_2}}} + {n_{{C_2}{H_4}}}\)
⇒ \({n_{B{r_2}}}\)= 2.0,1 + 0,2 - 0,2 = 0,2 mol
Câu 18:
Ba hiđrocacbon X,Y, Z là đồng đẳng kế tiếp, khối lượng phân tử của Z bằng 2 lần khối lượng phân tử của X. Các chất X, Y , Z thuộc dãy đồng đẳng:
Đáp án C
Phân tử Z hơn phân tử X 2 nhóm CH2 ⇒ MZ = MX + 28
Theo bài: MZ = 2MX ⇒ MX + 28 = 2MX
⇒ MX = 28
⇒ X là C2H4 (anken)
⇒ X, Y, X thuộc dãy đồng đẳng anken.
Câu 20:
Công thức phân tử của toluen là
Đáp án B
Công thức của toluen là C6H5-CH3.
⇒ Công thức phân tử của toluen là C7H8.
Câu 21:
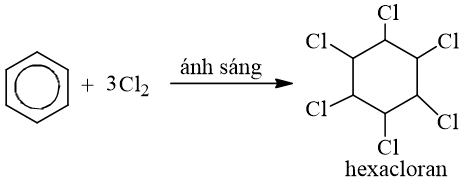
Benzen tác dụng với Cl2 có ánh sáng, thu được hexaclorua. Công thức của hexaclorua là
Đáp án B
Câu 22:
Chất nào sau đây làm mất màu dung dịch KMnO4 khi đun nóng?
Đáp án B
Toluen làm mất màu dung dịch KMnO4 khi đun nóng.
Phương trình hóa học:
C6H5CH3 + 2KMnO4 --> C6H5COOK + 2MnO2 + KOH + H2O
Câu 23:
Đốt cháy hoàn toàn 5,3 gam ankybenzen X thu được 8,96 lít CO2 (đktc). Công thức phân tử của X là
Đáp án D
Gọi công thức của ankylbenzen là \({C_n}{H_{2n - 6}}\) với n ≥ 6.
Ta có: \({n_{C{O_2}}} = \frac{{8,96}}{{22,4}} = 0,4\,mol\) ⇒ \({n_X} = \frac{{0,4}}{n}\,\,(mol)\)
⇒ 14n – 6 = \(\frac{{5,3}}{{\frac{{0,4}}{n}}} = \frac{{53n}}{4}\)
⇒ n = 8
⇒ Công thức phân tử của X là C8H10.
Câu 24:
Chất nào sau đây có đồng phân hình học?
Đáp án C
Anken có đồng phân hình học khi có dạng:
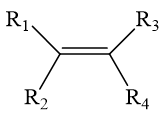 với R1 ≠ R2 và R3 ≠ R4. (R có thể là H)
với R1 ≠ R2 và R3 ≠ R4. (R có thể là H)⇒ CH3CH=CHCH3 có đồng phân hình học.
Câu 25:
Cho 3,36 lít (đktc) hỗn hợp gồm etan và etilen đi chậm qua dung dịch brom dư. Sau phản ứng khối lượng bình brom tăng thêm 2,8 gam. Số mol etan và etilen trong hỗn hợp lần lượt là
Đáp án B
Ta có: \({n_{hh}} = \frac{{3,36}}{{22,4}} = 0,15\,mol\)
Khối lượng bình brom tăng chính là khối lượng của etilen vì chỉ có etilen phản ứng với brom.
⇒ \({m_{{C_2}{H_4}}}\)= 2,8 gam ⇒ \({m_{{C_2}{H_4}}} = \frac{{2,8}}{{28}} = 0,1\,mol\)
⇒ \({n_{{C_2}{H_6}}}\)= 0,15 - 0,1 = 0,05 mol
Câu 26:
Đốt cháy hoàn toàn V lít (đktc) hỗn hợp X gồm CH4, C2H4 thu được 0,15 mol CO2 và 0,2 mol H2O. Giá trị của V là
Đáp án A
Ta có: \({n_{C{H_4}}} = {n_{{H_2}O}} - {n_{C{O_2}}}\)= 0,2 - 0,15 = 0,05 mol
Bảo toàn nguyên tố C: \[{n_{C{H_4}}}\; + {\rm{ }}2{n_{{C_2}{H_4}}}{\rm{ = }}{n_{C{O_2}}}\]
⇒ \({n_{{C_2}{H_4}}}\)= 0,05 mol
⇒ V = 22,4.(0,05 + 0,05) = 2,24 lít
Câu 27:
Hỗn hợp khí X gồm H2 và C3H6 có tỷ khối so với H2 là 9. Hỗn hợp X qua Ni nung nóng, thu được hỗn hợp khí Y có tỉ khối so với H2 là 11,25. Hiệu suất của phản ứng hiđro hóa là
Đáp án C
Ta có: \(\frac{{{n_{{H_2}}}}}{{{n_{{C_3}{H_6}}}}} = \frac{{42 - 9.2}}{{9.2 - 2}} = \frac{3}{2}\)⟹ Hiệu suất tính theo C3H6.
Mà mX = mY ⟹ \(\frac{{{n_X}}}{{{n_Y}}} = \frac{{{{\overline M }_Y}}}{{{{\overline M }_X}}} = \frac{{2.11,25}}{{2.9}} = \frac{5}{4}\)
Giả sử, nX = 5, nY = 4 ⟹ Trong hỗn hợp X chứa \({n_{{H_2}}} = 3\,mol\); \({n_{{C_3}{H_6}}} = 2\,mol\)
⟹ \({n_{{C_3}{H_6}\,pu}}\) = nX – nY = 5 – 4 = 1 mol
⟹ H = \[\frac{1}{2}.100\% = 50\% \]
Câu 28:
Công thức phân tử của etylbenzen là
Đáp án D
Công thức của etylbenzen là C6H5-CH2CH3.
⇒ Công thức phân tử của etylbenzen là C8H10.
Câu 29:
Đáp án B
Hiđrocacbon X có chứa vòng benzen, X không thể là C6H4 vì riêng vòng benzen đã chứa 3π + 1 vòng nên nếu có 6C thì số H phải là 6.