A. 1,0.
B. 0,25.
C. 0,75.
D. 0,5.
 Giải bởi qa.haylamdo.com
Giải bởi qa.haylamdo.com
Trả lời:
Mg2+ + CO32- → MgCO3
Ba2+ + CO32- → BaCO3
Ca2+ + CO32- → CaCO3
Ta có: nMg2+ + nBa2+ + nCa2+ = nCO3 2- = nNa2CO3= 0,25 mol
Áp dụng định luật bảo toàn điện tích với dung dịch X ta có:
2. (nMg2+ + nBa2+ + nCa2+)= nCl- + nNO3-
→ nCl- + nNO3- = 0,5 mol
Đáp án cần chọn là: D
Phần 1: Hòa tan hoàn toàn bằng dung dịch HCl dư thu được 1,792 lít H2 (đktc).
Phần 2: Nung trong không khí dư, thu được 2,84 gam hỗn hợp rắn chỉ gồm các oxit.
Khối lượng hỗn hợp X là:
(a) Cho dung dịch Ba(HCO3)2 vào dung dịch NaHSO4.
(b) Cho Na vào dung dịch FeCl2 dư.
(c) Cho dung dịch (NH4)2SO4 vào dung dịch Ba(OH)2.
(d) Sục khí CO2 dư vào dung dịch hỗn hợp NaOH và Ba(OH)2.
(e) Cho dung dịch AgNO3 vào dung dịch Fe(NO3)2.
Sau khi các phản ứng kết thúc, số thí nghiệm thu được cả kết tủa và khí là
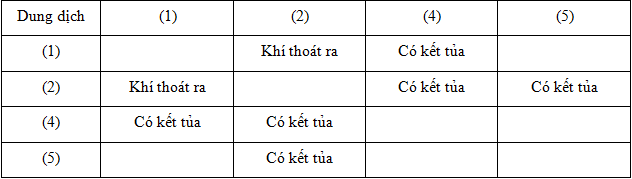
Các dung dịch (1), (3), (5) lần lượt là
Hỗn hợp X gồm Na và Ba có tỉ lệ mol 1 : 1. Hòa tan một lượng X vào nước được 3,36 lít H2 (đktc) và dung dịch Y. Cho 4,48 lít CO2 hấp thụ hết vào dung dịch Y thì thu được m gam kết tủa. Giá trị của m là:
Ion \[CO_3^{2 - }\]cùng tồn tại với các ion sau trong một dung dịch:
(1) (NH4)2SO4 + BaCl2
(2) CuSO4 + Ba(NO3)2
(3) Na2SO4 + BaCl2
(4) H2SO4 + BaSO3
(5) (NH4)2SO4 + Ba(OH)2
(6) Fe2(SO4)3 + Ba(NO3)2
Các phản ứng đều có cùng phương trình ion rút gọn là