20 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án
20 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án ( Đề 6)
-
2025 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Cần phân biệt rõ inox, tôn, sắt tây, gang hoặc thép: Fe-Cr: inox; Fe-Zn: tôn; Fe-Sn: sắt tây; Fe-C: gang hoặc thép.
Chọn đáp án A.
Câu 2:
Nguyên tố nào sau đây thường có hàm lượng cao ở ven đường quốc lộ?
Trước đây trong xăng dầu, người ta thường pha một lượng tetraetyl chì để tăng chỉ số octan. Khi đốt cháy xăng trong động cơ ôtô, xe máy, chất này thải ra ngoài môi trường một lượng lớn chì dưới dạng chì oxit PbO (độc hại với sức khỏe con người). Ven đường quốc lộ, mật độ xe lưu thông nhiều, lượng chì thải ra môi trường và tích tụ lớn.
Hàm lượng Pb đặc biệt cao đột biến trong các cây xanh trồng ven đường quốc lộ là do cây đã hấp thụ Pb trong khói xăng dầu do các phương tiện cơ giới thải ra. Ở Việt Nam, hiện nay đã cấm sử dụng xăng pha chì trên phạm vi toàn quốc.
Chọn đáp án D.
Câu 3:
Na tan trong nước giải phóng khí theo phương trình: .
Chọn đáp án C.
Câu 5:
Thủy phân vinyl axetat trong môi trường axit thu được?
Vinyl axetat thuỷ phân trong môi trường axit tạo và (không bền). .
Chọn đáp án B.
Câu 6:
Công thức nào sau đây biểu diễn đúng mối quan hệ giữa và độ pH trong dung dịch?
hay .
Chọn đáp án C.
Câu 7:
Chất nào sau đây thuộc loại ankađien liên hợp?
Trong công thức cấu tạo của Ankađien liên hợp, 2 nối đôi cách nhau 1 nối đơn.
Chọn đáp án D.
Câu 8:
Cacbohiđrat nhất thiết phải chứa nhóm chức nào sau đây?
Cacbohidrat nhất thiết phải chứa nhóm chức ancol trong phân tử.
Chọn đáp án A.
Câu 9:
Trong công nghiệp, nhôm được điều chế bằng cách nào dưới đây?
A. Sai, dễ thăng hoa, không điều chế bằng phương pháp điện phân nóng chảy được.
B. Sai, do Al bị điện phân sau nước.
C. Sai, cho Na vào dung dịch sẽ tạo .
D. Đúng, phương trình phản ứng: .
Chọn đáp án D.
Câu 10:
Cho các hợp kim: Fe - Cu; Fe - C; Zn - Fe; Mg - Fe tiếp xúc với không khí ẩm. Số hợp kim trong đó Fe bị ăn mòn điện hóa là?
Trong ăn mòn điện hóa, kim loại có tính khử mạnh hơn sẽ bị ăn mòn trước. Fe bị ăn mòn khi Fe là anot : Fe-Cu; Fe-C.
Chọn đáp án B.
Câu 11:
Lấy cùng 1 mol các kim loại Mg, Al, Zn, Fe cho tác dụng với dung dịch loãng dư. Kim loại nào giải phóng lượng khí nhiều nhất ở cùng điều kiện?
Khi phản ứng với
1 mol Al ® 1,5 mol
1 mol (Zn, Mg, Fe) ® 1 mol .
Chọn đáp án D.
Câu 12:
Cho dãy các chất: . Số chất trong dãy phản ứng được với dung dịch NaOH là?
Các chất phản ứng được với dung dịch NaOH là: .
Chọn đáp án A.
Câu 13:
Có 5 lọ mất nhãn đựng 5 chất bột màu trắng: . Chỉ dùng nước và khí cacbonic có thể nhận biết được mấy chất ?
Khi tác dụng với nước, các muối trên chia thành 2 nhóm:
Nhóm 1: Tan trong nước: .
Nhóm 2: Tạo kết tủa trắng: .
Sục vào 2 lọ đựng chất rắn không tan trong nhóm 2. Lọ chứa , kết tủa bị hòa tan. Lọ chứa không có hiện tượng gì xảy ra.
Dùng vừa thu được cho tác dụng với các lọ mất nhãn trong nhóm 1, sau đó sục khí vào và quan sát hiện tượng:
Không có hiện tượng gì: NaCl
Có kết tủa trắng xuất hiện, sau đó kết tủa bị hòa tan:
Có kết tủa trắng xuất hiện, sau đó kết tủa không bị hòa tan:
Chọn đáp án A.
Câu 14:
Dung dịch X chứa các ion sau:. Để tách được nhiều cation ra khỏi dung dịch nhất mà không đưa thêm cation mới vào, ta có thể cho dung dịch X tác dụng vừa đủ với dung dịch nào sau đây?
Cần chú ý đến cụm từ “tách được nhiều cation nhất ra khỏi dung dịch” và “không đưa thêm ion mới vào”.
Ion có thể được tách ra khỏi dung dịch dưới dạng kết tủa hoặc khí.
A. Loại, tạo 2 kết tủa và chỉ tách được 2 cation là: và .
B. Loại, do đưa thêm ion mới vào dung dịch
C. Loại, gốc khi kết hợp với các cation trong X đều tạo các muối tan không tách được ion nào ra khỏi dung dịch X
D. Đúng, do tạo được 3 kết tủa là và giải phóng khí tách được 4 cation: .
Chọn đáp án D.
Câu 15:
Lên men rượu dung dịch chứa 225 gam glucozơ thu được 92 gam ancol etylic. Hiệu suất quá trình lên men tạo thành ancol etylic là?
Phương trình phản ứng :
Hiệu suất quá trình lên men tạo thành ancol etylic là : .
Chọn đáp án C.
Câu 16:
Khi clo hóa PVC ta thu được tơ clorin chứa 66,18% clo về khối lượng. Hỏi trung bình 1 phân tử clo tác dụng với bao nhiêu mắt xích PVC?
Giả sử có k mắt xích thế với 1 phân tử Clo
Chọn đáp án B..
Câu 17:
Phát biểu nào sau đây đúng?
A. Sai, polietilen và poli(vinyl clorua) là sản phẩm của phản ứng trùng hợp.
B. Sai, tơ nilon-6,6 được điều chế từ hexametylenđiamin và axit ađipic.
C. Sai, tơ visco và tơ xenlulozơ axetat thuộc loại tơ bán tổng hợp (hay tơ nhân tạo).
D. Đúng, sợi bông và tơ tằm là polime thiên nhiên.
Chọn đáp án D.
Câu 18:
Nhiệt phân hoàn toàn hỗn hợp X gồm 2 muối và , rồi hấp thụ toàn bộ sản phẩm khí sinh ra vào nước dư, thấy có 0,56 lít khí thoát ra (đktc). Khối lượng trong X là
Phương trình phản ứng nhiệt phân xảy ra như sau: (1)
(2)
(3)
Toàn bộ khí sinh ra ở phản ứng (2) hấp thụ vừa đủ với nước để sinh ra ở phản ứng (3). Khí thoát ra là khí sinh ra ở phản ứng (1).
Từ (1) ta có: .
Ghi nhớ: Khi làm bài tập về phản ứng nhiệt phân muối nitrat, cần chú ý rằng độ bền nhiệt của các muối nitrat phụ thuộc vào bản chất cation kim loại tạo muối.
Chọn đáp án B.
Câu 19:
Cho các hợp chất sau:
(a)
(b)
(c)
(d)
(e)
(f)
Các chất đều tác dụng được với là:
Ancol cần thỏa mãn các điều kiện sau đây:
- Tác dụng được với Na: Cần có nguyên tử Hiđro linh động
- Tác dụng được với : Là ancol đa chức và có các nhóm -OH liền kề nhau.
Chọn đáp án C.
Câu 20:
Dãy gồm các chất được sắp xếp theo chiều tăng dần nhiệt độ sôi từ trái sang phải là?
§ Thứ tự tăng dần của các hợp chất hữu cơ có khối lượng phân tử tương đương nhau:
Hidrocacbon < Andehit < Ancol < Axit cacboxylic
§ tăng theo chiều tăng phân tử khối: .
Chọn đáp án D.
Câu 21:
Đốt cháy hoàn toàn 0,11 gam một este X, thu được 0,22 gam và 0,09 gam . Số công thức cấu tạo phù hợp của X là?
.
Suy ra trong X, ® X là este no, đơn chức, mạch hở.
Công thức phân tử của X là . Có 4 đồng phân cấu tạo phù hợp của X là:
.
Chọn đáp án D.
Câu 22:
Cho 0,1 mol axit glutamic vào 150 ml dung dịch HCl 2M, thu được dung dịch X. Cho KOH dư vào dung dịch X. Sau khi các phản ứng xảy ra hoàn toàn, số mol KOH đã phản ứng là?
Cách 1: Theo đầu bài:
Khi cho dư ta có:
Cách 2: Coi axit glutamic và HCl chưa phản ứng với nhau:
Khi cho dư ta có:
Câu 23:
Ta có phản ứng:
Áp dụng bảo toàn khối lượng:
.
Vậy:
Biện luận (*) ta có: (thỏa mãn) ® X là: .Câu 24:
Chất hữu cơ A chứa 7,86% H; 15,73% N về khối lượng. Đốt cháy hoàn toàn 2,225 gam A thu được , hơi nước và khí nitơ, trong đó thể tích khí là 1,68 lít (đktc). Công thức phân tử của A là (biết )?
Ta có:
.
Do đó:
Þ Công thức đơn giản nhất của A là .
Đặt công thức phân tử của A là . Theo giả thiết ta có:
.
Vậy công thức phân tử của A là .
Chọn đáp án B.
Câu 25:
Cho 11,8 gam amin no, đơn chức X, tác dụng vừa đủ với dung dịch HCl thu được 19,1 gam muối khan. Mặt khác nếu đốt cháy hoàn toàn lượng amin trên bằng lượng không khí vừa đủ thì thu được V (lít) khí (đktc). Giá trị của V là?
Áp dụng tăng giảm khối lượng:
Theo phản ứng:
.
Chọn đáp án D.
Câu 26:
Hấp thụ hoàn toàn 0,672 lít khí (đktc) vào 1 lít dung dịch gồm NaOH 0,025M và 0,0125M, thu được m gam kết tủa. Giá trị của m là?
Theo đầu bài ta có:
.
Nhận xét: Þ Phản ứng tạo ra muối và .
Phương trình phản ứng:
(1)
(2)
Từ (1), (2) và giả thiết ta có:
So sánh số mol ta thấy Þ Lượng kết tủa sinh ra theo ion .
(3)
Vậy .
Câu 28:
Phát biểu nào sau đây đúng?
A. Sai: không có tính khử vì số oxi hóa của Al trong đã cao nhất.
B. Sai: Fe, Cu có thể điều chế bằng phương pháp nhiệt luyện.
C. Đúng: .
D. Sai: Chỉ có là oxit axit, CO là oxit trung tính (oxit không tạo muối) - không tác dụng với nước, axit, bazơ ở điều kiện thường.
Chọn đáp án C.
Câu 29:
Cho sơ đồ chuyển hóa sau:
T và Y lần lượt là?
1)
2)
3)
4)
5)
Chọn đáp án D.
Câu 30:
Phát biểu nào sau đây là đúng?
A. Sai: Trong pin điện hóa, anot là cực âm, catot là nơi xảy ra sự khử.
B. Sai: Trong bình điện phân, anot là cực dương, nơi xảy ra sự oxi hóa.
C. Đúng: Trong pin và bình điện phân, anot là nơi xảy ra sự oxi hóa, catot là nơi xảy ra sự khử.
D. Sai: Các điện cực trong pin và bình điện phân giống nhau về bản chất, khác nhau về dấu.Câu 31:
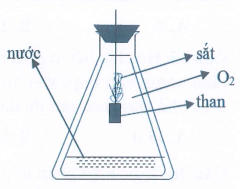
Cho phản ứng của sắt (Fe) với oxi () như hình vẽ dưới đây. Trong số các phát biểu sau, số phát biểu đúng là?
(1) Sản phẩm của phản ứng là .
(2) Khi đưa vào lọ chứa oxi, dây thép cháy trong oxi sáng chói, nhiều hạt nhỏ sáng bắn tóe như pháo hoa.
(3) Nước trong bình có vai trò là chất xúc tác để cho phản ứng xảy ra nhanh hơn.
(4) Mẩu than gỗ có tác dụng làm mồi vì khi than cháy, tỏa ra nhiệt lượng đủ lớn để phản ứng giữa Fe và xảy ra (có thể thay mẩu than bằng que diêm).
(5) Cần làm sạch và uốn sợi dây thép thành hình lò xo để tăng diện tích tiếp xúc, phản ứng xảy ra nhanh hơn.
(1) Sai: Sản phẩm của phản ứng là .
(2) Đúng.
(3) Sai: Do phản ứng tỏa nhiệt mạnh, nước được dùng để truyền nhiệt, tránh vỡ bình.
(4) Đúng.
(5) Đúng.
Chọn đáp án C.
Câu 32:
X, Y, Z, T là một trong các chất sau: glucozơ, anilin, fructozơ và phenol. Tiến hành các thí nghiệm để nhận biết chúng và ta có kết quả như sau:
| Thuốc thử | X | T | Y | Z |
| Kết tủa | Nhạt màu | Kết tủa | (-) | |
|
|
(-) | Kết tủa | (-) | Kết tủa |
|
Dd NaOH
|
(-) | (-) | (+) | (-) |
Các chất X, Y, Z, T lần lượt là?
Xét chất Z ta có: Glucozơ và anilin không phản ứng với NaOH ® Loại B và C, còn lại A và D.
Xét chất Y ta có: Anilin phản ứng được với nước ® Loại A ® Đáp án đúng là D.
Câu 33:
Cho các phát biểu sau:
(1) Mỡ động vật chủ yếu cấu thành từ các gốc axit béo chưa no.
(2) Phản ứng thủy phân este trong môi trường axit gọi là phản ứng xà phòng hóa.
(3) Tristearin, triolein có công thức lần lượt là: .
(4) Etyl fomat có phản ứng tráng bạc.
(5) Isoamyl axetat có mùi chuối chín.
(6) Este có tên gọi là etyl metacrylat.
Số phát biểu đúng là?
(1) Sai, mỡ động vật chủ yếu cấu thành từ các gốc axit béo no.
(2) Sai, phản ứng thủy phân este trong môi trường kiềm gọi là phản ứng xà phòng hóa.
(3) Sai, tristearin là và triolein là .
(4) Đúng, etyl fomat có phản ứng tráng bạc.
(5) Đúng, isoamyl axetat có mùi chuối chín.
(6) Đúng, este có tên gọi là etyl metacrylat.
Chọn đáp án A.
Câu 34:
Tiến hành các thí nghiệm sau:
(a) Cho Mg vào dung dịch dư
(b) Sục khí vào dung dịch
(c) Dẫn khí dư qua bột CuO nung nóng
(d) Cho Na vào dung dịch dư
(e) Nhiệt phân
(f) Điện phân nóng chảy
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kim loại là?
Phương trình xảy ra:
(a)
+ Nếu cho Mg tác dụng với dư thì chỉ dừng lại ở phản ứng (1) khi đó sản phẩm sẽ không có kim loại.
+ Nếu cho Mg dư tác dụng với thì xảy ra cả 2 phản ứng (1) và (2) khi đó sản phẩm thu được có chứa kim loại.
(b)
(c) ® sản phẩm có kim loại
Chọn đáp án C.
Câu 35:
Hòa tan hết m gam hỗn hợp X gồm (trong đó oxi chiếm 8% khối lượng hỗn hợp) vào nước dư, thu được dung dịch Y và 1,792 lít (đktc). Dung dịch Y có khả năng hòa tan tối đa 8,64 gam Al. Giá trị của m là?
.
Chọn đáp án C.
Câu 36:
Thực hiện phản ứng nhiệt nhôm hỗn hợp X gồm Al và 2,28 gam (trong điều kiện không có không khí), sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp Y. Cho toàn bộ Y vào một lượng dư dung dịch HCl (loãng, nóng), sau khi các phản ứng xảy ra hoàn toàn, thu được 1,008 lít (đktc). Còn nếu cho toàn bộ Y vào một lượng dư dung dịch NaOH (đặc, nóng), sau khi phản ứng kết thúc thì số mol NaOH đã phản ứng là?
Nếu Al không dư, dư
(đề bài) (vì Cr + HCl loãng ® )
® Chứng tỏ Y phải có Al dư và 0,03 mol Cr.
Như vậy .
Chọn đáp án A.
Câu 37:
Điện phân với điện cực trơ, có màng ngăn, dung dịch chứa m gam hỗn hợp hai muối NaCl và bằng dòng điện một chiều có cường độ ổn định. Đồ thị dưới đây biểu diễn mối liên hệ giữa thời gian điện phân và tổng số mol khí thoát ra ở hai điện cực?
Giá trị của m là?
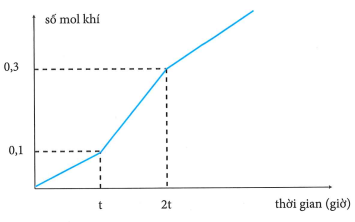
Thứ tự oxi hóa trên anot là: ; thứ tự khử trên catot là: .
Độ dốc đồ thị: Đoạn :
Chọn đáp án B.
Câu 38:
Hỗn hợp X gồm một este đơn chức mạch hở và ba este nhị chức, mạch hở, không phân nhánh là đồng phân của nhau. Đun nóng 11,88 gam X với 200 ml dung dịch NaOH 1,5M. Cô cạn dung dịch sau phản ứng thu được chất rắn Y và phần hơi chỉ chứa một ancol đơn chức Z. Cho toàn bộ lượng ancol Z vào bình Na dư, sau khi phản ứng xảy ra hoàn toàn thấy khối lượng bình Na tăng 5,85 gam. Trộn Y với CaO rồi nung trong điều kiện không có không khí, thu được 2,016 lít (đktc) một hidrocacbon duy nhất. Mặt khác đốt cháy 11,88 gam X cần 14,784 lít (đktc), thu được 25,08 gam. Este nào sau đây có mặt trong hỗn hợp X?
Theo đầu bài: Vì Z là ancol đơn chức ® Loại A (do xà phòng hóa tạo andehit) ® nhìn đáp án cũng đoán ancol Z là .
Áp dụng bảo toàn khối lượng, ta được:
Áp dụng bảo toàn nguyên tố O, ta được
® số mol nhóm
· Gọi công thức ancol đơn chức Z là ROH; công thức trung bình của 4 este là
; (chú ý sẽ có NaOH dư từ phản ứng xà phòng hóa)
Gọi công thức ba este hai chức là và công thức este đơn chức là .
.
® CTPT, CTCT este đơn chức là:
® CTPT, CTCT của ba este hai chức là:
Chọn đáp án C.
Câu 39:
Cho hỗn hợp X gồm peptit A mạch hở có công thức và hợp chất hữu cơ B có công thức phân tử là . Đốt cháy hoàn toàn 41,325 gam hỗn hợp X bằng lượng oxi vừa đủ thì thu được và 96,975 gam hỗn hợp và . Mặt khác, nếu lấy 0,09 mol X tác dụng vừa đủ với 0,21 mol NaOH chỉ thu được sản phẩm là dung dịch gồm ancol etylic và a mol muối của glyxin, b mol muối của alanin. Giá trị a : b gần nhất với?
Từ số nguyên tử N trong peptit A, ta có thể suy luận ra A là pentapeptit và B (thuỷ phân ra ancol) là
Với thí nghiệm 2:
Với thí nghiệm 1:
.
Vậy ở thí nghiệm sau
® Gần giá trị ở đáp án D nhất.
Câu 40:
Nung hỗn hợp X gồm Al, Fe và Cu (trong đó Cu chiếm 34,72% khối lượng) trong không khí một thời gian, thu được 6,17 gam hỗn hợp rắn Y gồm các kim loại và oxit tương ứng. Cho hỗn hợp Y tác dụng với dung dịch A chứa 0,36 mol và 0,04 mol . Sau phản ứng, thu được dung dịch B chỉ chứa 56,05 gam muối sunfat trung hòa (không làm mất màu thuốc tím) và thoát ra 336 ml hỗn hợp khí Z chứa các hợp chất của nitơ có . Cho dung dịch B tác dụng hoàn toàn với 170 ml dung dịch NaOH 2M thì thu được m gam kết tủa. Giá trị của m gần nhất với giá trị nào sau đây?
·
·
·
·
· (1)
Do Cu chiếm 34,72% về khối lượng trong X
· (2)
Từ (1), (2):
· ® lượng dùng để kết hợp các cation là:
· hòa tan
.
Chọn đáp án D.
