20 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án
20 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án ( Đề 10)
-
2018 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Kim loại nào sau đây là kim loại kiềm thổ?
Kim loại kiềm thổ là Ba.
Chọn đáp án B.
Câu 2:
Tinh bột trong gạo nếp có thành phần chính là?
Tinh bột trong gạo nếp, ngô nếp chứa lượng amilopectin rất cao, khoảng 90% làm cho cơm nếp, xôi nếp,... rất dẻo, dẻo đến mức dính.
Chọn đáp án B.
Câu 3:
Trong công nghiệp, kim loại nào sau đây có thể được sản xuất từ quặng hematit?
Trong công nghiệp, sắt được sản xuất từ quặng hematit (một dạng khoáng vật của oxit sắt Fe2O3).
Chọn đáp án B.
Câu 4:
Thuốc thử được dùng để phân biệt Gly - Ala - Gly và Gly - Ala là
Tripeptit Gly- Ala - Gly có 2 liên kết peptit nên có phản ứng màu với Cu(OH)2 tạo thành phức chất có màu tím đặc trưng (phản ứng màu biure).
Đipeptit Gly - Ala chỉ có 1 liên kết peptit nên không tham gia phản ứng này.
Chọn đáp án A.
Câu 5:
Hợp chất nào sau đây trong công thức cấu tạo có 9 liên kết xích ma (s) và 2 liên kết pi (p)?
Trong công thức cấu tạo của buta-1,3-đien: CH2=CH-CH=CH2 có 9 liên kết xích ma (s) và 2 liên kết pi (p).
Chọn đáp án C.
Câu 6:
Etyl propionat là este có mùi thơm của dứa. Công thức của etyl propionat là
Etyl propionat là este có mùi thơm của dứa, có công thức là: C2H5COOC2H5.
Chọn đáp án B.
Câu 7:
Thực hiện phản ứng nào sau đây để thu được bơ nhân tạo từ dầu thực vật?
Dầu thực vật chứa các gốc axit béo không no dạng lỏng, khi hiđro hóa dầu thực vật sẽ thu được bơ nhân tạo (chứa các gốc axit béo no, dạng rắn).
Chọn đáp án C.
Câu 8:
Axit e-aminocaproic được dùng để điều chế nilon-6. Công thức của axit e-amino- caproic là
Công thức của axit e-aminocaproic được dùng để điều chế nilon-6 là: H2N-(CH2)5-COOH.
Chọn đáp án D.
Câu 9:
Thủy phân este mạch hở X có công thức phân tử C4H6O2, thu được sản phẩm đều có khả năng tham gia phản ứng tráng bạc. Số công thức cấu tạo phù hợp của X là
Công thức cấu tạo của X thoả mãn là HCOOCH=CH-CH3.
Chọn đáp án D.
Câu 10:
Đun nóng hỗn hợp gồm glyxin, phenylalanin, tyrosin, valin, alanin tạo ra pentapeptit có chứa các gốc amino axit khác nhau. Số lượng pentapeptit có thể tạo ra là
Số pentapeptit tạo ra bởi 5 amino axit khác nhau là 5! = 120.
Chọn đáp án B.
Câu 11:
Giữ cho bề mặt kim loại luôn sạch, không để bùn đất bám vào, bôi dầu mỡ, quét sơn, là một trong các biện pháp để bảo vệ kim loại không bị ăn mòn. Như vậy là đã áp dụng phương pháp chống ăn mòn nào sau đây?
Giữ cho bề mặt kim loại luôn sạch, không để bùn đất bám vào, bôi dầu mỡ, quét sơn, chính là biện pháp cách li kim loại với môi trường, để bảo vệ kim loại không bị ăn mòn.
Chọn đáp án A.
Câu 12:
Cho phản ứng:
Sau khi cân bằng phản ứng trên, tổng hệ số tối giản của phản ứng là?
Ta có phương trình phản ứng sau khi cân bằng:
Chọn đáp án B.
Câu 13:
Phương trình hóa học nào sau đây không đúng?
Phương trình phản ứng không đúng là:
Do đúng phải là:
Chọn đáp án D.
Câu 14:
Cho dãy các chất: axit acrylic, phenyl axetat, anlyl axetat, metylamoni axetat, etyl fomat, tripanmitin. Số chất trong dãy khi thủy phân trong dung dịch NaOH (dư), đun nóng sinh ra ancol là
Các chất thoả mãn khi thủy phân trong dung dịch NaOH (dư), đun nóng sinh ra ancol là: anlyl axetat, etyl fomat, tripanmitin.
Chọn đáp án D.
Câu 15:
Môi trường không khí, đất, nước xung quanh một số nhà máy hoá chất thường bị ô nhiễm nặng bởi khí độc, ion kim loại nặng và các hoá chất. Biện pháp nào sau đây cần phải được thực hiện nhằm chống gây ô nhiễm môi trường?
Để tránh gây ô nhiễm môi trường sống, các nhà máy hóa chất cần phải lắp đặt các hệ thống xử lí chất thải trước khi xả ra ngoài hệ thống không khí, sông, hồ, biển. Quá trình sản xuất cần được thực hiện theo quy trình khép kín để tận dụng lượng chất thải một cách hiệu quả. Ngoài ra, cần thường xuyên thay đổi công nghệ sản xuất, sử dụng nhiên liệu sạch.
Chọn đáp án D.
Câu 16:
Nhiệt phân hoàn toàn 9,4 gam muối nitrat của kim loại M hóa trị II. Thu được 4,0 gam oxit kim loại tương ứng. M là kim loại:
Phương trình phản ứng nhiệt phân:
mol: a 2a 0,5a
mKhí = mrắn giảm
Theo đầu bài:Câu 17:
Cho các polime sau đây: (1) tơ tằm ; (2) sợi bông; (3) sợi đay; (4) tơ enang; (5) tơ visco; (6) nilon-6,6 ; (7) tơ axetat. Loại tơ có nguồn gốc xenlulozơ là:
Các loại tơ có nguồn gốc xenlulozơ là: sợi bông, sợi đay, tơ visco, tơ axetat.
Chọn đáp án B.
Câu 18:
Cho 2,13 gam P2O5 tác dụng với 80 ml dung dịch NaOH 1M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X chứa m gam muối B. Qua sự thủy phân của các ion, giá trị của m là
Theo đầu bài ta có:
Chọn đáp án A.
Câu 19:
Chọn đáp án A.
Câu 20:
Hỗn hợp X gồm alanin và axit glutamic. Cho a gam X tác dụng hoàn toàn với dung dịch NaOH (dư), thu được dung dịch Y chứa (a + 30,8) gam muối. Mặt khác, nếu cho a gam X tác dụng hoàn toàn với dung dịch HCl, thu được dung dịch Z chứa (a +36,5) gam muối. Giá trị của a là:
Đặt số mol của H2N - CH(CH3) - COOH là x và của HOOC - (CH2)2 - CH(NH2) –COOH là y.
Phương trình phản ứng: - COOH + NaOH ® - COONa + H2O (1)
mol: (x + 2y) ® (x + 2y)
-NH2 + HCl ® -NH3Cl (2)
mol: (x + y) ® (x + y) ® (x + y)
Theo (1), (2) và giả thiết ta có:
Chọn đáp án A.
Câu 21:
mrắn giảm loại A, B.
Ta có hệ phương trình:
® loại D.
Chọn đáp án C.
Câu 22:
Vì hiệu suất phản ứng thủy phân là 75% nên tổng số mol mantozơ và saccarozơ tham gia phản ứng thủy phân là:
Số mol của mantozơ dư sau phản ứng thủy phân là
Sơ đồ phản ứng: C12H22O11 (gồm mantozơ và saccarozơ phản ứng) ® 2C6H12O6 ® 4Ag (1)
mol: 0,0225 ® 0,045 ® 0,09
C12H22O11 (mantozơ dư) ® 2Ag (2)
mol: 0,0025 0,005
Saccarozơ dư không tham gia phản ứng tráng gương.
Theo sơ đồ (1) và (2) suy ra tổng số mol Ag tạo ra là 0,095 mol.
Chọn đáp án B.
Câu 23:
Dung dịch X chứa x mol K2CO3 và y mol NaHCO3. Thực hiện các thí nghiệm sau: Thí nghiệm 1 (TN1): Cho (x + y) mol CaCl2 vào dung dịch X, thu được m1 gam kết tủa.
Thí nghiệm 2 (TN2): Cho (x + y) mol Ca(OH)2 vào dung dịch X, thu được m2 gam kết tủa. Khối lượng kết tủa thu được trong 2 TN là:
Ở thí nghiệm 1:
CaCl2 + K2CO3 ® CaCO3 ¯ +2KCl
mol: x x x
Ở thí nghiệm 2:
Ca(OH)2 + K2CO3 ® CaCO3 ¯ +2KOH
mol: x x x
Ca(OH)2 + NaHCO3 ® CaCO3 ¯ + NaOH + H2O
mol: y y y
Từ (1) và (2)
Câu 24:
Trộn 100 ml dung dịch A gồm KHCO3 1M và K2CO3 1M vào 100 ml dung dịch B gồm NaHCO3 1M và Na2CO3 1M thu được dung dịch C. Nhỏ từ từ 100 ml dung dịch D gồm H2SO4 1M và HC1 1M vào dung dịch C thu được V lít CO2 (đktc) và dung dịch E. Cho dung dịch Ba(OH)2 tới dư vào dung dịch E thì thu được m gam kết tủa. Giá trị của m và V lần lượt là:
Dung dịch C chứa:
Dung dịch D có tổng:
Nhỏ từ từ dung dịch D vào dung dịch C:
Tiếp tục xảy ra phản ứng:
Trong dung dịch E còn 0,3 mol HCO3-. Tiếp tục cho dung dịch Ba(OH)2 dư vào E
Þ Khối lượng kết tủa là:
Chọn đáp án D.
Câu 25:
Một chất hữu cơ X có công thức phân tử là C4H11NO2. Cho X tác dụng hoàn toàn với 100 ml dung dịch NaOH 2M, sau phản ứng thu được dung dịch Y và 2,24 lít khí Z (đktc). Nếu trộn lượng khí Z này với 3,36 lít H2 (đktc) thì được hỗn hợp khí có tỉ khối so với H2 là 9,6. Khối lượng chất rắn thu được khi cô cạn dung dịch Y là
X (C4H11NO2) + NaOH ® Z ® Z là NH3 hoặc amin, X là muối amoni.
Theo đầu bài, ta có:
Ta có:
Chọn đáp án D.
Câu 26:
Theo giả thiết ta có:
Phương trình phản ứng:
Theo các phương trình phản ứng và giả thiết ta có:
Vậy phần trăm khối lượng ancol bị oxi hóa là:
Chọn đáp án C.
Câu 27:
Hỗn hợp A gồm 1 axit no đơn chức (mạch hở) và một axit không no đơn chức mạch hở có một liên kết đôi ở gốc hiđrocacbon. Khi cho a gam A tác dụng hết với CaCO3 thoát ra 1,12 lít CO2 (đktc). Cho 7,8 gam hỗn hợp B gồm CH3OH và C2H5OH tác dụng hết với Na thoát ra 2,24 lít H2 (đktc). Nếu trộn a gam A với 3,9 gam B rồi đun nóng có H2SO4 đặc xúc tác thì thu được m gam este (hiệu suất H%). Giá trị m theo a, H là:
Đặt công thức trung bình của hai axit trong X là
Đặt công thức trung bình của hai ancol trong Y là
Phương trình phản ứng:
Theo (1), (2) và giả thiết ta có:
Như vậy khi cho a gam hỗn hợp axit phản ứng với 3,9 gam hỗn hợp ancol thì số mol đem phản ứng của axit và ancol đều bằng nhau và bằng 0,1 mol.
Với hiệu suất 100% thì khối lượng este thu được là:
Trên thực tế hiệu suất phản ứng este hóa là H% nên khối lượng este thu được là:
Chọn đáp án B.
Câu 28:
Este X mạch hở có công thức phân tử C7H10O4. Từ X thực hiện các phản ứng sau:
Các phương trình phản ứng xảy ra như sau:
A. Đúng, X có mạch cacbon không phân nhánh.
B. Đúng, đun nóng X3 với H2SO4 đặc (170°C), thu được chất Z.
C. Sai, trong Y có số nguyên tử cacbon nhỏ hơn số nguyên tử hidro.
D. Đúng, X3 có nhiệt độ sôi cao hơn X2.
Chọn đáp án C.
Câu 29:
Đặt công thức phân tử của hiđrocacbon là CnH2n+2-2k (k là số liên kết pi trong phân tử).
Các phản ứng:
Theo giả thiết và phương trình phản ứng ta thấy:
Vì hiđrocacbon ở thể khí nên và từ (3) suy ra (vì hợp chất có 1 C không thể có liên kết p).
• Nếu thì hiđrocacbon là
• Nếu thì hiđrocacbon là C3H2 (loại).
• Nếu thì hiđrocacbon là
Câu 30:
Để phân tích định tính các nguyên tố trong hợp chất hữu cơ, người ta thực hiện một thí nghiệm được mô tả như hình vẽ:
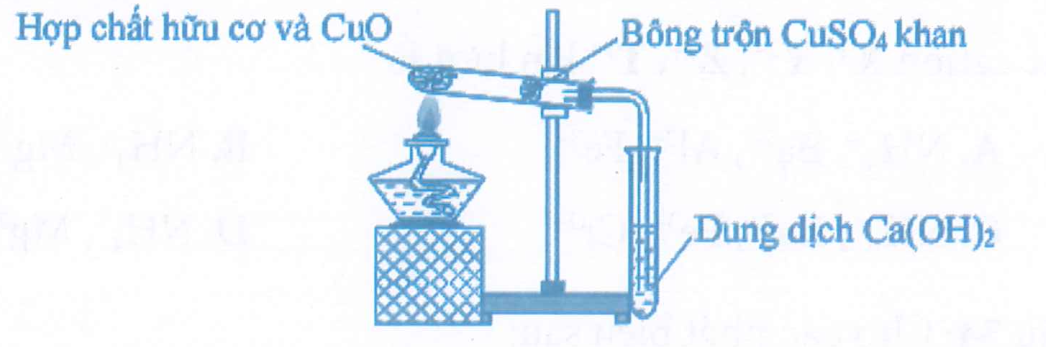
Phát biểu đúng là: Thí nghiệm trên dùng để xác định sự có mặt của C và H trong các hợp chất hữu cơ.
Chọn đáp án B.
Câu 31:
X, Y là hai peptit mạch hở, có tổng số nguyên tử oxi là 9 và đều được tạo bởi từ glyxin và valin. Đốt cháy m gam hỗn hợp E chứa X, Y cần dùng 2,43 mol O2, thu được CO2, H2O, N2; trong đó khối lượng của CO2 nhiều hơn khối lượng của H2O là 51,0 gam. Mặt khác thủy phân hoàn toàn m gam E với 600ml dung dịch KOH 1,25M (đun nóng), cô cạn dung dịch sau phản ứng thu được (1,6m + 8,52) gam rắn khan. Phần trăm khối lượng của Y (Mx < My) có trong hỗn hợp E là
Đặt Đ. chéo:
Chọn đáp án A.
Câu 32:
Cho các phát biểu sau:
(1) Điều chế kim loại Al bằng cách điện phân nóng chảy A12O3;
(2) Tất cả kim loại kiềm thổ đều tan trong nước ở nhiệt độ thường;
(3) Quặng boxit có thành phần chính là Na3AlF6;
(4) Bột nhôm tự bốc cháy khi tiếp xúc với khí clo;
(5) Thạch cao sống có công thức là CaSO4.2H2O;
(6) Đun nóng có thể làm mềm nước có tính cứng vĩnh cửu.
Số phát biểu đúng là
Phát biểu đúng là (1), (4), (5).
(2) Sai, do Ba không tác dụng với nước dù ở nhiệt độ cao, Mg không tác dụng với nước ở nhiệt độ thường.
(3) Sai, do quặng boxit có thành phần chính là Al2O3, Na3AlF6 là criolit.
(6) Sai, chỉ làm mềm được nước cứng tạm thời.
Chọn đáp án B.
Câu 33:
Kết quả thí nghiệm với các dung dịch muối clorua riêng biệt của các cation: X+, Y2+, Z3+, T3+ được ghi vào bảng dưới đây:
|
Mẫu thử |
Thí nghiệm |
Hiện tượng |
|
X+ |
Tác dụng với dung dịch NaOH |
Có mùi khai |
|
Y2+ |
Tác dụng với dung dịch Na2SO4 |
Kết tủa trắng |
|
Z3+ |
Nhỏ từ từ dung dịch NH3 vào đến dư |
Kết tủa keo trắng |
|
T3+ |
Tác dụng với dung dịch Na2CO3 |
Kết tủa nâu đỏ và có khí không màu thoát ra |
Các cation X+, Y2+, Z3+, T3+ lần lượt là
Y2+ tác dụng với dung dịch Na2SO4 có kết tủa trắng ® loại B và D.
Z3+ tác dụng với dung dịch NH3 dư ® tạo kết tủa keo trắng không tan ® loại C.
Chọn đáp án A.
Câu 34:
Cho các phát biểu sau:
(a) Phản ứng thủy phân este trong môi trường kiềm là phản ứng một chiều.
(b) Trong phản ứng điều chế este, người ta thường thêm cát (SiO2) để xúc tác cho phản ứng.
(c) Hiđro hóa glucozơ (xt, t°), thu được sobitol.
(d) "Da giả" được tổng hợp từ phản ứng trùng ngưng amino axit.
(e) Thủy phân hoàn toàn các peptit trong dung dịch kiềm, thu được các amino axit.
(f) Dung dịch các amin có vòng benzen đều không làm đổi màu quỳ tím.
Số phát biểu đúng là
(a) Đúng.
(b) Sai, trong phản ứng điều chế este, người ta thường cho thêm H2SO4 đặc để xúc tác cho phản ứng.
(c) Đúng.
(d) Sai, "Da giả" được tổng hợp từ phản ứng trùng hợp vinyl clorua.
(e) Sai, thủy phân hoàn toàn các peptit trong dung dịch kiềm, thu được muối của các amino axit.
(f) Sai, C6H5CH2NH2 làm quỳ tím hoá xanh.
Chọn đáp án C.
Câu 35:
Cho 100 ml dung dịch hỗn hợp X chứa A12(SO4)3 a M, MgCl2 b M, và H2SO4 c M. Đổ từ từ V lít dung dịch hỗn hợp Y gồm KOH 0,6M và Ba(OH)2 0,2M, kết quả thí nghiệm thu được cho trong hình sau.
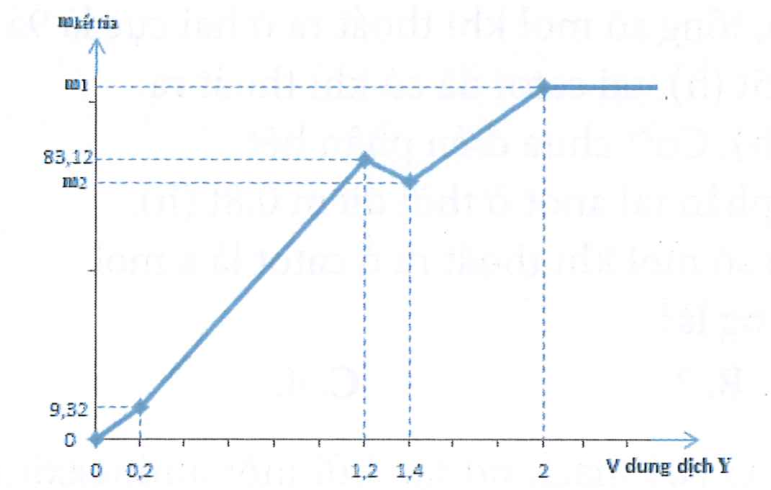
Giá trị m1 + m2 là:
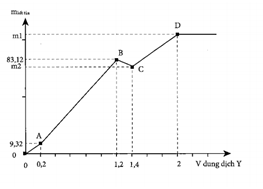
Từ dung dịch Y:
Từ A: Thông qua Có thể coi đoạn đầu, chưa có kết tủa hidroxit
Tại điểm B, toàn bộ và kết tủa hết.
(khi không có điểm gãy, Al3+ và Mg2+ sẽ kết tủa đồng thời)
Từ số mol
Lúc này:
Vì sau đó kết tủa còn tăng dư.
Từ khối lượng kết tủa:
Hệ:
Tại D: Kết tủa cực đại,
Chọn đáp án C.
Câu 36:
Tiến hành các thí nghiệm sau:
(a) Cho Mg vào dung dịch Fe2(SO4)3 dư; (b) Sục khí Cl2 vào dung dịch FeCl2;
(c) Dẫn khí H2 dư qua bột CuO nung nóng; (d) Cho Na vào dung dịch CuSO4 dư;
(e) Nhiệt phân AgNO3; (g) Đốt FeS2 trong không khí;
(h) Điện phân dung dịch CuSO4 với điện cực trơ;
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kim loại là:
Các phản ứng xảy ra như sau:
Sau khi kết thúc các phản ứng, thí nghiệm thu được kim loại: (c), (e), (h).
® Số thí nghiệm thu được kim loại là 3.
Chọn đáp án A.
Câu 37:
Nung nóng 1,26 mol hỗn hợp X gồm Mg, Fe(NO3)2 và FeCO3 trong một bình kín đến khối lượng không đổi thu được chất rắn Y và 13,44 lít hỗn hợp khí Z (đktc) có tỉ khối đối với H2 là 22,8. Cho toàn bộ chất rắn Y tác dụng với dung dịch hỗn hợp 2,7 mol HCl và 0,38 mol HNO3 đun nhẹ thu được dung dịch A và 7,168 lít hỗn hợp khí B (đktc) gồm NO và N2O. Cho toàn bộ dung dịch A tác dụng với một lượng dư dung dịch AgNO3 thu được 0,448 lít NO (đktc) là sản phẩm khử duy nhất và m gam kết tủa. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
Vì Y còn tính khử nên Z không chứa O2.
Theo đề ta có:
Quy đổi Y thành và đặt với
Cho A tác dụng với AgNO3 thoát khí NO (0,02 mol) nên A chứa H+ dư (0,08) và A không chứa NO3-
và
Từ (1), (2), (3) suy ra:
Câu 38:
Cho các chất hữu cơ sau đây: X là axit cacboxylic không no, đơn chức (chứa 2 liên kết p); Y là axit cacboxylic no, đơn chức; Z là ancol no; T là este mạch hở, 3 chức, tạo từ X, Y và Z (chứa 5 liên kết p). Cho 26,5 gam hỗn hợp E gồm X, Y, Z, T tác dụng vừa đủ với 250 ml dung dịch NaOH 1M, thu được 20,9 gam hỗn hợp muối F và 13,8 gam ancol Z. Toàn bộ Z tác dụng với Na dư, thu được 5,04 lít H2 (đktc). Nung F với NaOH dư và CaO ở nhiệt độ cao, thu được hỗn hợp khí Q có tỉ khối so với H2 là 8,8. Các phản ứng xảy ra hoàn toàn. Phần trăm theo khối lượng của X trong E gần nhất với giá trị nào sau đây?
Theo đề, X là axit không no, có 1 liên kết C=C đơn chức và T là este ba chức được tạo thành từ 2 phân tử chất X, 1 phân tử chất Y và 1 ancol Z ba chức.
Từ phản ứng của Z với Na
Khi cho E tác dụng với
Ta có: Muối thu được gồm HCOONa hoặc CH3COONa và RCOONa.
+ Xét muối HCOONa (a mol) và RCOONa (b mol)
Vậy X là
Chọn đáp án D.
Câu 39:
Điện phân (với điện cực trơ, màng ngăn) dung dịch chứa hỗn hợp CuSO4 và NaCl (tỉ lệ mol 1:1) bằng dòng điện một chiều có cường độ ổn định. Sau t (h), thu được dung dịch X và sau 2t (h), thu được dung dịch Y. Dung dịch X tác dụng với bột Al dư, thu được a mol khí H2. Dung dịch Y tác dụng với bột Al dư, thu được 4a mol khí H2. Cho các phát biểu sau:
(1) Tại thời điểm 2t (h), tổng số mol khí thoát ra ở hai cực là 9a mol.
(2) Khi thời gian là 1,75t (h), tại catot đã có khí thoát ra.
(3) Tại thời điểm 1,5t (h), Cu2+ chưa điện phân hết.
(4) Nước bắt đầu điện phân tại anot ở thời điểm 0,8t (h).
(5) Tại thời điểm 2t (h) số mol khí thoát ra ở catot là a mol.
Số phát biểu không đúng là?Xét tại thời điểm t(h); dung dịch sau điện phân hòa tan Al sinh ra H2 mà tỷ lệ CuSO4 : NaCl = 1 : 1
® Đặt số mol CuSO4 và NaCl đều là b mol.
Ở catot: Cu2+ + 2e ® Cu0; ở anot: 2Cl- - 2e ® Cl2 ; 2H2O - 4e ® 4H+ + O2.
Dung dịch X phản ứng với Al sinh ra a mol H2 ® lượng H+ đã phản ứng = 2a mol.
® Số mol e trao đổi = b + 2a mol.
■ Xét tại thời điểm 2t(h), số mol e trao đổi = 2 (2a + b) mol.
Ở catot:
Cu2+ + 2e ® Cu0 ; 2H2O + 2e ® 2OH- + H2 ½½ Ở anot: 2Cl- - 2e ® Cl2 ; 2H2O - 4e ® 4H+ + O2.
Số mol e Cl- nhường = b mol ® số mol e H2O nhường = 4a + b mol ® Lượng H+ sinh ra = 4a + b
Số mol e Cu2+ nhận = 2b mol ® Số mol e H2O nhận = 4a mol ® số mol OH- = 4a mol. Trong dung dịch có OH- và H+ nên: H+ + OH- ® H2O.
® Lượng H+ dư = b mol.
Cho Al dư vào dung dịch: Al + 3H+ ® Al3+ + 3/2 H2.
® Số mol H2 = b /2 = 4a ® a : b = 1 : 8
■ Xét các nhận định:
+ Tại thời điểm 2t(h) số mol khí thoát ra ở hai cực là: 2a + 0,5 b + 0,25(4a + b), thay b = 8a ® số mol khí thoát ra = 9a mol ® (1) đúng.
+ Tại thời điểm 1,75t(h) thì số mol e trao đổi = 1,75 (2a + b) mol.
Nếu H2O điện phân thì Cu2+ điện phân hết ® số mol e Cu2+ nhận = 2b mol <1,75 (2a + b) ® 0,25b < 3,5a ® b : a < 14 đúng (do b : a = 8) ® (2) đúng.
+ Tại thời điểm 1,5t(h) thì số mol e trao đổi =1,5 (2a + b) mol.
Nếu H2O điện phân thì Cu2+ điện phân hết ® số mol e Cu2+ nhận = 2b mol < 1,5 (2a + b)
® 0,5b < 3a ® a : b > 1 / 6 ® sai (do a : b = 1 : 8) ® Cu2+ chưa điện phân hết ® (3) đúng.
+ Tại thời điểm 0,8t (h) thì số mol e trao đổi = 0,8 (2a + b) mol.
Nếu H2O điện phân thì Cl- vừa bị điện phân hết ® số mol e Cl- nhường là b mol = 0,8 (2a + b)
® 0,2b = 1,6 a ® a : b = 1 / 8 đúng (do a : b = 1: 8) ® (4) đúng.
+ Tại thời điểm 2t (h) thì số mol H2 sinh ra = 2a mol ® (5) sai.
Chọn đáp án A.
Câu 40:
Peptit X (CxHyOzN6) mạch hở tạo bởi một aminoaxit no chứa 1 nhóm NH2 và 1 nhóm COOH. Để phản ứng hết 19 gam hỗn hợp E chứa X, este Y (CnH2n-2O4) và este Z (CmH2m-4O6) cần 300 ml dung dịch NaOH 1M thu được hỗn hợp muối và hỗn hợp gồm 2 ancol có cùng số cacbon. Lấy toàn bộ muối nung với vôi tôi xút được hỗn hợp F chứa 2 khí có tỉ khối so với H2 là 3,9. Đốt cháy 19 gam E cần 0,685 mol O2 thu được 9,72 gam H2O. Thành phần phần trăm khối lượng của X trong E gần nhất với:
Nhận thấy Y, Z đều là hợp chất no, đa chức.
F chứa 2 khí có F chứa H2 ® muối chứa HCOONa.
F chứa 2 khí, 1 khí sinh ra từ muối của amino axit, 1 khí sinh ra từ muối của este.
® Este Y, Z có dạng (HCOO)nR ® Quy đổi hỗn hợp E theo đồng đẳng hóa:
BTKL khi đốt cháy E:
Ta có hệ phương trình:
Do d=0 nên các chất trong E chính là các chất mà ta quy đổi được ® X là Gly6.
Chọn đáp án C.
