25 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án
25 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án (Đề 3)
-
3497 lượt thi
-
40 câu hỏi
-
90 phút
Danh sách câu hỏi
Câu 1:
X là kim loại cứng nhất, được sử dụng để mạ các dụng cụ kim loại, chế tạo các loại thép chống gỉ,... Kim loại X là
Đáp án A
Kim cương cao nhất > Cr > W > Fe > Cu > Al.
Độ cứng của kim loại:
Thấp nhất: kim loại nhóm IA: Cs thấp nhất
Câu 2:
Đáp án B
Kim loại kiềm gồm: Li, Na, Cs.
Câu 4:
Công thức phân tử của este etyl propionat là
Đáp án D
Công thức của este: CH3CH2COOCH2CH3Câu 5:
Dung dịch nào sau đây không tác dụng với Al2O3 ?
Đáp án B
A12O3 là oxit lưỡng tính, vừa tác dụng với axit, vừa tác dụng với dung dịch bazơ.
Câu 6:
Amin nào sau đây không phải là chất khí ở điều kiện thường?
Đáp án D
Các amin là chất khí ở điều kiện thường: metylamin, etylamin, đimetylamin, trimetylamin.
Câu 7:
Trong công nghiệp, khí nitơ được điều chế từ
Đáp án A
Trong công nghiệp, nitơ được điều chế bằng cách chưng cất phân đoạn không khí lỏng.
Câu 9:
Đáp án C
CT của nilon-6,6: .
Các mắt xích nối với nhau bằng liên kết –CONH–.
Câu 10:
Đáp án C
- Cu và Ag không phản ứng với HCl.
- Fe + 2HCl → FeCl2 + H2.
- 2Fe + 3C12 → 2FeCl3.
- 2Al + 6HCl → 2AlC13 + 3H2.
- 2Al + 3Cl2 → 2AlCl3.
Câu 11:
Đisaccarit và polisaccarit tham gia phản ứng thủy phân trong môi trường axit tạo thành monosaccarit.
Câu 12:
Đáp án C
Có 4 đồng phân:
(1) CH3CH2CH2CH2OH (2) (CH3)2CHCH2OH
(3) CH3CH2CH(OH)CH3 (4) (CH3)3COH
Câu 13:
Cho phương trình hóa học của 2 phản ứng sau:
FeO + CO → Fe + CO2.
3FeO + 10HNO3 → 3Fe(NO3)3 + NO + 5H2O.
Hai phản ứng trên chứng tỏ FeO là chất
Đáp án D
(2): FeO thể hiện tính khử.
(1): FeO thể hiện tính oxi hóa.
Câu 14:
Đáp án A
2M + 2H2O → 2MOH + H2
Câu 15:
Đáp án B
PTHH:
C6H5CH2NH3Cl + NaOH → C6H5CH2NH2 + NaCl + H2O
HCOOH + NaOH → HCOONa + H2O
HCOOCH3 + NaOH → HCOONa + CH3OH
Câu 16:
Hỗn hợp X gồm hai chất là glucozơ và fructozơ có khối lượng là 27 gam. Cho X tác dụng với một lượng dư AgNO3 trong NH3 thu được m gam kết tủa. Tính giá trị của m
Đáp án B
Glucozơ 2Ag
Fructozơ 2Ag
mol
mol
gam.
Câu 17:
Để trung hòa 25 gam dung dịch của một amin đơn chức X nồng độ 12,4% cần dùng 100 ml dung dịch HCl 1M. Công thức phân tử của X là
Đáp án A
RNH2 + HCl → RNH3Cl
mol
là CH5N.
Câu 18:
Đáp án D
Phản ứng của hợp chất hữu cơ thường xảy ra không hoàn toàn và không theo hướng nhất định.
Câu 19:
Chất nào sau đây thuộc loại điện li mạnh?
Đáp án B
PT điện li: NaCl → .
|
Những chất điện ly mạnh bao gồm: - Axit mạnh: H2SO4, HCl, HNO3 - Bazơ mạnh: LiOH, KOH, NaOH, Ca(OH)2, Ba(OH)2 - Muối tan: NaCl, CuSO4, FeCl2,… |
Câu 20:
Cho các phát biểu sau:
(a) Saccarozơ, tinh bột, xenlulozơ đều có thể bị thủy phân.
(b) Glucozơ, fructozơ đều tham gia phản ứng tráng bạc.
(c) Tinh bột và xenlulozơ là đồng phân của nhau.
(d) Glucozơ làm mất màu dung dịch Br2.
Trong các phát biểu trên, số phát biểu đúng là
Đáp án C
Những phát biểu đúng: (a), (b), (d).
(c) sai vì tinh bột và xenlulozơ không phải là đồng phân của nhau.
Câu 21:
Người ta có thể bảo vệ vỏ tàu biển bằng thép bằng cách gắn những tấm Zn vào vỏ tàu ở phần chìm trong nước biển vì
Đáp án A
Đây là cách bảo vệ vỏ tàu biển bằng thép bằng phương pháp điện hóa.
Câu 22:
Cho sơ đồ chuyển hóa:
Triolein X Y Z
Tên của Z là
Đáp án D
(C17H33COO)3C3H5 (C17H35COO)3C3H5 C17H35COONa C17H35COOH
Câu 23:
Tiến hành các thí nghiệm sau:
(1) Cho Cu(OH)2 vào dung dịch lòng trắng trứng.
(2) Cho dung dịch iot vào dung dịch hồ tinh bột ở nhiệt độ thường.
(3) Cho Cu(OH)2 vào dung dịch glixerol.
(4) Cho Cu(OH)2 vào dung dịch axit axetic.
(5) Cho Cu(OH)2 vào dung dịch propan-1,3-điol.
Màu xanh xuất hiện ở những thí nghiệm nào?
Đáp án D
Hiện tượng các thí nghiệm:
(1) tím.
(2) xanh tím.
(3) xanh lam.
(4) xanh lam.
(5) không có hiện tượng.
|
Những chất hữu cơ tác dụng được với Cu(OH)2: - Chất có từ 2 nhóm chức hiđroxyl () liền kề trở lên, tạo dung dịch xanh lam. - Axit hữu cơ (): tạo dung dịch xanh lam. - Chất có nhóm chức anđehit (): khi đun nóng tạo kết tủa đỏ gạch. - Pepit có từ 2 liên kết peptit trở lên: tạo phức tím đặc trưng. |
Câu 24:
Fe có màu trắng, dẻo, dễ rèn.
Câu 25:
Đáp án B
2MCl 2M + Cl2
mol
Muối clorua là NaCl.
Câu 26:
Đáp án D
(RCOO)3C3H5 + 3NaOH -↓ 3RCOONa + C3H5 (OH)3
mol
BTNT:
|
Đối với dạng bài tập chất béo, ngoài cách làm trên, nhiều học sinh còn giải quyết theo cách tìm ra công thức hóa học của chất béo, từ đó tính khối lượng xà phòng. Cách làm này giải quyết được bài toán nhưng việc tính toán lâu hơn và khó áp dụng cho những bài tính toán có sự biến đổi phức tạp hơn nên áp dụng phương pháp bảo toàn khối lượng là phương pháp hiệu quả cho dạng bài này. |
Câu 27:
Phát biểu nào sau đây là đúng?
Đáp án D
A sai vì đây là phản ứng thuận nghịch.
B sai vì phản ứng có thể sinh ra anđehit, xeton và nước.
C sai vì thủy phân chất béo thu được glixerol có công thức C3H5(OH)3
Câu 28:
Cho hình vẽ mô tả thí nghiệm điều chế khí Cl2 trong phòng thí nghiệm:
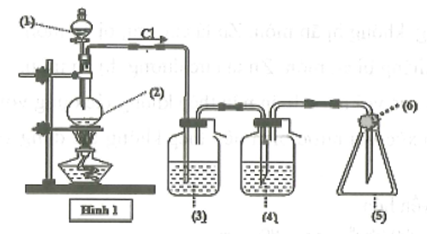
Trong phễu (1) chứa dung dịch nào sau đây?
Đáp án D
MnO2 + 4HCl MnCl2 + Cl2 + 2H2O
|
Vai trò của các bình (3) và (4) giúp khí Cl2 thu được tinh khiết. - Bình (3) chứa NaCl bão hòa dùng để giữ HCl lại. - Bình (4) chứa H2SO4 đặc giúp giữ nước lại. Bông (6) tẩm NaOH giúp ngăn khí Cl2 thoát ra ngoài. |
Câu 29:
Cho 61,2 gam hỗn hợp gồm Cu và Fe3O4 tác dụng với HNO3 đun nóng, khuấy đều. Sau khi các phản ứng xảy ra hoàn toàn thu đuợc 3,36 lít khí NO duy nhất (đktc), dung dịch Y và còn lại 2,4 gam kim loại. Cô cạn dung dịch Y thu được m gam muối khan. Giá trị của m là
Đáp án A
Kim loại còn lại 2,4 gam là Cu.
→ khối lượng hỗn hợp đã tham gia phản ứng là gam
mol
Quá trình nhường nhận e:
x 2x 3y 2y
0,45 0,15
mol
mol
Bảo toàn điện tích trong dung dịch Y: mol
gam.
Câu 30:
Hỗn hợp X gồm C2H2, C3H6, C4H10 và H2. Cho 11,2 lít (đktc) hỗn hợp X qua bình đựng dung dịch brom dư thấy có 64 gam brom tham gia phản ứng. Mặt khác, đốt cháy hoàn toàn 11,2 lít (đktc) hỗn hợp X được 55 gam CO2 và m gam nước. Giá trị của m là
Đáp án B
mol
gam.
Câu 31:
Hỗn hợp X gồm Na, Ba và Al. Cho m gam X vào dung dịch NaOH dư thu được 12,32 lít H2 (đktc). Cũng m gam X tác dụng với dung dịch HCl dư thu được dung dịch Y và H2. Cô cạn Y thu được 66,1 gam muối khan. Giá trị của m là
Đáp án B
X tác dụng với dung dịch NaOH hay dung dịch HCl, thì quá trình nhường nhận e đều như sau:
BTKL:
Câu 32:
Cho sơ đồ chuyển hóa sau:
(1) C4H6O2 (A) + NaOH → (B) + (C)
(2) (C) + AgNO3 + NH3 + H2O → (D) + NH4NO3 + Ag ↓
(3) (D) + NaOH → (B) + NH3+H2O
Công thức của A là
Đáp án B
(1) CH3COOCH=CH2 +NaOH CH3COONa + CH3CHO
(2) CH3CHO + 2AgNO3 + 3NH3 + H2O CH3COONH4 + 2NH4NO3 + 2Ag
(3) CH3COONH4 +NaOH CH3COONa + NH3 +H2O
Câu 33:
Cho hỗn hợp X gồm Mg, Al vào 200 ml dung dịch CuCl2 0,75M và FeCl3 0,60M. Sau khi kết thúc các phản ứng, thu được dung dịch Z và chất rắn Y. Cho dung dịch NaOH dư vào dung dịch Z, thấy lượng NaOH phản ứng là 28,80 gam. Cho toàn bộ Y vào dung dịch H2SO4 loãng dư, thấy thoát ra 4,704 lít khí H2 (đktc). Biết các phản ứng đều xảy ra hoàn toàn. Phần trăm khối lượng của Al trong hỗn hợp X là
Đáp án C
→ Kết tủa Al(OH)3 tan tiếp trong NaOH.
Nên mol
hỗn hợp Y chứa Al dư, đồng thời dung dịch Z không chứa ion của Fe, tức là FeCl3 phản ứng hết.
mol
BT e: mol
BTĐT trong dung dịch Z: mol
mol
.
Câu 34:
Hỗn hợp X gồm triolein và hai oligopeptit mạch hở có cùng số nguyên tử cacbon. Đốt cháy hoàn toàn 0,2 mol X cần dùng 3,265 mol O2, sản phẩm cháy gồm CO2, H2O và N2 được dẫn qua dung dịch nước vôi trong lấy dư, thu được 258,0 gam kết tủa. Mặt khác, đun nóng 0,2 mol X cần dùng 360 ml dung dịch NaOH 2M, cô cạn dung dịch sau phản ứng thu được hỗn hợp Y gồm ba muối, trong đó có hai muối của glyxin và alanin. Phần trăm khối lượng của oligopeptit có khối lượng phân tử nhỏ là
Đáp án C
nên có peptit chỉ chứa glyxin.
2 hoặc 3
Từ các dữ kiện trên → Peptit
|
Đối với dạng bài peptit mà việc tính toán tìm ra các chất gặp khó khăn, nên sử dụng phương pháp biện luận. Các cách biện luận chủ yếu của bài tập peptit: Tỉ lệ: chính là số amino axit trung bình của hỗn hợp peptit. Ví dụ: hỗn hợp 2 peptit hơn kém nhau 1 liên kết peptit có số amino axit trung bình là 5,3 chứng tỏ 2 peptit đó là pentapeptit và hexapeptit. Tỉ lệ: chính là số gốc CH2 trung bình trong peptit. Ví dụ: tính được số gốc CH2 trung bình bằng 0,8 thì chứng tỏ trong hỗn hợp peptit có chứa peptit chỉ chứa amino axit là gly. Tùy từng dạng bài cụ thể mà biến đổi phương pháp biện luận sao cho phù hợp để giải quyết yêu cầu bài toán. |
Câu 35:
Cho m gam hỗn hợp gồm Na2O và Al2O3 vào 400 ml dung dịch H2SO4 0,3M và HCl 0,9M. Sau khi kết thúc phản ứng, thu được dung dịch X. Cho dung dịch Ba(OH)2 dư vào X, phản ứng được biểu diễn theo đồ thị sau:
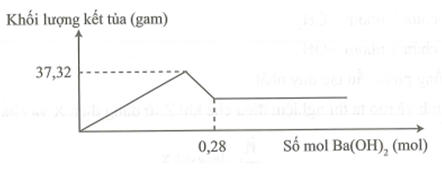
Giá trị của m là?
Đáp án C
Khi kết tủa không đổi là lúc kết tủa Al(OH)3 tan hết
0,12 0,36
0,12 0,12
Lúc này
Theo đồ thị
Chứng tỏ trong dung dịch X có axit:
Vậy trong X chứa: gam.
Câu 36:
Tiến hành thí nghiệm điều chế xà phòng theo các bước dưới đây:
Bước 1: Cho vào bát sứ nhỏ 1 ml dầu ăn và 3 ml dung dịch NaOH 40%.
Bước 2: Đun hỗn hợp sôi nhẹ và liên tục khuấy đều bằng đũa thủy tinh khoảng 8-10 phút. Thỉnh thoảng thêm vài giọt nước cất để giữ cho thể tích hỗn hợp không đổi.
Bước 3: Rót thêm vào hỗn hợp 4 - 5 ml dung dịch NaCl bão hòa nóng, khay nhẹ. Sau đó để nguội.
Phát biểu nào sau đây không đúng?
Đáp án D
D sai vì sau bước 3 thu được xà phòng là lớp chất rắn màu trắng đục.
Câu 37:
Cho 56,36 gam hỗn hợp X gồm Mg, Fe(NO3)3, FeCl2 và Fe3O4 vào dung dịch chứa 1,82 mol HCl được dung dịch Y và hỗn hợp khí Z gồm 0,08 mol NO và 0,06 mol N2O. Cho dung dịch AgNO3 dư vào Y, kết thúc phản ứng thấy thoát ra 0,045 mol NO (sản phẩm khử duy nhất) đồng thời thu đuợc 298,31 gam kết tủa. Nấu cô cạn dung dịch Y thì thu đuợc 97,86 gam muối. Phần trăm khối luợng FeCl2 trong X là
Đáp án B
BTKL:
BT H:
BT N:
BT O:
Gọi
BT Cl:
Bảo toàn e cho cả quá trình: (1)
(2)
(3)
.
|
Đối với bài toán có kim loại tác dụng với dung dịch chứa và , lưu ý chất khử có Mg, Al, Zn và đề bài không đề cập đến sản phẩm khử duy nhất thì khả năng cao sẽ tạo muối của . Ở bài trên, đề bài chỉ nói tạo sản phẩm khử duy nhất ở giai đoạn sau nên lưu ý tránh nhầm lẫn. |
Câu 38:
Đun nóng hợp chất hữu cơ X mạch hở với dung dịch NaOH vừa đủ, chưng cất dung dịch sau phản ứng thu được duy nhất một muối natri của axit cacboxylic (có mạch không phân nhánh và không chứa nhóm chức khác) và 9,3 gam ancol Y. Dẫn toàn bộ 9,3 gam Y qua bình đựng Na dư, thấy khối lượng bình tăng 9,0 gam. Đốt cháy toàn bộ muối cần dùng 0,6 mol O2 ; thu được CO2, 2,7 gam H2O và 15,9 gam Na2CO3. Nhận định nào sau đây là sai?
Đáp án D
BT O:
BT C:
Vậy công thức của muối là
Vậy công thức của X là:
Hoặc .
|
Định luật bảo toàn nguyên tố cũng được dùng khá phổ biến trong bài toán tìm công thức hợp chất hữu cơ. Ngoài ra, cần áp dụng triệt để cách tính nhanh số nguyên tử cacbon, hiđrô của hợp chất. - Số cacbon - Số hiđrô |
Câu 39:
Cho hình vẽ mô tả thí nghiệm điều chế khí Z từ dung dịch X và chất rắn Y:
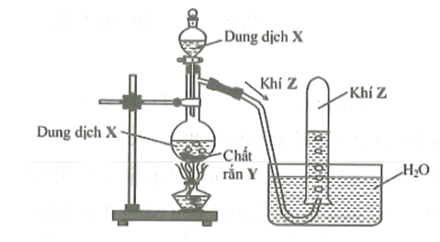
Khí Z được tạo ra từ phản ứng hóa học nào dưới đây?
Đáp án A
Z đuợc thu bằng phương pháp đẩy nước nên Z không tan trong nước, không tác dụng với nước.
Vậy loại B và C.
Z được điều chế từ một chất rắn và một dung dịch nên loại D vì cả CH3COONa và NaOH đều phải ở trạng thái rắn.
|
Nguyên tắc thu khí: - Thu bằng phương pháp đấy nước thì khí thu phải không tan trong nước. - Thu khí bằng phương pháp đẩy không khí thì khí thu phải nặng hơn không khí (đặt ngửa bình), khí thu nhẹ hơn không khí (đặt úp bình). |
Câu 40:
X, Y là 2 peptit được tạo từ các α-amino axit no, mạch hở chứa 1 nhóm -NH2 và 1 nhóm –COOH. Đun nóng 0,1 mol hỗn hợp E chứa X, Y bằng dung dịch NaOH vừa đủ. Cô cạn dung dịch sau phản ứng thu được m gam muối khan. Đốt cháy toàn bộ lượng muối này thu được 0,2 mol Na2CO3 và hỗn hợp gồm CO2, H2O, N2 trong đó tổng khối lượng của CO2 và H2O là 65,6 gam. Mặt khác, đốt cháy 1,51m gam hỗn hợp E cần dùng a mol O2, thu được CO2, H2O , N2. Giá trị của a gần nhất với
|
Những điểm cần nắm khi làm bài tập này: - Đề sử dụng lượng chất khác nhau cho các phản ứng nên cần quy đổi tỉ lệ. - Sử dụng một số cách tính số gốc amino axit hay số -CH2 để biện luận. tính số gốc amino axit trung bình. Biện luận số -CH2 bằng cách xem hỗn hợp peptit là . |
Đáp án B
C2H4NO2Na → 0,5Na2CO3 + 1,5CO2 + 2H2O
CH2 + 1,5O2 → CO2 + H2O
Vậy khi đốt cháy 67,044 gam E thì cần số mol O2 là: mol.
