25 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án
25 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án (Đề 25)
-
3486 lượt thi
-
40 câu hỏi
-
90 phút
Danh sách câu hỏi
Câu 1:
Tính chất vật lý nào sau đây không phải là tính chất chung của kim loại?
Đáp án D
|
Tính chất chung của kim loại là tính dẻo, tính dẫn điện, tính dẫn nhiệt và có ánh kim do các electron tự do trong mạng tinh thể gây ra. |
Câu 2:
Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường thu được dung dịch có môi trường kiềm là
Đáp án A
Câu 3:
Etanol là chất tác động đến thần kinh trung ương. Khi hàm lượng etanol trong máu tăng thì sẽ có hiện tượng nôn, mất tỉnh táo và có thể tử vong. Tên gọi khác của etanol là
Đáp án B
Etanol còn có tên gọi khác là ancol etylic và có công thức hóa học là C2H5OH.
Câu 6:
Trong môi trường kiềm, lòng trắng trứng (anbumin) tác dụng với Cu(OH)2 cho hợp chất màu
Đáp án B
Protein tham gia phản ứng màu biurê (Cu(OH)2/NaOH) tạo phức màu tím.
Câu 7:
Muối nào sau đây dễ tan trong nước?
Đáp án A
|
Tính tan của muối photphat: - Muối trung hòa và muối axit của Na, K, đều tan trong nước. - Muối đihiđrophotphat đều tan trong nước. - Muối trung hòa và muối axit của các kim loại khác không tan hoặc ít tan trong nước. |
Câu 8:
X là hợp chất màu xanh lam, không tan trong nước nhưng dễ tan trong axit. X là
Câu 9:
Polime X có hệ số trùng hợp là 560 và phân tử khối là 35000. Công thức một mắt xích của X là
Đáp án C
Khối lượng của một mắt xích của X là
Vậy một mắt xích là
|
Lưu ý: Mắt xích là không phải là là đơn vị monome để tổng hợp nên polime. |
Câu 10:
Để loại bỏ kim loại Cu ra khỏi hỗn hợp bột gồm Ag và Cu, người ta ngâm hỗn hợp kim loại trên vào lượng dư dung dịch nào sau đây?
Đáp án A
Cu tác dụng với dung dịch AgNO3 tạo ra kim loại Ag nên loại được Cu ra khỏi hỗn hợp.
PTHH:
Câu 11:
Ứng dụng nào sau đây không phải của glucozơ?
Đáp án B
Công thức của ancol etylic là C2H5OH. Công thức chung là hoặc ROH hoặcCâu 13:
Nhúng một lá Fe vào dung dịch chứa một trong những chất sau: FeCl3, AlCl3, CuSO4, HCl, HNO3 (đặc, nguội, dư), H2SO4 (đặc, nóng, dư), H2SO4 (loãng). Số trường hợp tạo muối sắt (III) là
Đáp án A
Câu 14:
Nhiệt phân hoàn toàn 8,4 gam muối NaHCO3 thu được bao nhiêu gam chất rắn?
Đáp án A
Câu 15:
Cho dãy các chất sau: phenyl fomat, glyxylvalin (Gly-Val), saccarozơ, triolein. Số chất bị thủy phân trong môi trường axit là
Đáp án A
PTHH:
Câu 16:
Xenlulozơ trinitrat được điều chế từ phản ứng giữa axit nitric với xenlulozơ (hiệu suất đạt 60% theo xenlulozơ). Dùng 2 tấn xenlulozơ thì khối lượng xenlulozơ trinitrat điều chế được là
Đáp án A
Câu 17:
Thủy phân 1250 gam protein X thu được 425 gam alanin. Nếu phân tử khối của X là 100000 đvC thì số mắt xích alanin có trong phân tử X là
Đáp án B
Vậy số mắt xích alanin trong X là 382.
Câu 19:
Axit mạnh HNO3 và axit yếu HNO2 có cùng nồng độ 0,1M và ở cùng nhiệt độ. Sự so sánh đúng là
Đáp án C
Vì HNO3 là axit mạnh nên phân li hoàn toàn ra ion
Vì HNO2 là axit yếu nên chỉ phân li 1 phần ra ion
Nên
Câu 20:
Thủy phân saccarozơ, thu được hai monosaccarit X và Y. Chất Y chiếm 40% trong mật ong nên làm mật ong có vị ngọt sắc. Phát biểu nào sau đây đúng?
Đáp án D
Thủy phân saccarozơ thu được glucozơ và fructozơ.
Y chiếm 40% trong mật ong nên làm mật ong có vị ngọt sắc nên Y là fructozơ, X là glucozơ.
A sai vì fructozơ tan tốt trong nước.
B sai vì glucozơ và fructozơ đều phản ứng tráng bạc.
C sai vì fructozơ có phân tử khối là 180.
Câu 21:
Trong các phát biểu sau, phát biểu nào sai?
Đáp án D
|
Không thể dùng khí H2 hoặc CO để khử oxit của kim loại có tính khử mạnh như Mg, Al, Na… |
Câu 22:
Thủy phân este X có công thức phân tử C3H6O2 trong môi trường axit, thu được axit cacboxylic Y và ancol Z. Biết Z có số nguyên tử cacbon gấp đôi Y. Tên gọi của X là
Đáp án A
Câu 23:
Tìm phát biểu sai trong các phát biểu sau:
Đáp án B
Có thể phân biệt PVC và PE bằng phương pháp hóa học: đốt 2 loại polime trong phễu chứa sẵn AgNO3 thì mẫu PVC cháy và có kết tủa trắng xuất hiện (AgCl).
Câu 25:
Hòa tan m gam hỗn hợp X gồm Al và Na có tỉ lệ mol 1:2 vào nước dư, thu được 4,48 lít khí (đktc). Giá trị của m là
Đáp án B
HH
Sau phản ứng, dung dịch chứa NaOH và NaAlO2.
Câu 26:
Đun nóng 0,2 mol hỗn hợp X chứa hai este mạch hở gồm este Y (C4H6O2) và este Z (C3H6O2) với dung dịch KOH vừa đủ, chưng cất dung dịch sau phản ứng thu được hỗn hợp gồm hai ancol có khối lượng 9,65 gam và hỗn hợp T chứa hai muối. Khối lượng của muối có khối lượng phân tử nhỏ trong hỗn hợp T là
Đáp án B
Ancol tạo ra từ este Y là Y là
Hỗn hợp T chứa 2 muối nên X phải là CH3COOCH3 : y.
Câu 27:
Cho vào ống nghiệm 2 ml etyl axetat, sau đó thêm tiếp 1 ml dd H2SO4 20% quan sát hiện tượng (1), đun sôi 5 phút, quan sát hiện tượng (2). Kết quả hai lần quan sát (1) và (2) lần lượt là
Đáp án D
Phản ứng este thủy phân trong môi trường axit là phản ứng thuận nghịch nên cho dù chưa xảy ra phản ứng hay phản ứng đã xảy ra thì chất lỏng vẫn phân thành 2 lớp do este ít tan trong nước.
C sai vì phản ứng giữa axit và rượu khi có H2SO4 đặc là phản ứng thuận nghịch.
Câu 28:
Cho dung dịch Ba(OH)2 đến dư vào dung dịch muối X, thu được kết tủa Y. Y tan trong dung dịch HNO3 loãng, thấy thoát ra khí không màu hóa nâu trong không khí. Muối X là
Đáp án C
(khí màu nâu)
Câu 29:
Dẫn a mol hỗn hợp X (gồm hơi nước và khí CO2) qua cacbon nung đỏ, thu được 1,8a mol hỗn hợp khí Y gồm H2, CO, CO2. Cho Y đi qua ống đựng hỗn hợp gồm CuO và Fe2O3 dư đun nóng. Biết các phản ứng xảy ra hoàn toàn. Sau phản ứng khối lượng chất rắn giảm 1,28 gam. Nếu cho Y đi qua dung dịch Ba(OH)2 dư thì thu được m gam kết tủa. Giá trị của m là
Đáp án D
BTNT H&C:
Xem phản ứng giữa Y và oxit là
Khối lượng oxit giảm chính là khối lượng oxi đã mất
BT e:
Câu 30:
Hỗn hợp khí X gồm một ankan và một anken. Tỉ khối của X so với H2 bằng 11,25. Đốt cháy hoàn toàn 4,48 lít khí X, thu được 6,72 lít CO2 (đktc). Công thức của ankan và anken là
Đáp án B
Ankan:
Câu 31:
Hòa tan hết 26,43 gam hỗn hợp bột X gồm Mg, Al, Al2O3 và MgO bằng 795 ml dung dịch hỗn hợp gồm HCl 0,5M và H2SO4 0,75M (vừa đủ). Sau phản ứng thu được dung dịch Y và 4,368 lít khí H2 (ở đktc). Cô cạn dung dịch Y thu được khối lượng muối khan là
Đáp án D
BTKL:
|
Dạng này không viết phương trình hóa học, áp dụng định luật bảo toàn nguyên tố và bảo toàn khối lượng để giải. Chú ý bảo toàn H: H+ trong axit sau phản ứng về H trong H2 và H2O. |
Câu 32:
Cho các nhận định sau:
(a) Triolein là hợp chất hữu cơ đa chức.
(b) Glucozơ cho được phản ứng tráng gương.
(c) Dung dịch metylamin không làm hồng dung dịch phenolphtalein.
(d) Poliacrilonitrin thuộc tơ tổng hợp.
(e) Sau khi mổ cá, có thể dùng giấm ăn để giảm mùi tanh.
(g) Thành phần chính của bông nõn là xenlulozơ.
Các nhận định đúng là
Đáp án A
Những phát biểu đúng: (a), (b), (d), (e), (g).
(c) sai vì dung dịch metylamin có tính bazơ nên làm hồng dung dịch phenolphtalein.
(e) đúng vì mùi tanh của cá do các amin gây nên, vì vậy dùng giấm ăn (CH3COOH) có tính axit để giảm mùi tanh.
Câu 33:
Tiến hành điện phân dung dịch chứa Cu(NO3)2 1,2M và NaCl 0,8M bằng điện cực trơ, sau một thời gian thấy khối lượng dung dịch giảm 17,7 gam. Cho 0,18 mol bột Fe vào dung dịch sau điện phân, kết thúc phản ứng, thấy thoát ra 0,06 mol khí NO (sản phẩm khử duy nhất); đồng thời còn lại x gam rắn không tan. Giá trị x là
Đáp án C
Dung dịch ban đầu:
Sau phản ứng thấy thoát khí NO, chứng tỏ: dung dịch sau điện phân chứa ion nên ở anot đã điện phân hết, nước đã điện phân.
Thứ tự điện phân:
Sau phản ứng còn lại chất rắn không tan là Cu, nên Fe bị oxi hóa thành
BT e:
Khối lượng dung dịch giảm là khối lượng của Cu tạo thành và khối lượng khí Cl2, O2
Từ (1) và (2)
Vậy điện phân hết.
BT e:
|
Trong điện phân: Khối lượng dung dịch giảm chính là khối lượng kim loại tạo thành ở catot và khối lượng khí thoát ra ở catot và anot. |
Câu 34:
Hỗn hợp E gồm etyl axetat, metyl fomat, phenyl fomat và một số trieste của glyxerol với các axit no, hở, đơn chức (biết số mol phenyl fomat = số mol etyl axetat + số mol metyl fomat). Lấy 0,09 mol E đem đốt cháy hoàn toàn cần dùng 0,675 mol O2 thu được 0,43 mol H2O. Nếu lấy 51,92 gam E thì tác dụng hết với dung dịch chứa 0,8 mol KOH. Làm bay hơi dung dịch sau phản ứng thu được m gam chất rắn X và phần hơi chứa 16 gam các chất hữu cơ. Thành phần % khối lượng của kaliphenolat trong X là
Đáp án D
Vậy với 51,92 gam E thì số mol mỗi chất là
BTKL:
|
Bài tập này phải thực hiện quy đổi hỗn hợp về hỗn hợp đơn giản hơn và vì số mol phenyl fomat = số mol etyl axetat + số mol metyl fomat nên |
Câu 35:
Cho m gam hỗn hợp X gồm K2O, Ba vào dung dịch chứa 0,06 mol HCl và 0,08 mol BaCl2 thu được x mol khí và dung dịch Y. Hấp thụ từ từ CO2 vào dung dịch Y ta có đồ thị sau:
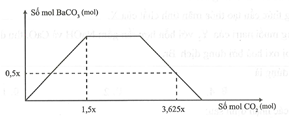
Giá trị của m là
Đáp án A
Dựa vào đồ thị, nhận thấy:
- Đoạn 1: tạo kết tủa BaCO3 max.
- Đoạn 2: nằm ngang, tạo muối K2CO3 và muối tác dụng với CO2 tạo muối KHCO3.
- Đoạn 3: kết tủa BaCO3 tan.
Sau phản ứng tạo khí H2:
Khi kết tủa BaCO3 max thì
Lúc thì
BT K:
Câu 36:
Tiến hành thí nghiệm theo các bước sau đây:
Bước 1: Dùng 4 kẹp sắt kẹp 4 vật liệu riêng lẻ: mẫu màng mỏng PE, mẫu ống nhựa dẫn nước làm bằng PVC, sợi len (làm từ lông cừu) và vải sợi xenlulozơ (hoặc bông).
Bước 2: Hơ các vật liệu này (từng thứ một) ở gần ngọn lửa vài phút.
Bước 3: Đốt các vật liệu trên.
Cho các nhận định sau:
(a) PVC bị chảy ra trước khi cháy, cho nhiều khói đen, khí thoát ra có mùi xốc khó chịu.
(b) Sợi len cháy mạnh, khí thoát ra không có mùi khét.
(c) PE bị chảy ra thành chất lỏng, sản phẩm cháy tạo hoàn toàn thành khí, không có chất lỏng hay rắn.
(d) Sợi vải cháy mạnh, khí thoát ra không có mùi.
(e) Khi hơ nóng 4 vật liệu: PVC bị chảy ra, PE bị chảy thành chất lỏng.
Số nhận định không đúng là
Đáp án C
(a) đúng. PVC là chất dẻo, sẽ chảy ra trước khi cháy, khi cháy sinh ra muội than (cacbon), khí Cl2 có mùi xốc.
(b) sai. Sợi len khi cháy có tạo mùi khét.
(c) đúng.
(d) đúng. Sợi vải cháy sinh ra CO2 và H2O.
(e) đúng.
Câu 37:
Hòa tan hết 27,2 gam hỗn hợp rắn X gồm Fe3O4, Fe2O3 và Cu trong dung dịch chứa 0,9 mol HCl (dùng dư), thu được dung dịch Y có chứa 13,0 gam FeCl3. Tiến hành điện phân dung dịch Y bằng điện cực trơ đến khi catot bắt đầu có khí thoát ra thì dừng điện phân, thấy khối lượng dung dịch giảm 13,64 gam. Cho dung dịch AgNO3 dư vào dung dịch sau điện phân, kết thúc phản ứng thấy khí NO thoát ra (sản phẩm khử duy nhất), đồng thời thu được m gam kết tủa. Giá trị của m là
Đáp án A
Thứ tự điện phân:
Vì khi catot bắt đầu điện phân thì (1) chưa xảy ra, tức là chưa điện phân.
BT e:
Sau điện phân dung dịch chứa:
BT e:
|
- Chú ý thứ tự điện phân: + Khí ở catot bắt đầu xuất hiện, lúc này chưa điện phân. + chỉ điện phân tạo |
Câu 38:
Thủy phân hoàn toàn chất hữu cơ X (C8H12O4, chứa 2 chức este) bằng dung dịch NaOH, thu được sản phẩm gồm ancol Z và hỗn hợp Y gồm hai muối. Axit hóa Y thu được hai axit cacboxylic Y1 và Y2 có cùng số nguyên tử hiđro Cho các phát biểu sau:
(a) Phân tử khối của Z là 62 g/mol.
(b) Có 3 công thức cấu tạo thỏa mãn tính chất của X.
(c) Nung nóng muối natri của Y2 với hỗn hợp rắn gồm NaOH và CaO, thu được CH4.
(d) Chất Y1 bị oxi hóa bởi dung dịch Br2.
Số phát biểu đúng là
Đáp án A
, X chứa 2 chức este nên còn 1 liên kết
Y1 và Y2 là 2 muối cùng H, nên 2 muối này là: và
X là:
Hoặc
Hoặc
(a) sai. (b) đúng. (c) đúng. (d) đúng.
Câu 39:
Cho các nhận định sau:
(a) Muối natri cacbonat là nguyên liệu trong công nghiệp sản xuất thủy tinh, xà phòng.
(b) Thạch cao nung (CaSO4.H2O) được dùng làm phấn viết bảng, bó bột khi gãy xương.
(c) Nhôm và hợp kim của nhôm được dùng làm khung cửa và trang trí nội thất.
(d) Oxit sắt (III) được dùng để pha sơn chống gỉ.
(e) KCr(SO4)2.14H2O được dùng làm chất cầm màu trong ngành nhuộm vải.
Số nhận định đúng là
Đáp án C
Những phát biểu đúng: (a), (b), (c), (d).
(e) sai. được dùng làm chất cầm màu trong ngành nhuộm vải.
Câu 40:
Hỗn hợp E gồm hai chất: X là muối amoni của axit cacboxylic hai chức, chất Y là muối amoni của một amoni axit với amin, n > m. Cho 0,1 mol hỗn hợp E tác dụng với lượng dư dung dịch KOH, đun nóng, thu được 17,56 gam hỗn hợp hai muối và 3,584 lít hỗn hợp khí Z (đktc) gồm hai amin kế tiếp nhau, tỉ khối với H2 là 18,125. Phần trăm khối lượng của X trong E là
Đáp án D
Vậy X là: CH3NH3OOCRCOONH3C2H5
Y là:
