25 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án
25 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án (Đề 13)
-
3505 lượt thi
-
40 câu hỏi
-
90 phút
Danh sách câu hỏi
Câu 1:
Đáp án D
- Khối lượng riêng nhỏ nhất: Li, khối lượng riêng lớn nhất Os.
- Kim loại có khối lượng riêng nhỏ là kim loại nhẹ như: Na, K, Mg, Al...
- Kim loại có khối lượng riêng lớn là kim loại nặng như: Fe, Zn, Pb, Cu, Ag, Hg...
Câu 2:
Trong công nghiệp, nhôm được sản xuất bằng cách điện phân nóng chảy chất nào sau đây?
Đáp án B
PTHH: 2Al2O3 4Al + 3O2.
Câu 3:
Đáp án B
Câu 4:
Baking soda (thuốc muối, bột nở) là tên gọi thường dùng trong thực phẩm của hợp chất sodium bicarbonate (natri hiđrocacbonat hay natri bicacbonat). Công thức hóa học của baking soda là
Đáp án C
Câu 6:
Chất nào sau đây phản ứng với dung dịch FeCl3 tạo kết tủa?
Đáp án C
Dung dịch metylamin có tính bazơ, phản ứng được với dung dịch muối FeCl3 tạo kết tủa nâu đỏ.
PTHH: 3CH3NH2 + FeCl3 + 3H2O → Fe(OH)3 + 3CH3NH3Cl.
Câu 8:
Thép là hợp kim của sắt với cacbon và một số nguyên tố khác trong đó hàm lượng cacbon chiếm
Đáp án B
|
Thép là hợp kim của sắt chứa từ 0.01 - 2% khối lượng cacbon cùng với một số nguyên tố khác (Si, Mn, Cr, Ni,...). Gang là hợp kim của sắt với cacbon, trong đó hàm lượng cacbon chiếm từ 2-5%, ngoài ra còn có một lượng nhỏ các nguyên tố khác như Si, Mn, s,... Gang cứng và giòn hơn sắt. |
Câu 9:
Công thức nào tương ứng với tên gọi nào sau đây là không đúng?
Đáp án C
Công thức hóa học của plexiglas
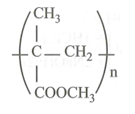
Câu 10:
Đáp án D
Phương pháp thủy luyện thường dùng để điều chế kim loại có tính khử yếu như Cu, Ag,...
Ví dụ: Điều chế Cu từ muối CuSO4 và kim loại Fe.
PTHH: CuSO4 + Fe → Cu + FeSO4Câu 11:
Phát biểu nào sau đây là đúng?
Đáp án C
A sai vì saccarozo không tham gia phản ứng tráng gương.
B sai vì glucozo bị oxi hóa bởi dung dịch AgNO3 trong NH3.
D sai vì xenlulozo có cấu trúc mạch không phân nhánh.Câu 12:
Hiện tượng khi cho phenol tác dụng với dung dịch Br2
Đáp án D
PTHH: C6H5OH + 3Br2 → C6H2Br3OH ↓ +3HBr.
Câu 13:
Khử hoàn toàn 16 gam Fe2O3 bằng khí co ở nhiệt độ cao. Khí đi ra sau phản ứng được dẫn vào dung dịch Ca(OH)2 dư. Khối lượng kết tủa thu được là
Đáp án D
mol
mol
Xem phản ứng khử oxit kim loại là quá trình chất khử lấy O trong oxit.
mol
Dẫn CO2 vào dung dịch Ca(OH)2 dư chỉ thu được kết tủa CaCO3
mol
Vậy (g).
Câu 14:
Để hòa tan hết 0,15 mol A12O3 và 0,2 mol AI thì cần dùng vừa đủ số mol NaOH là
Đáp án D
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
Al2O3 + 2NaOH → 2NaAlO2 + H2O
Câu 15:
Các chất trong dãy nào sau đây đều tạo kết tủa khi cho tác dụng với dung dịch AgNO3 /NH3, đun nóng?
Đáp án C
- Glucozơ, anđehit axetic: có nhóm chức -CHO.
- Vinylaxetilen: có nối 3 đầu mạch.
Câu 16:
Thuỷ phân saccarozơ, thu được 180 gam hỗn hợp glucozơ và fructozơ. Khối lượng saccarozơ đã thuỷ phân là
Đáp án A
Saccarozơ Glucozơ + Fructozơ
C12H22O11 2C6H12O6
mol
gam
Câu 17:
Hỗn hợp X gồm alanin và axit glutamic. Cho m gam X phản ứng hoàn toàn với dung dịch NaOH (dư), thu được dung dịch Y chứa gam muối. Mặt khác, m gam X phản ứng hoàn toàn với dung dịch HCl, thu được dung dịch Z chứa gam muối. Giá trị của m là
Đáp án D
Tóm tắt phản ứng xảy ra:
NH2CH(CH3)COOH:
HOOC(CH2)2CH(NH2)COOH:
Ta có:
gam
|
Công thức tính nhanh:
|
Câu 18:
Khi phân tích định tính nguyên tố hiđro trong hợp chất hữu cơ người ta thường đốt cháy chất hữu cơ đó rồi cho sản phẩm đi qua
Đáp án B
CuSO4 khan ngậm nước sẽ chuyển thành màu xanh nên nhận biết được trong họp chất hữu cơ có nguyên tử hiđro hay không.
Câu 19:
Dung dịch X chứa: a mol , b mol , c mol Cl- và d mol . Biểu thức nào sau đây biểu diễn mối quan hệ giữa a, b, c, d?
Đáp án A
Bảo toàn điện tích:
Câu 20:
Phương trình: 6nCO2 + 5nH2O → + 6nO2 là phản ứng hóa học chính của quá trình nào sau đây?
Câu 22:
Hợp chất X có công thức đơn giản nhất là CH2O . X tác dụng được với dung dịch NaOH nhung không tác dụng được với natri. Công thức cấu tạo của X là
Đáp án C
X tác dụng được với dung dịch NaOH nhưng không tác dụng được với natri nên X là este: HCOOCH3 với .
Câu 23:
Phát biểu đúng là
Đáp án C
A sai vì phenol có vòng benzen làm tăng tính linh động của H trong OH nên nó có tính axit mạnh hơn ancol.
B sai vì axit axetic có tính axit yếu hơn tính axit của axit fomic.
D sai vì tính bazơ sắp xếp như sau: CH3NH2 > NH3 > C6H5NH2.
|
Sắp xếp tính bazơ của amin như sau: C2H5NH2 > CH3NH2 > NH3 > C6H5NH2 > (C6H5)2NH |
Câu 24:
Đáp án A
B sai vì Cr tạo được oxit bazơ, oxit axit và oxit lưỡng tính.
C sai vì Cr không có tính lưỡng tính.
D sai vì Cr có độ cứng cao nhất trong các kim loại.
Câu 25:
Cho 200 ml dung dịch AlCl3 1,5M tác dụng với V lít dung dịch NaOH 0,5M, lượng kết tủa thu được là 15,6 gam. Giá trị lớn nhất của V là
Đáp án D
Để giá trị V lớn nhất thì kết tủa Al(OH)3 sau khi tạo thành tiếp tục tan 1 phần trong NaOH.
(1)
(2)
mol
mol
mol
(l)
Câu 26:
Đốt cháy hoàn toàn m gam một triglixerit A cần vừa đủ 1,51 mol O2, sau phản ứng thu được 1,06 mol CO2 và 1,02 mol H2O . Mặt khác, thủy phân 41,7 gam A bằng dung dịch NaOH dư thu được X gam muối. Giá trị của X gần nhất với
Đáp án B
BTKL: gam
BTNT O: mol
(RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
BTKL:
gam
16,68 gam A → 17,24 gam muối
41,7 gam A → x ?
gam
Câu 27:
Phát biểu nào dưới đây đúng?
Đáp án D
A sai vì có những phản ứng tạo anđehit, xeton, nước.
B sai vì thủy phân chất béo luôn thu được glixerol.
Câu 28:
Cho dung dịch Ba(HCO3)2 lần lượt vào các dung dịch: CaCl2, Ca(NO3)2, NaOH, Na2CO3, KHSO4, Na2SO4, Ca(OH)2, H2SO4, HCl. số trường hợp có tạo ra kết tủa là
Đáp án A
Trường hợp có tạo ra kết tủa là NaOH, Na2CO3, KHSO4, Na2SO4, Ca(OH)2, H2SO4.
Câu 29:
Dung dịch X gồm 0,01 mol Cu(NO3)2 và 0,1 mol NaHSO4. Khối lượng Fe tối đa phản ứng được với dung dịch X là (biết NO là sản phẩm khử duy nhất của NO3)
Đáp án D
Sau phản ứng: H+ dư.
Fe phản ứng tối đa với dung dịch X nên Fe bị oxi hóa thành Fe2+.
BT e: mol
gam.
Câu 30:
Hỗn hợp X gồm C2H2 và H2 có cùng số mol. Lấy một lượng hỗn hợp X cho đi qua chất xúc tác thích hợp, đun nóng được hỗn hợp Y gồm 4 chất. Dẫn Y qua bình đựng nước brom thấy khối lượng bình tăng 10,8 gam và thoát ra 4,48 lít khí Z (đktc) có tỉ khối so với H2 là 8. Thể tích O2 (đktc) cần để đốt cháy hoàn toàn hỗn hợp Y là
Đáp án A
Khối lượng bình brom tăng chính là khối lượng hiđrocacbon không no: C2H2, C2H4
gam
mol
Đốt cháy hỗn hợp Y cũng như đốt cháy hỗn hợp X.
C2H2 + 2,5O2 2CO2 + H2O
2H2 + O2 2H2O
mol
(l)
|
Những điểm lưu ý của bài này: - có thể hiểu khối lượng bình brom tăng chính là khối lượng hiđrocacbon không no đã tác dụng với brom. - Cần linh hoạt trong việc sử dụng yêu cầu đề bài: đốt hỗn hợp X cũng như đốt hỗn hợp Y vì thành phần khối lượng các nguyên tố vẫn không thay đổi. |
Câu 31:
Chia m gam Al thành hai phần bằng nhau:
- Phần một tác dụng với lượng dư dung dịch NaOH, sinh ra X mol khí H2.
- Phần hai tác dụng với lượng dư dung dịch HNO3 loãng, sinh ra Y mol khí N2O (sản phẩm khử duy nhất).
Quan hệ giữa X và Y là
Đáp án B
Phần 1:
2x x
Phần 2:
BT e: 8y y
Câu 32:
Este X mạch hở, không tồn tại đồng phân hình học và có công thức phân tử C6H8O4. Đun nóng 1 mol X với dung dịch NaOH dư, thu được muối Y và 2 mol ancol Z. Biết Z không tác dụng với Cu(OH)2 ở điều kiện thường, khi đun Z với H2SO4 đặc ở không tạo ra anken. Nhận định nào sau đây là đúng?
Đáp án C
X là este 2 chức thủy phân tạo 2 mol ancol Z. Z không tạo anken nên Z: CH3OH.
X có 1 liên kết π C–C nhưng không có đồng phân hình học.
Vậy X có công thức: CH3OOC-C(=CH2)-COOCH3
A sai vì X có mạch cacbon phân nhánh.
B sai vì Y có công thức phân tử: C4H2O4Na2.
C đúng.
D sai vì X phản ứng với H2 (xúc tác Ni, to) theo tỉ lệ mol 1:1.
|
Nếu tách nước một ancol no đơn chức không thu được anken thì ancol đó chỉ có V) thể là CH3OH |
Câu 33:
Điện phân dung dịch X chứa CuSO4, KCl và HCl với điện cực tro, màng ngăn xốp. Cường độ dòng điện không đổi. Tổng số mol khí thoát ra ở cả hai điện cực phụ thuộc vào thời gian điện phân theo đồ thị sau:
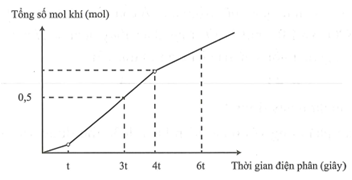
Biết hiệu suất phản ứng điện phân là 100%, các khí sinh ra không tan trong nước và không bay hơi trong quá trình điện phân. Phần trăm thể tích khí H2 ở thời điểm 6t là
Đáp án B
Giai đoạn 1: khí Cl2 thoát ra.
Giai đoạn 2: khí Cl2 và H2 thoát ra.
Giai đoạn 3: H2 và O2.
Lúc t giây:
Lúc 3t giây:
0,5x → x 1,5x → 3x
Lúc 4t giây:
0,1 → 0,2 0,4 → 0,8
0,6
Lúc này H+ điện phân hết:
Lúc 6t giây:
.
Câu 34:
Hỗn hợp X gồm hai este đơn chức và một este hai chức (trong đó có hai este của phenol). Đốt cháy hoàn toàn 22,96 gam X cần dùng 1,23 mol O2, thu được CO2 và 12,6 gam H2O . Nếu đun nóng 22,96 gam X cần dùng tối đa 13,6 gam NaOH trong dung dịch, thu được hỗn hợp Y gồm hai ancol kế tiếp thuộc cùng dãy đồng đẳng và hỗn hợp X gồm ba muối. Dần toàn bộ Y qua bình đựng Na dư, thấy khối lượng bình tăng 5,94 gam. Tổng khối lượng muối của axit cacboxylic có trong Z là
Đáp án A
(vì COOPhe tác dụng với NaOH với tỉ lệ 1:2)
Thủy phân thu được 2 ancol đồng đẳng liên tiếp, nên đó là 2 este đơn chức.
2 ancol khác nhau nên nó không thể cùng thuộc este 2 chức. Vậy trong 2 este của phenol, có 1 este phenol đơn chức và 1 este của phenol trong este 2 chức.
Vì thu được 3 muối nên công thức của các este là:
|
Một số công thức tính nhanh:
|
Câu 35:
Tiến hành phản ứng nhiệt nhôm 28,08 gam hỗn hợp X gồm Al và FeO sau một thời gian thu được hỗn hợp rắn Y. Cho Y vào dung dịch KOH dư, sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp rắn Z và thoát ra 4,032 lít khí H2 (đktc). Hoà tan hoàn toàn Z trong dung dịch HNO3 dư thu được 0,22 mol NO (sản phẩm khử duy nhất của N). Hiệu suất phản ứng nhiệt nhôm là
Đáp án B
BTKL: (1)
BT e: (2)
2Al + 3FeO 3Fe + Al2O3
(3)
Từ (1), (2), (3)
BTNT Fe, Al
2Al + 3FeO 3Fe + Al2O3
0,24 0,3
0,12 0,18 0,06
Vậy hiệu suất phản ứng tính theo FeO
Câu 36:
Tiến hành thí nghiệm điều chế etyl butirat theo các bước sau đây:
- Bước 1: Cho 1 ml C2H5OH, 1 ml axit butiric C2H5CH2COOH và vài giọt dung dịch H2SO4 đặc vào ống nghiệm.
- Bước 2: Lắc đều ống nghiệm, đun cách thủy (trong nồi nước nóng) khoảng 7-8 phút ở .
- Bước 3: Làm lạnh, sau đó rót 2 ml dưng dịch NaCl bão hòa vào ống nghiệm.
Cho các phát biểu sau:
(a) H2SO4 đặc có vai trò vừa làm chất xúc tác vừa làm tăng hiệu suất tạo sản phẩm.
(b) Ở bước 2 có thể tiến hành đun sôi trực tiếp hỗn hợp.
(c) Sau bước 2, trong ống nghiệm vẫn còn C2H5OH và C2H5CH2COOH.
(d) Hỗn hợp thu được sau bước 3 có mùi thơm của hoa nhài.
(e) Sau bước 3, chất lỏng trong ống nghiệm tách thành hai lớp.
(f) Dùng HCl đặc thay cho H2SO4 đặc thì hiệu suất phản ứng cũng như nhau.
Số phát biểu đúng là
Đáp án A
Những phát biểu đúng: (a), (c), (e).
(b) sai. Đun nóng quá sẽ làm các chất bay hơi.
(c) đúng. Phản ứng este hóa là phản ứng thuận nghịch.
(d) sai. Este etyl butirat có mùi dứa.
(e) đúng. Este không tan nên tách lớp.
(f) sai. Vì HCl dễ bay hơi, còn H2SO4 đặc không bay hơi.
Câu 37:
Hòa tan hết hỗn hợp gồm Mg, Fe3O4 và Fe(NO3)2 trong dung dịch chứa 1,44 mol HCl, kết thúc phản ứng, thu được dung dịch X chỉ chứa các muối clorua có tổng khối lượng 75,28 gam và 3,584 lít (đktc) hỗn hợp khí Y gồm NO và H2 có tỉ khối so với H2 bằng 11,5. Cho dung dịch NaOH dư vào X (không có mặt oxi), thu được 47,24 gam kết tủa. Nếu cho dung dịch AgNO3 dư vào X, thu được X gam kết tủa. Giá trị gần nhất của X là
Đáp án A
(1)
BTĐT: (2)
BT N:
BT Fe:
gam
Câu 38:
Hỗn hợp X gồm HO-CH2-CHO, CH2=CHCOOH , CH2 (COOCH3)2, C6H12O6 (glucozơ). Đốt cháy hoàn toàn m gam X cần dùng 0,33 mol O2, sản phẩm cháy gồm CO2 và H2O cho vào dung dịch Ca(OH)2, sau khi kết thúc phản ứng, lọc bỏ kết tủa thu được dung dịch Y có khối lượng tăng 10,56 gam so với dung dịch ban đầu. Cho từ từ dung dịch NaOH 1M vào Y, đến khi thu được kết tủa lớn nhất thì đã dùng 120 ml. Giá trị của m là
Đáp án A
Quy đổi hỗn hợp X thành C và H2O:
Ca(HCO3)2 + NaOH → CaCO3 + NaHCO3 + H2O
BT C:
BTKL: gam
|
Giải thích sự quy đổi: Hỗn hợp X gồm: HO-CH2-CHO: C2(H2O)2 CH2=CHCOOH: C3(H2O)2 CH2(COOCH3)2: C5(H2O)4 C6H12O6: C6(H6O)2 Vậy quy đổi hỗn hợp X thành C và H2O |
Câu 39:
Cho các phản ứng:
(1) O3 + dung dịch KI → (2) F2 + H2O →
(3) MnO2 + HCl → (4) Cl2 + dung dịch H2S →
Các phản ứng tạo ra đơn chất là
Đáp án A
(1) O3 + 2KI + H2O → O2 + 2KOH + I2
(2) 2F2 + 2H2O → O2 + 4HF
(3) MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
(4) 4Cl2 + H2S + 4H2O → H2SO4 + 8HCl
Câu 40:
Hỗn hợp E gồm X (C7H16O6N2) và Y (C5H14O4N2), là muối của axit cacboxylic hai chức tác dụng hoàn toàn với dung dịch KOH, thu được ancol etylic; 0,2 mol hỗn hợp hai amin no, đơn chức, kế tiếp nhau trong dãy đồng đẳng, có tỉ khối so với H2 bằng 16,9 và dung dịch Z. Cô cạn dung dịch Z thu được hỗn hợp T gồm hai muối khan có cùng số nguyên tử cacbon trong phân tử, trong đó có một muối của axit cacboxylic và một muối của α-amino axit. Phần trăm khối lượng của muối có phân tử khối lớn hơn trong T là
Đáp án A
.
|
Đối với dạng bài toán này, việc tính toán không hề khó, chủ yếu là tìm được công thức chính xác của chất hữu cơ. |
