25 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án
25 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án (Đề 20)
-
3490 lượt thi
-
40 câu hỏi
-
90 phút
Danh sách câu hỏi
Câu 1:
Ion nào sau đây có tính oxi hóa mạnh nhất?
Đáp án B.
Thứ tự tính oxi hóa tăng dần của các ion kim loại:
Câu 2:
Đáp án B.
- Tất cả kim loại kiềm phản ứng với nước ở điều kiện thường.
- Các kim loại kiềm thổ phản ứng với nước ở điều kiện thường như Ba, Ca, Sr.
- Mg phản ứng với nước khi đun nóng.
- Be không phản ứng với nước kể cả khi đun nóng.
Câu 3:
Bảo quản thực phầm (thịt, cá,..) bằng cách nào sau đây được xem là an toàn?
Đáp án C.
Câu 5:
Đáp án B.
Thạch cao có thành phần chính là muối canxi sunfat.
Câu 8:
Số oxi hóa cao nhất của crom thể hiện trong hợp chất nào sau đây?
Đáp án B.
Số oxi hóa của crom trong các hợp chất:
Câu 9:
Quá trình kết hợp của nhiều phân tử nhỏ (monome) thành phân tử lớn (polime) được gọi là phản ứng
Đáp án C.
Câu 10:
Kim loại nào sau đây phản ứng với dung dịch
Đáp án B.
- Ag, Hg có tính khử yếu hơn Cu nên 2 kim loại này không phản ứng với dung dịch
- PTHH:
Câu 11:
Đáp án A.
- Glucozơ và fructozơ đều không tham gia phản ứng thủy phân.
- Chỉ có glucozơ có nhóm chức
- Glucozơ và fructozơ đều thuộc monosaccarit.
Câu 12:
Đáp án A.
- Ancol bậc 1 bị oxi hóa bởi CuO thu được anđehit.
- Ancol bậc 2 bị oxi hóa bởi CuO thu được xeton.
- Ancol bậc 3 không bị oxi hóa.Câu 13:
Cho hỗn hợp X gồm và Cu tác dụng với dung dịch HCl (dư) thu được dung dịch Y và phần không tan Z. Cho Y tác dụng với dung dịch NaOH (loãng, dư) thu được kết tủa là
Đáp án D.
- Phần không tan Z là Cu thì trong Y chứa các muối của
- Vì ban đầu tác dụng với HCl tạo muối nhưng vì phần không tan chứa Cu nên tất cả lượng muối đã tác dụng với một phần Cu tạo thành muối của và
- Y tác dụng dung dịch NaOH (loãng, dư) thu được kết tủa là và
- Kết tủa tạo thành đã tan trong dung dịch NaOH dư.
Câu 14:
Hòa tan hoàn toàn 5,1 gam cần vừa đủ V ml dung dịch NaOH 1M. Giá trị của V là
Đáp án B.
Câu 15:
Chất nào sau đây không bị thủy phân trong môi trường bazơ?
Đáp án B.
Các chất bị thủy phân trong môi trường bazơ: Ala-Val, etyl axetat, triolein.
Câu 16:
Để điều chế 26,73 kg xenlulozơ trinitrat (hiệu suất 75%) cần dùng ít nhất V lít axit nitric 94,5% (d = 1,5 g/ml). Giá trị của V là
Đáp án C.
(phản ứng)
(đã dùng)
Câu 17:
Thủy phân 0,4 mol peptit X chỉ thu được 90 gam glyxin. Vậy X thuộc loại
Đáp án B.
X là tripeptit.
Câu 18:
Chất nào sau đây có dồng phân hình học?
Đáp án D.
Điều kiện để có đồng phân hình học
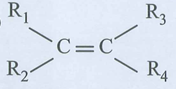
và
Câu 19:
Nếu bỏ qua sự điện li của nước thì dãy gồm đầy đủ các ion trong dung dịch axit photphoric là
Đáp án A.
Quá trình điện li:
Câu 20:
Cho các phát biểu sau:
(a) Glucozơ và fructozơ phản ứng với H2 (đun nóng, Ni) đều cho sản phẩm là sobitol.
(b) Trong môi trường axit, glucozơ và fructozơ có thể chuyển hóa lẫn nhau.
(c) Có thể phân biệt glucozơ và fructozơ bằng phản ứng với dung dịch
(d) Trong dunh dịch, glucozơ và fructozơ đều hòa tan ở nhiệt độ thường cho dung dịch màu xanh lam.
(e) Fructozơ là hợp chất đa chức.
(f) Có thể điều chế ancol etylic từ glucozơ bằng phương pháp sinh hóa.
Số phát biểu đúng là
Đáp án A.
Những phát biểu đúng: (d), (f).
(a) sai vì glucozơ phản ứng với (đun nóng, Ni) cho sản phẩm là sobitol còn fructozơ phản ứng với (đun nóng, Ni) cho sản phẩm là poliancol.
(b) sai vì glucozơ và fructozơ có thể chuyển hóa lẫn nhau trong môi trường bazơ.
(c) sai vì glucozơ và fructozơ đều phản ứng với dung dịch tạo kết tủa bạc nên không thể phân biệt glucozơ và fructozơ bằng phản ứng với dung dịch
(e) sai vì fructozơ là hợp chất tạp chức.
Câu 21:
Cho biết thứ tự từ trái sang phải của các cặp oxi hóa – khử trong dãy điện hóa (dãy thế điện cực chuẩn) như sau: Các kim loại và ion đều phản ứng được với ion Fe2+ trong dung dịch là
Đáp án B.
Thứ tự trong dãy điện hóa:
Zn Fe Cu
Theo quy tắc a: phản ứng được với Zn và
Câu 22:
Thủy phân este trong môi trường axit thì ta thu được một hỗn hợp các chất đều có phản ứng tráng gương. Vậy công thức cấu tạo của este có thể là ở đáp án nào sau đây?
Đáp án C.
Câu 23:
Kết luận nào sau đây không đúng?
Đáp án A.
Tơ visco, tơ xenlulozơ axetat là tơ nhân tạo hay tơ bán tổng hợp, chúng đều được tổng hợp từ xenlulozơ.
Câu 24:
Đáp án D.
Dung dịch có màu vàng, dung dịch có màu da cam.
Câu 25:
Cho m hỗn hợp Na, Ba vào nước thu được dung dịch X và 6,72 lít khí (đktc). Thể tích dung dịch hỗn hợp và HCl 1M để trung hòa vừa đủ dung dịch X là
Đáp án A.
Câu 26:
Xà phòng hóa chất béo X bằng dung dịch NaOH thu được 18,4 gam glixerol và 182,4 gam muối của axit béo. Số nguyên tử cacbon có trong chất béo là
Đáp án D.
® Muối là:
® X là Vậy số nguyên tử cacbon là 57.
Câu 27:
Cho các nhận định sau:
(a) Chất béo thuộc loại hợp chất este.
(b) Triolein tác dụng với thu được tristearin.
(c) Mỡ động vật và mỡ bôi trơn máy có cùng thành phân các nguyên tố hóa học.
(d) Thủy phân chất béo trong dung dịch NaOH, thu được xà phòng.
Các nhận định đúng là
Đáp án D.
(c) sai vì mỡ động vật là chất béo (C, H, O), mỡ bôi trơn là hiđrocacbon (C, H).
Câu 28:
Cho Cu và dung dịch loãng tác dụng với chất X (một loại phân bón hóa học), thoát ra khí không màu hóa nâu trong không khí. Mặt khác, khi X tác dụng với dung dịch NaOH thì có khí mùi khai thoát ra. Chất X là
Đáp án A.
Amoni nitrat:
Câu 29:
Hòa tan hoàn toàn hỗn hợp gồm 1,12 gam Fe và 1,44 gam FeO bằng 300 ml dung dịch HCl 0,4M, thu được dung dịch X. Cho dung dịch dư vào X, thu được khí NO (sản phẩm khử duy nhất của ) và m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
Đáp án C.
nHCl (phản ứng)
0,04 0,04 0,04 0,03
BT e:
Khối lượng kết tủa:
Câu 30:
Cho 11,2 lít (đktc) hỗn hợp X gồm và qua bình đựng Ni (đun nóng), thu được hỗn hợp Y (chỉ chứa ba hiđrocacbon) có tỉ khối so với là 14,5. Biết Y phản ứng tối đa với a mol trong dung dịch. Giá trị của a là
Đáp án D.
Công thức mặc dù không có ý nghĩa về mặt hóa học, nhưng với việc tính toán, dùng công thức này không làm ảnh hưởng đến kết quả của bài, mà còn làm cho việc giải trở nên đơn giản hơn.
Vì vậy, đối với hỗn hợp nhiều chất, nên quy về công thức đơn giản hơn.
Câu 31:
Dung dịch X gồm a mol/l và b mol/l. Cho 400ml dung dịch X tác dụng với 612ml dung dịch NaOH 1M thu được 8,424 gam kết tủa. Mặt khác nếu cho 400ml dung dịch X tác dụng với dung dịch dư thu được 33,552 gam kết tủa. Tỉ số a/b là
Đáp án B.
BT số mol gốc
kết tủa tạo thành đã tan một phần trong NaOH.
x 3x x
y y
Câu 32:
Cho các phản ứng sau:
(1) (4)
(2) (5)
(3) (6)
Số phản ứng oxi hóa – khử xảy ra là.
Đáp án A.
Những phản ứng oxi hóa khử: (1), (3), (5), (6).
(1)
(2)
(3)
(4)
(5)
(6)
Câu 33:
Điện phân dung dịch chứa và NaCl với điện cực trơ, cường độ dòng điện không đổi 2A, hiệu suất 100%. Kết quả thí nghiệm được ghi trong bảng sau:
|
Thời gian điện phân (giây) |
t |
t + 2895 |
2t |
|
Tổng số mol khí ở 2 điện cực |
a |
a + 0,03 |
2,125a |
|
Số mol Cu ở catot |
b |
b + 0,02 |
b + 0,02 |
Giá trị của t là
Đáp án B.
Giai đoạn 2: Trong khoảng thời gian 2895 giờ.
Trong khoảng thời gian từ t giây đến 2t giây, chỉ có ở 2 cực điện phân thêm tạo khí O2 và H2
2z z
t 4t
Trong khoảng thời gian từ t giây đến 2t giây:
Trong thời gian từ 0 đến t giây:
Vì đều điện phân trong 2 khoảng thời gian bằng nhau: từ 0 đến t giây, từ t đến 2t giây nên số mol e nhường nhận ở 2 khoảng thời gian trên là như nhau.
Từ (1) (2)
Lúc t giây:
- Bài toán này khá phức tạp vì có nhiều khoảng thời gian điện phân. Cần xét từng khoảng thời gian đã xảy ra quá trình điện phân nào.
- Trong những khoảng thời gian điện phân giống nhau, thì số mol e nhường nhận là như nhau
Câu 34:
Cho hỗn hợp X gồm hỗn hợp bốn este mạch hở, trong đó có một este đơn chức và ba este hai chức là đồng phân của nhau. Đốt cháy hoàn toàn 11,88 gam X cần 14,784 lít O2 (đktc), thu được 25,08 gam CO2. Đun nóng 11,88 gam X với 300 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thu được chất rắn Y và phần hơi chỉ chứa một ancol đơn chức Z. Lấy toàn bộ Z cho vào bình đựng Na dư, sau khi phản ứng xảy ra hoàn toàn thấy khối lượng chất rắn trong bình đựng Na tăng 5,85 gam. Trộn Y với CaO rồi nung trong điều kiện không có không khí, thu được 2,016 lít (ở đktc) một hiđrocacbon duy nhất. Phần trăm khối lượng của este đơn chức trong X là
Đáp án D.
nNaOH phản ứng
Sau khi thủy phân chỉ thu được một ancol duy nhất nên đó là ancol đơn chức.
Vậy nNaOH phản ứng = 0,13
BTKL: mmuối
nmuối
%meste đơn chức
Câu 35:
Cho 400 ml dung dịch E gồm x mol/lít và y mol/lít tác dụng với 612 ml dung dịch NaOH 1M, sau khi các phản ứng kết thúc thu được 8,424 gam kết tủa. Mặt khác, khi cho 400 ml E tác dụng với dung dịch (dư) thì thu được 33,552 gam kết tủa. Tỉ lệ x : y là
Đáp án D.
0,108 0,324 0,108
0,072
Câu 36:
Este X hai chức mạch hở có công thức phân tử là không có khả năng tham gia phản ứng tráng bạc, được tạo ra từ ancol Y và axit cacboxylic Z. Đun Y với đặc, không tạo ra được anken. Y không phản ứng với ở điều kiện thường. Nhận xét nào sau đây là đúng?
Đáp án A.
X không tráng bạc nên X không có dạng là
Y không phản ứng với ở điều kiện thường nên Y không có từ 2 OH liền kề.
Y không tạo anken.
Vậy công thức của X là:
Z:
Y:
Câu 37:
Hòa tan hết hỗn hợp X gồm Fe, (x mol), (y mol) trong dung dịch chứa 0,06 mol và 0,48 mol kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối và 0,08 ml khí NO (sản phẩm khử duy nhất của ). Cho 600 ml dung dịch NaOH 1M vào Y, lọc bỏ kết tủa, cô cạn phần dung dịch nước lọc, sau đó đem nung đến khối lượng không đổi, thu được 40,9 gam rắn khan. Tỉ lệ x:y là
Đáp án A.
Nước lọc chứa NaOH dư và
Đối với bài này cần lưu ý:
- đóng vai trò: kết hợp tạo nước, kết hợp với đóng vai trò oxi hóa tạo NO nên:
- Sau khi NaOH phản ứng với các chất trong dung dịch Y thì NaOH còn dư.
Câu 38:
X là este no, đơn chức; Y là este đơn chức, không no chứa một liên kết đôi (X, Y đều mạch hở). Đốt cháy hoàn toàn 0,08 mol hỗn hợp E chứa X, Y (số mol X lớn hơn số mol Y) cần dùng 7,28 lít (đktc). Mặt khác đun nóng 0,08 mol E với dung dịch NaOH (lấy dư 20% so với phản ứng), cô cạn dung dịch sau phản ứng thu được m gam rắn khan và hỗn hợp F chứa 2 ancol đồng đẳng kế tiếp. Đun nóng F với CuO thu được hỗn hợp chứa 2 anđehit, lấy toàn bộ hỗn hợp 2 anđehit này tác dụng với thu được 28,08 gam Ag. Giá trị m là
Đáp án B.
Nên 2 anđehit là và
BTKL: mmuối mmuối
Chú ý: Tỉ lệ xác định được số nguyên tử Ag mà mỗi anđehit tạo thành.
Như ví dụ trên, nhận thấy số Ag trung bình là 3,25 nên suy ra được 2 anđehit là HCHO và vì HCHO tạo 4 Ag và tạo 2 Ag.
Câu 39:
Cho các nhận định sau:
(a) Ăn mòn hóa học làm phát sinh dòng điện một chiều.
(b) Cho Mg dư vào dung dịch thu được dung dịch chứa 2 muối.
(c) Các kim loại dẫn điện được là vì electron tư do trong mạng tinh thể kim loại gây ra.
(d) Nhôm, sắt, crom không tan trong dung dịch loãng, nguội.
(e) Hỗn hợp và Cu (tỉ lệ mol 1:1) tan hết trong dung dịch HCl dư.
Số nhận định đúng là
Đáp án B.
(a) sai vì ăn mòn hóa học không làm phát sinh dòng điện, ăn mòn điện hóa mới làm phát sinh dòng điện.
(b) sai:
(c) đúng.
(d) sai vì nhôm, sắt, crom không tan trong dung dịch đặc, nguội.
(e) đúng.
Câu 40:
Hỗn hợp E gồm chất X () và chất Y () đều là các muối amoni của axit cacboxylic với amin. Cho 0,12 mol E tác dụng vừa đủ với dung dịch chứa 0.19 mol NaOH, đun nóng, thu được sản phẩm hữu cơ gồm 18,24 gam một muối và 7,15 gam hỗn hợp hai amin. Phần trăm khối lượng của Y trong E là
Đáp án A.
Vì chỉ thu được 1 muối nên đó là muối đơn chức.
nmuối
