Trắc nghiệm chuyên đề Hóa 9 Chủ đề 5: Bài toán đốt cháy Hidrocacbon có đáp án
Trắc nghiệm chuyên đề Hóa 9 Chủ đề 5: Bài toán đốt cháy Hidrocacbon có đáp án
-
297 lượt thi
-
12 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Khi đốt hoàn toàn 3 gam một hợp chất hữu cơ A thu được 8,8 gam CO2 và 5,4 gam H2O
a) Trong A có chứa những nguyên tố nào?
b) Biết phân tử khối của A nhỏ hơn 40. Xác định công thức phân tử của A?
c) A có làm mất màu dung dịch brom không?
a)
→ mO = 3 – (mC + mH) = 3 – 2,4 – 0,6 = 0
→ A chỉ chứa 2 nguyên tố C và H
b)
nC : nH = 0,2 : 0,6 = 1 : 3
→ Công thức đơn giản nhất của A: (CH3)n
MA < 40 → 15n < 40 → n < 2,67 → n chỉ có thể là 1 hoặc 2
TH 1: n = 1 → Công thức phân tử của A là CH3 ( Loại)
TH 2: n = 2 → Công thức phân tử của A là C2H6 ( thỏa mãn)
c) C2H6 không làm mất màu dung dịch brom
Câu 2:
Đốt cháy hoàn toàn 0,15 mol hỗn hợp A gồm 2 hidrocacbon no thu được 9,45g H2O. Cho sản phẩm cháy vào dung dịch Ca(OH)2 dư thì khối lượng kết tủa thu được là bao nhiêu?
nH2O = 9,45/18 = 0,525 mol
nA = nH2O – nCO2 ⇒ nCO2 = nH2O – nA =0,525-0,15 = 0,375 mol
nCaCO3 = nCO2 = 0,375 mol
⇒ mCaCO3 = 0,375.100 = 37,5g
Câu 3:
nX = 1,68/84 = 0,02 mol
nCO2 = 5,28/44 = 0,12 mol ⇒ nC = 0,12 mol
Gọi x là số nguyên tử C trong phân tử X, ta có:
x = nC/nX = 0,12/0,02 = 6 (nguyên tử C)
Câu 4:
Chọn đáp án B
Câu 5:
Đốt cháy CxHy và CO thu được số mol CO2 bằng số mol H2O.
Gọi số mol của CxHy và CO lần lượt là a và b.
Theo định luật bảo toàn nguyên tố ta có:
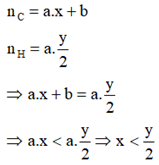
Vậy khi đốt cháy hidrocacbon CxHy có nCO2< nH2O.
Vậy hợp chất hidrocacbon là ankan, suy ra CTTQ là CnH2n+2.
Câu 6:
Chọn đáp án B
VCO2 = 65-25 = 40 cm3
⇒ VO/H2O = VO/O2(bđ) - VO/CO2 - VO/O2(dư) = 80.2-40.2-25.2 = 30cm3
Gọi hidrocacbon là CxHy, ta có:
x = VCO2/10 = 40/10 = 4
y = 2VH2O/10 = 2.30/10 = 6
Vậy Hidrocacbon có CT là C4H6.
Câu 7:
Chọn đáp án C
Câu 8:
Chọn đáp án A.
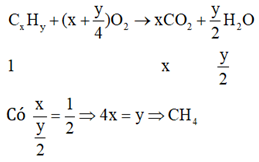
Câu 9:
Tương tự bài 6.
Câu 10:
Ta biết hỗn hợp X chỉ gồm các hidrocacbon có nguyên tố C và H.
Quy đổi hỗn hợp X gồm C và H.
Khi đó ta có: mX = mC + mH
nCO2 = 26,4/44 = 0,6 mol ⇒ nC = 0,6 mol ⇒ mC = 0,6.12 = 7,2g
nH2O = 16,2/18 = 0,9 mol ⇒ nC = 0,9.2 = 1,8 mol ⇒ mH = 1,8g
⇒mX = mC + mH = 7,2+1,8 = 9g
Câu 11:
nCO2 = 7,84/22,4 = 0,35 mol
nH2O = 11,7/18 = 0,65 mol
⇒ nCO2 < nH2O ⇒ ankan
Câu 12:
nankan = 5,6/22,4 = 0,25 mol
nH2O = 8,1/18 = 0,45 mol
Vì ankan có CTTQ là CnH2n+2 nên ta có:
nH2O - nCO2 = nankan ⇒ nCO2 = 0,45 - 0,25 = 0,2 mol
Vì CO2 tác dụng với Ca(OH)2 dư nên tạo kết tủa hoàn toàn.
⇒ n↓ = nCO2 = 0,2 mol
⇒ m↓ = 0,2.100 = 20g
