Bộ 30 đề thi vào 10 Chuyên Hóa năm 2022-2023 có lời giải chi tiết ( Đề 1)
-
15676 lượt thi
-
25 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 2:
b) Cho đồng thời các chất X, Y, Z, T có cùng số mol vào trong một lượng nước dư, rồi đun nhẹ thu được khí A, dung dịch B và kết tủa C. Xác định các chất có trong A, B và C. Viết các phương trình hóa học xảy ra.
b) Đặt số mol mỗi chất là 1 mol.
BaO + H2O → Ba(OH)2
1 1 mol
Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3↓
1 1 2
NaOH + NH4Cl → NaCl + NH3↑ + H2O
1 1 1
NaOH + NH4NO3 → NaNO3 + NH3↑ + H2O
1 1 1
Vậy khí A là NH3, dung dịch B gồm NaCl và NaNO3, kết tủa C là BaCO3.
Câu 3:
2. Chia 76,8 gam hỗn hợp F gồm Mg và Fe thành hai phần bằng nhau:
- Cho phần 1 vào dung dịch HCl dư, thu được 17,92 lít H2 (đktc).
- Cho phần 2 vào 0,6 lít dung dịch Cu(NO3)2 aM, thu được dung dịch G và b gam chất rắn H. Cho dung dịch G vào dung dịch NaOH dư, lọc lấy kết tủa rồi nung đến khối lượng không đổi, thu được 40 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Tính các giá trị a và b.
2.
Khối lượng mỗi phần = 76,8/ 2 = 38,4 gam.
Đặt số mol trong mỗi phần của Mg là x, Fe là y.
+ Phần 1: mol → x + y = 0,8 (1)
Mà 24x + 56y = 38,4 (2)
Giải (1) và (2) ta có: x = 0,2 và y = 0,6
+ Phần 2:
Giả sử rắn chỉ gồm MgO → nMgO = 1,0 mol > 0,8 loại → Cu2+ hết, Fe dư.
Vậy rắn gồm MgO (x mol) và Fe2O3 (z mol)
Mg + Cu2+ → Mg2+ + Cu
0,2 0,2 0,2 0,2
Fe + Cu2+ → Fe2+ + Cu
Trước: 0,6 (0,6a – 0,2)
P/ ư: (0,6a – 0,2) (0,6a – 0,2) (0,6a – 0,2) (0,6a – 0,2)
Sau: (0,8-0,6a) 0
Mà nên 40.0,2 + 160.(0,3a-0,1) = 40 → a = 1
Ta có: b = mCu + mFe (dư) = 64.0,6 + 56.0,2 = 49,6 (gam)
Câu 4:
1. Mùa hè năm ngoái, bạn Tuấn được bố mẹ cho về quê ngoại thăm ông, bà. Bà ngoại Tuấn hay ăn trầu nên đã bảo Tuấn đi xin ít vôi tôi của hàng xóm, Tuấn đã lấy một cái ca bằng nhôm để đựng vôi tôi. Mấy hôm sau, khi bà ngoại Tuấn mang vôi ra ăn trầu thì thấy ca bị thủng và vôi bị chảy hết ra ngoài. Em hãy giúp Tuấn giải thích tại sao ca bằng nhôm đựng vôi tôi lại bị thủng?
1.
Vôi tôi là Ca(OH)2
Khi đựng vôi tôi vào ca bằng nhôm xảy ra các phản ứng sau:
Al2O3 + Ca(OH)2 → Ca(AlO2)2 + H2O
2Al + Ca(OH)2 + 2H2O → Ca(AlO2)2 + 3H2
Ca nhôm bị ăn mòn dần theo các phương trình hóa học ở trên nên khiến ca bị thủng.
Câu 5:
2. Mặc dù nhôm là một kim loại khá hoạt động (chỉ sau kim loại kiềm và kiềm thổ) nhưng nhôm vẫn được dùng để chế tạo các dụng cụ nhà bếp như xoong, nồi, … Hãy giải thích ngắn gọn.
2.
Kim loại nhôm dễ dàng phản ứng với O2 trong không khí để tạo Al2O3 che phủ xung quanh bề mặt kim loại nhôm. Các vật dụng và dụng cụ nhà bếp bằng nhôm luôn được bảo vệ bởi một lớp màng oxit nhôm rất mỏng và bền, ngăn không cho nước và không khí thấm qua. Mặt khác, nhiệt độ nóng chảy của Al2O3 rất cao so với nhiệt độ ngọn lửa nên nó không bị phá hủy khi đun nấu.
Câu 6:
3. Dưới đây là sơ đồ chuyển hóa có sự tham gia của nhôm và hợp chất của nhôm.
Al + HCl → A + H2
A + G → D + E + H
A + B + C → D + E
A + NaOH dư → B + C + E
B + H + C → D + G
Xác định các chất A, B, C, D, E, G và H. Viết phương trình hóa học xảy ra.3.
A: AlCl3, B: NaAlO2, C: H2O, D: Al(OH)3, E: NaCl, G: NaHCO3 và H: CO2
2Al + 6HCl → 2AlCl3 + 3H2
AlCl3 + 3NaHCO3 → Al(OH)3↓ + 3NaCl + 3CO2↑
AlCl3 + 3NaAlO2 + 6H2O → 4Al(OH)3↓ + 3NaCl
AlCl3 + 4NaOH dư → NaAlO2 + 2H2O + 3NaCl
NaAlO2 + CO2 + H2O → Al(OH)3↓ + NaHCO3
Câu 7:
4. Trong tự nhiên, nhôm có trong quặng boxit. Quặng boxit có chứa Al2O3.2H2O, tạp chất là Fe2O3, SiO2, … Để sản xuất nhôm, người ta sẽ loại bỏ tạp chất để thu được Al2O3, sau đó tiến hành điện phân nóng chảy (đpnc) với điện cực dương (anot bằng than chì) hỗn hợp Al2O3 và criolit theo phản ứng sau:
2Al2O3 4Al + 3O2
Biết hiệu suất quá trình điện phân là 90% và quặng boxit chứa 25% (về khối lượng) tạp chất không chứa nhôm.
a) Cho biết vai trò của criolit trong quá trình điện phân.
4.
a) Vai trò của criolit trong quá trình điện phân:
+ Làm giảm nhiệt độ nóng chảy của Al2O3
+ Làm tăng độ dẫn điện của Al2O3 nóng chảy.
+ Tạo lớp ngăn cách để bảo vệ nhôm nóng chảy.
Câu 8:
b) Sau một thời gian điện phân, người ta thấy cực dương bị ăn mòn và phải thay thế. Giải thích và viết phương trình hóa học minh họa.
b) Trong quá trình điện phân, O2 sinh ra tại cực dương, tại đây xảy ra phản ứng ăn mòn điện cực than chì: C + O2 → CO2.
Do đó sau một thời gian điện phân, người ta thấy cực dương bị ăn mòn và phải thay thế.
Câu 9:
c) Ta có sơ đồ:
Al2O3 → 2Al
102 g → 54 g
? tấn → 54 tấn
Khối lượng quặng boxit cần dùng là:
= 151,11 tấn.
Câu 10:
Kali là một trong số các nguyên tố hóa học quan trọng đối với cơ thể con người. Thiếu kali, cơ thể đối mặt với nguy cơ yếu cơ, liệt cơ và rối loạn nhịp tim, … Kali đặc biệt cần thiết cho hệ thần kinh. Sự sụt giảm nồng độ kali trong máu có thể ảnh hưởng đến khả năng tạo ra xung thần kinh của cơ thể. Kali cũng là nguyên tố rất cần thiết cho cây trồng, đặc biệt là cho những cây ăn quả.
1. Đồng vị là những nguyên tử của cùng một nguyên tố có cùng số proton, khác số nơtron. Trong tự nhiên, kali có ba loại đồng vị là 39K (93,258%), 40K (0,012%) và 41K (6,730%).
a) Tính nguyên tử khối trung bình của kali.
Hướng dẫn giải:
1.
a) = 39,135
Câu 11:
b) Chuối là một trong những loại hoa quả giàu kali. Khi thi đấu, nhiều vận động viên tennis thường ăn chuối để bổ sung kịp thời lượng kali cho cơ thể. Một quả chuối nặng 150 g chứa 420 mg kali. Tính khối lượng mỗi loại đồng vị của kali trong quả chuối này.
b)
Câu 12:
c) Kali luôn có mặt trong máu người với một nồng độ ổn định. Một người trưởng thành nặng 70 kg có lượng máu trong cơ thể là 5 lít, có chứa lượng kali trong máu từ 0,690 – 0,986 g. Tính nồng độ kali (mmol/l) có trong máu người trưởng thành trên.
c) Nồng độ kali trong máu người này trong khoảng từ
M
đến M
Câu 13:
2. Cây thanh long có nguồn gốc nhiệt đới. Chúng dễ trồng trên nhiều loại đất khác nhau như đất bạc màu (Bình Thuận), đất phèn (đồng bằng sông Cửu Long), đất đỏ (Đồng Nai), … Chất lượng thanh long phụ thuộc nhiều vào phân bón. Chế độ bón giàu đạm, ít kali thường cho trái có độ ngọt kém, mau hư thối, khó bảo quản và vận chuyển. Ngược lại chế độ bón phân cân đối đạm và kali hoặc giàu kali sẽ cho trái có độ ngọt cao hơn, trái cứng chắc và lâu hư thối, dễ bảo quản, vận chuyển.
Độ dinh dưỡng của một số loại phân được quy định như sau:
- Độ dinh dưỡng của phân đạm được tính bằng %m(N) có trong phân.
- Độ dinh dưỡng của phân lân được tính bằng %m(P2O5) tương ứng với lượng P có trong phân.
- Độ dinh dưỡng của phân đạm được tính bằng %m(K2O) tương ứng với lượng K có trong phân.
a) Tính độ dinh dưỡng của phân KNO3, biết loại phân này chứa 20% (về khối lượng) tạp chất không chứa kali và nitơ.
a) Xét 100 gam phân KNO3 có gam
→ →
→Câu 14:
b) Bảng dưới đây hướng dẫn liều lượng trộn tỉ lệ các loại phân bón để bón cho cây thanh long.
|
Giai đoạn phát triển của cây |
Loại phân bón |
Thành phần |
|
Ngay trước khi thu hoạch |
N P2O5 Chất hữu cơ |
216 g 216 g 20 kg |
|
Hai tháng sau khi thu hoạch quả |
N P2O5 K2O |
162 g 144 g 45 g |
|
Ngay sau khi cây ra hoa |
N P2O5 K2O |
54 g 288 g 120 g |
|
Khi trái non đang phát triển |
N P2O5 K2O |
108 g 72 g 135 g |
Nguồn: http://chemicalsolutionstech.wordpress.com
Một bác nông dân trộn phân để bón cho thanh long như sau: Trộn 430 g KCl (phân kali) với 1312 g NaNO3 (phân đạm) và 334 g Na3PO4 (phân lân). Cho biết bác nông dân đó chuẩn bị bón phân cho cây thanh long ở giai đoạn nào?b)
gam
gam
gam
So sánh bảng trên ta thấy, lượng phân kali và đạm bón nhiều, lân bón ít ứng với giai đoạn cây thanh long khi có trái non đang phát triển.
Kiểm tra lại tỉ lệ phân:
Câu 15:
1. Đốt cháy hoàn toàn 4,16 gam hiđrocacbon A (mạch hở, là chất khí ở điều kiện thường và MA > 26) rồi dẫn hỗn hợp sản phẩm cháy vào dung dịch Ca(OH)2 dư, thu được 32 gam kết tủa trắng.
a) Tìm công thức phân tử và viết công thức cấu tạo của A.
a) mol →
→nC : nH = 0,32 : 0,32 = 1 : 1
Đặt công thức của hiđrocacbon A là CxHx (MA > 26, x ≤4 và chẵn ), ta có bảng sau:
|
x |
2 |
4 |
|
CTPT |
C2H2 |
C4H4 |
|
M |
26 (loại) |
52 (t/m) |
Vậy CTPT của A là C4H4.
Các CTCT có thể có của A (∆ = 3), mạch hở là
CH≡C-CH=CH2 hoặc CH2=C=C=CH2.
Câu 16:
b) Dẫn 1,12 lít A (đktc) vào lượng dư dung dịch AgNO3/NH3, thu được m gam kết tủa. Tính m.
b) Vì A có phản ứng với dung dịch AgNO3/NH3 nên CTCT của A là CH≡C-CH=CH2.
mol
→ Khối lượng kết tủa CAg≡C-CH=CH2 = 0,05.159 = 7,95 gam.
Câu 17:
2. Biến thiên entanpi của phản ứng (kí hiệu là ∆H) có thể hiểu đơn giản là nhiệt tỏa ra hoặc thu vào khi phản ứng hóa học xảy ra. Nếu phản ứng tỏa nhiệt thì ∆H có dấu âm và ngược lại, nếu phản ứng thu nhiệt thì ∆H có dấu dương.
Khi một phản ứng hóa học xảy ra, các liên kết trong chất phản ứng bị cắt đứt và liên kết mới được hình thành, tạo nên chất sản phẩm. Để tính ∆H của phản ứng, người ta dựa vào năng lượng các liên kết (Elk). Elk là năng lượng cần cung cấp để cắt đứt một liên kết thành các nguyên tử ở thể khí. Năng lượng tỏa ra khi hình thành liên kết đó từ các nguyên tử ở thể khí cũng có giá trị bằng giá trị của Elk nhưng có dấu ngược lại. Elk của một số liên kết được cho trong bảng sau:
|
Liên kết |
C≡C |
C-C |
C-H |
H-H |
|
Elk (kJ/mol) |
839,0 |
343,3 |
418,4 |
432,0 |
Xét phản ứng:
C2H2 + 2H2 → C2H6 (1)
Dựa vào bảng số liệu trên hãy:
a) Tính năng lượng cần cung cấp để phá vỡ liên kết của các chất tham gia trong phản ứng (1) (lưu ý hệ số của các chất trong phương trình phản ứng).
a) Năng lượng cần cung cấp để phá vỡ liên kết của các chất tham gia trong phản ứng (1) là
Elk (đầu) = 2.418,4 + 839,0 + 2.432,0 = 2539,8 (kJ/mol)
Câu 18:
b) Tính năng lượng tỏa ra khi hình thành các liên kết trong chất sản phẩm của phản ứng (1).
b) Năng lượng tỏa ra khi hình thành các liên kết trong chất sản phẩm của phản ứng (1)
Elk (cuối) = 343,3 + 6.418,4 = 2853,7 (kJ/mol)
Câu 19:
c) Từ các kết quả trên, xác định ∆H của phản ứng (1) và cho biết phản ứng (1) tỏa nhiệt hay thu nhiệt?
c) ∆H = Elk (đầu) - Elk (cuối) = 2539,8 – 2853,7 = - 313,9 (kJ/mol) < 0
Vậy (1) là phản ứng tỏa nhiệt, năng lượng tỏa ra của phản ứng (1) là 313,9 (kJ/mol).
Câu 20:
1. Axit X (chỉ chứa C, H, O trong phân tử) là một hợp chất hữu cơ sinh học. Khi vận động mạnh trong một thời gian dài và cơ thể không được cung cấp đủ oxi, glucozơ trong cơ thể sẽ bị chuyển hóa thành axit X. Axit X sinh ra trong quá trình vận động là nguyên nhân chính tạo ra cảm giác mỏi ở cơ bắp. Axit X cũng có mặt trong sữa chua và dưa muối.
a) Bằng phương pháp phổ khối lượng MS, người ta xác định được phân tử khối của X là 90. Bằng các phương pháp phổ hiện đại khác như phổ hồng ngoại IR và phổ cộng hưởng từ hạt nhân NMR, người ta xác định được phân tử của X chứa các nhóm chức –OH và –COOH cùng liên kết với một nguyên tử cacbon. Xác định công thức phân tử và công thức cấu tạo của X.
1.
a) Vì MX = 90 nên X chỉ có thể chứa 1 nhóm –OH và 1 nhóm –COOH.
Đặt CT của X là R(OH)(COOH) → MR = 28
→CTPT phù hợp của X là: C2H4(OH)(COOH) hay C3H6O3
CTCT phù hợp: CH3-CH(OH)COOH
Hay
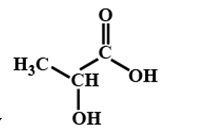
Câu 21:
b) Nêu một biện pháp đơn giản giúp vận động viên giảm cảm giác mỏi cơ do axit X bị tích tụ nhiều trong quá trình tập luyện thể thao.
b) Một số biện pháp giúp hạn chế tích tụ axit lactic gây mỏi cơ:
- Uống đủ nước, bổ sung oserol khi tập thể thao nặng ra nhiều mồ hôi.
- Nghỉ ngơi giữa các buổi tập, thực hiện bài tập thở.
- Làm nóng và giãn cơ để hạn chế tích tụ axit lactic….
Câu 22:
c) Để axit X trong bình phản ứng, cho thêm vài giọt axit sunfuric đặc (làm xúc tác), rồi đun nóng. Sau một thời gian, thu được hỗn hợp các chất, trong đó có hợp chất hữu cơ Y. Trong phân tử Y, nguyên tố oxi chiếm 44,44% về khối lượng và phân tử khối của Y nằm trong khoảng từ 75 đến 150. Xác định công thức phân tử, công thức cấu tạo của Y. Viết phương trình hóa học của phản ứng tạo ra chất Y.
c) Khi có mặt axit sunfuric đặc (làm xúc tác), axit lactic sẽ thực hiện phản ứng este hóa. Dễ thấy 90.2 – 150 >18 nên sản phẩm tạo thành phải là este vòng, 2 chức.
Phương trình hóa học:
C3H6O3 C6H8O4 + 2H2O
Kiểm tra lại: %mO = = 44,44% (thỏa mãn đề bài)
Vậy CTPT của Y là C6H8O4.
CTCT của Y là
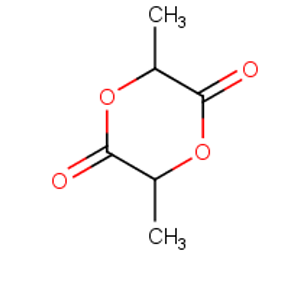
Câu 23:
2. Chất Z là một tác nhân hóa học được dùng nhiều trong tổng hợp hữu cơ.
a) Bằng phương pháp phân tích nguyên tố người ta xác định được thành phần phần trăm về khối lượng của N và H trong Z lần lượt là 87,5% và 12,5%. Do điều kiện thí nghiệm không đầy đủ nên người ta chỉ xác định được phân tử khối của Z nằm trong khoảng 30 đến 40. Viết công thức cấu tạo của chất Z.
2.
a) Ta có: N : H =
Vì 30 < MZ < 40 nên Z chỉ có 1 hoặc 2 nguyên tử N, vì số H chẵn nên số N cũng phải chẵn
→ Z phải có 2 nguyên tử N → CTPT của Z là N2H4.
CTCT của Z là NH2-NH2.
Câu 24:
b) Biết chất Z có tính khử, viết phương trình hóa học xảy ra khi cho Z phản ứng với Cl2.
b) N2H4 + Cl2 → N2 + HCl
Câu 25:
c) Ngoài việc thu được chất Y khi nhỏ axit sunfuric vào axit X (trong Câu V.1, ý c ở trên), người ta còn thu được chất hữu cơ T. Quá trình hình thành và chuyển hóa T (có sử dụng tác nhân Z) thành chất hữu cơ Q như sau:
X T P Q
Dự đoán công thức cấu tạo của chất T, P và Q, biết trong phân tử của Q, N chiếm 32,56% về khối lượng.
c) CTCT của các chất:
T là CH3-CH(OH)-COOCH(CH3)COOH hoặc CH2=CH-COOCH(CH3)COOH
P là CH3-CH(OH)-COOCH(CH3)COOCH3 hoặc CH2=CH-COOCH(CH3)COOCH3
Vì trong Q có N chiếm 32,56%, mà Q phải có 2 nguyên tử N nên MQ = 86 → Q là CH2=CH-CONH-NH2
