Bộ đề thi thử môn Hóa THPT Quốc gia năm 2022 có lời giải (30 đề)
Bộ đề thi thử môn Hóa THPT Quốc gia năm 2022 có lời giải (Đề 7)
-
2858 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 3:
Chọn A
và
dư dư = 0,05
trong
Câu 4:
Chọn C
phản ứng = 5,6 gam
Câu 5:
Chọn D
gam
Câu 6:
Thí nghiệm xác định định tính nguyên tố cacbon và hidro trong phân tử saccarozơ được tiến hành theo các bước sau
- Bước 1: Trộn đều khoảng 0,2 gam saccarozơ với 1 đến 2 gam đồng (II) oxit, sau đó cho hỗn hợp vào ống nghiệm khô (ống số 1) rồi thêm tiếp khoảng 1 gam đồng (II) oxit để phủ kín hỗn hợp. Nhồi một nhúm bông có rắc bột CuSO4 khan vào phần trên ống số 1, rồi nút bằng nút cao su có ống dẫn khí.
- Bước 2: Lắp ống số 1 lên giá thí nghiệm, rồi nhúng ống dẫn khí vào dung dịch Ca(OH)2 đựng trong ống nghiệm (ống số 2)
- Bước 3: Dùng đèn cồn đun nóng ống số 1 (lúc đầu đun nhẹ, sau đó đun tập trung vào phần có hỗn hợp phản ứng)
Cho các phát biểu sau:
(a) Sau bước 3, màu trắng của CuSO4 khan chuyển thành màu xanh CuSO4.5H2O.
(b) Thí nghiệm trên còn được dùng để xác định định tính nguyên tố oxi trong phân tử saccarozơ.
(c) Dung dịch Ca(OH)2 được dùng để nhận biết CO2 sinh ra trong thí nghiệm trên.
(d) Ở bước 2, lắp ống số 1 sau cho miệng ống hướng lên.
(e) Kết thúc thí nghiệm: tắt đèn cồn, để ống số 1 nguội hẳn rồi mới đưa ống dẫn khí ra khỏi dung dịch trong ống số 2.
Số phát biểu đúng làChọn A
(a) Đúng
(b) Đúng:
(c) Sai, lắp sao cho miệng ống hơi cúi xuống (thấp hơn đáy ống), mục đích là làm cho nước bám vào thành ống nghiệm (CuSO4 khan có thể không hấp thụ hết) không chảy ngược xuống đáy ống nghiệm (gây vỡ ống).
(d) Sai, thí nghiệm chỉ định tính được C và H trong saccarozơ.
(e) Sai, tháo ống dẫn khí trước rồi mới tắt đèn cồn. Nếu làm ngược lại, khi tắt đèn cồn trước, nhiệt độ ống 1 giảm làm áp suất giảm, nước có thể bị hút từ ống 2 lên ống 1, gây nguy cơ vỡ ống 1Câu 10:
Chọn B
là este no, đơn chức, mạch hở.
Số X là C3H6O2.
Chất rằn gồm RCOOK (0,16) và KOH dư (0,04)
m rắn
X là là
Câu 11:
Chọn D
Câu 13:
Chọn B
(muối)
(muối)
Để phương trình nghiệm đúng thì cả hai dấu bằng phải đồng thời xảy ra.
(muối) = (muối) = 0,1
Ancol là và muối là HCOONa (0,1)
và b = 0,03
X là HCOOCH3 (0,04) và
Câu 14:
Chọn B
X và Y đều tác dụng với dung dịch AgNO3 dư trong NH3 theo tỉ lệ mol 1 : 2.
là và Y là
Dễ thấy X, Y đều có k = số C nên:
Câu 16:
Chọn B
Sản phẩm khử
Câu 17:
Cho các sơ đồ phản ứng:
(1) E + NaOH → X + Y; (2) F + NaOH → X + Z; (3) Y + HCl → T + NaCl
Biết E, F đều là các hợp chất hữu cơ no, mạch hở, chỉ chứa nhóm chức este (được tạo thành từ axit cacboxylic và ancol) và trong phân tử có số nguyên tử cacbon bằng số nguyên tử oxi; E và Z có cùng số nguyên tử cacbon; ME < MF < 175.Cho các phát biểu sau:
(a) Nhiệt độ sôi của E thấp hơn nhiệt độ sôi của CH3COOH
(b) Có hai công thức cấu tạo của F thỏa mãn sơ đồ trên.
(c) Hai chất E và T có cùng công thức đơn giản nhất
(d) Đốt cháy hoàn toàn Z, thu được Na2CO3, CO2 và H2O.
(e) Từ X điều chế trực tiếp được CH3COOH.
Số phát biểu đúng là
Chọn A
E và F có số C bằng số O nên có dạng
Số chức este là 0,5n
E và F đều no, mạch hở nên
là và F là
là muối natri. Mặt khác, E và Z cùng C nên:
E là HCOOCH3; X là CH3OH và Y là HCOONa.
F là là
T là HCOOH.
(a) Đúng
(b) Sai
(c) Sai, CTĐGN của E là của T là
(d) Sai, đốt Z tạo Na2CO3, CO2 (không tạo H2O).
(e) Đúng:
Câu 19:
Chọn A
max Phải có kim loại dư, Cu2+ hết.
Nếu chỉ Zn phản ứng thì khối lượng chất rắn phải giảm, vô lý. Vậy Zn phản ứng hết, Fe phản ứng một phần.
Đặt a, b, c là số mol Zn, Fe phản ứng với Fe dư
m rắn
Câu 20:
Chọn A
Bảo toàn
gamCâu 21:
Cho các phát biểu sau:
(1) Tất cả các nguyên tố kim loại đều là chất rắn ở điều kiện thường.
(2) Để xử lí thủy ngân bị rơi vãi người ta dùng bột lưu huỳnh.
(3) Tính dẫn điện được sắp xếp là: Ag > Cu > Au > Al > Fe.
(4) Cho Mg tác dụng với dung dịch FeCl3 dư thu được Fe.
(5). Khi cho Na dư vào dung dịch CuSO4 thấy có khí thoát ra, đồng thời thu được kết tủa màu xanh.
Số phát biểu đúng làChọn C
(1) Sai, Hg là chất lỏng điều kiện thường
(2) Đúng
(3) Đúng
(4) Sai, dư
(5) Đúng:
Câu 22:
Chọn A
Để tạo 1 mol khí X cần k mol electron
là N2
Câu 23:
Khi nhúng thanh Mg có khối lượng m gam vào dung dịch hỗn hợp X chứa a mol Cu(NO3)2 và b mol HCl ta có đồ thị biểu diễn sự phụ thuộc của khối lượng Mg vào thời gian phản ứng được biểu diễn như hình vẽ dưới đây:
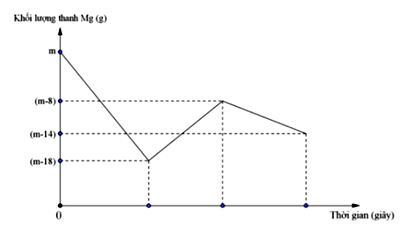
Chọn B
Đoạn 1: Khối lượng Mg giảm 18 gam (0,75 mol)
Đoạn 2: Khối lượng Mg tăng gam
Đoạn 3: Khối lượng Mg giảm gam (0,25 mol)
Vậy
Câu 24:
Chọn B
Muối gồm và
m muối = 68,4 gamCâu 25:
Chọn C
Câu 26:
Chọn C
Câu 28:
Chọn A
Quy đổi Z thành:
và
m muối
Số N trung bình tỉ lệ mol 1 : 1 và Y có 1N nên X có 5N sai.
Nếu Y là Ala thì X có số và số
Vậy Y là Không thỏa mãn giả thiết , loại.
Vậy Y là Gly và X là
Kết luận D đúngCâu 29:
Chọn D
Bảo toàn khối lượng
Số
Số
là
và
dạng
là
Muối còn lại là
gamCâu 31:
Chọn D
Câu 32:
Chọn A
Các chất trong dãy làm mất màu dung dịch Br2 là:
Metanal, axit metanoic, phenol, stirenCâu 33:
Chọn D
X khi tác dụng với dung dịch CuCl2 vừa thu được kết tủa, vừa thi được khí:
Câu 34:
Cho các phát biểu sau:
(1) Có thể dùng Cu(OH)2 trong môi trường kiềm để phân biệt các dung dịch glucozơ, etanol và lòng trắng trứng ;
(2) Ở nhiệt độ thường, C2H4 phản ứng được với nước brom;
(3) Các este đơn chức đều tác dụng với NaOH, đun nóng theo tỉ lệ mol 1:1;
(4) Ứng với công thức C3H7O2N có 2 amino axit là đồng phân cấu tạo của nhau;
(5) Oxi hóa glucozơ bằng H2( XT Ni, t0C) thu được sobitol ;
(6) Anilin là chất lỏng, không màu, ít tan trong nước, nặng hơn nước. Để lâu trong không khí, anilin có nhuốm màu hồng vì bị oxi hoá;
(7) Cao su buna có tính đàn hồi và độ bền tốt hơn cao su thiên nhiên;
(8) Toluen và stiren đều làm mất màu dung dịch thuốc tím ở điều kiện thường.
Số phát biểu không đúng làChọn B
(1) Đúng, glucozơ tạo phức xanh lam, lòng trắng trứng tạo phức tím, etanol không phản ứng.
(2) Đúng:
(3) Sai, este đơn chức của phenol (ví dụ ) tác dụng với NaOH theo tỉ lệ 1:2
(4) Đúng: và
(5) Sai, khử glucozơ bằng H2.
(6) Sai, anilin hóa nâu đen vì bị oxi hóa.
(7) Sai
(8) Sai, toluene cần đun nóng, stiren phản ứng ngay điều kiện thườngCâu 35:
Chọn D
Y là
Amin và ancol là và
G chứa 3 muối khan là
Muối gồm HCOOK (0,1), GlyK (0,1) và K2CO3 (0,15)
Câu 37:
Chọn C
Câu 38:
Cho x mol glyxin tác dụng vừa đủ dung dịch HNO3, sau phản ứng thu được 28,98 gam muối. Giá trị của x là:
Chọn D
n muối = 0,21
Câu 39:
Chọn C
Dung dịch X chứa , để lượng kết tủa lớn nhất nhưng dùng NaOH ít nhất thì phản ứng là:
Bảo toàn lúc đầu
Bảo toàn
m tinh bột gamCâu 40:
Chọn C
Trong Y đặt và lần lượt là a, b, c, d mol. Ta có trong Y = 0,0225 mol.
Sản phẩm sau đó là
Vừa đủ để tạo ra
Sau đó thêm tiếp dư Tạo thêm và
Như trên đã có tổng = 0,455
Bảo toàn H:
mol
Bảo toàn khối lượng:
m muối + m khí +
gam.
