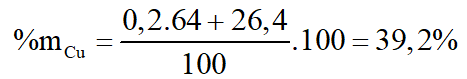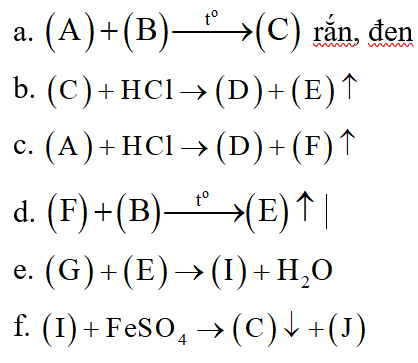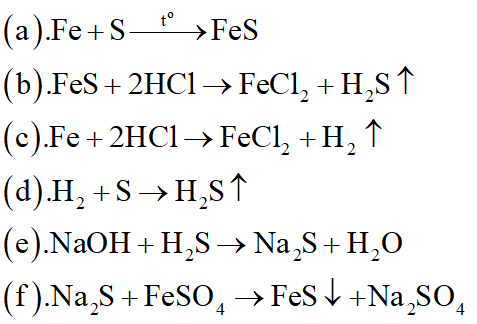Trắc nghiệm tổng hợp Hóa 9 Chương 2: Các loại hợp chất vô cơ có đáp án - Đề 6
-
1121 lượt thi
-
16 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Hãy chọn 1 đơn chất, 1 oxit, 1 hiđroxit và 2 muối khác loại nhau đều tác dụng được với cả dung dịch HCl và dung dịch NaOH. Viết các phương trình phản ứng.
+ Đơn chất cần chọn là Al hoặc Zn:
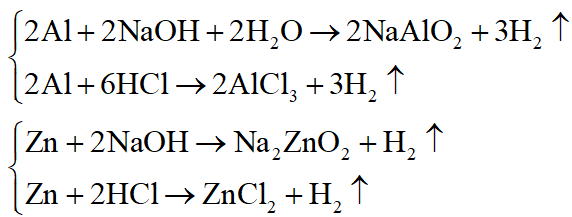
+ Oxit cần chọn là Al2O3 hoặc ZnO
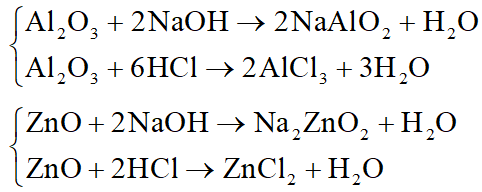
+ Hiđroxit cần chọn là Al(OH)3 hoặc Zn(OH)2:
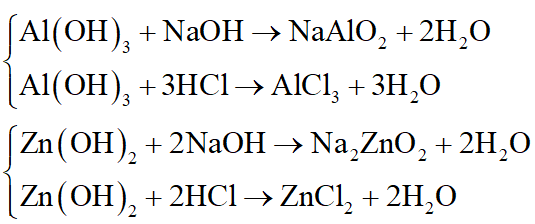
+ Muối cần chọn là NaHCO3, (NH4)2CO3 hoặc KHS, Pb(NO3)2 hoặc …:
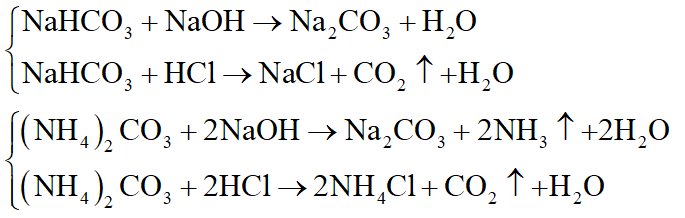
*Nhận xét:
- Kim loại có tính oxit, hiđroxit lưỡng tính như Al, Zn… vừa tác dụng với dung dịch axit (HCl, H2SO4 loãng…), vừa tác dụng với dung dịch bazơ (NaOH, KOH, Ba(OH)2,…).
- Oxit lưỡng tính (Al2O3, ZnO,…) vừa tác dụng với dung dịch axit (HCl, H2SO4 loãng…), vừa tác dụng với dung dịch bazơ (NaOH, KOH, Ba(OH)2,…).
- Hiđroxit lưỡng tính (Al(OH)3, Zn(OH)2…) vừa tác dụng với dung dịch axit (HCl, H2SO4 loãng…), vừa tác dụng với dung dịch bazơ (NaOH, KOH, Ba(OH)2,…).
- Các muối axit của axit yếu (NaHCO3, KHS, KHSO3…) vừa tác dụng với dung dịch axit (HCl, H2SO4 loãng…), vừa tác dụng với dung dịch bazơ (NaOH, KOH, Ca(OH)2, Ba(OH)2,…).
Câu 2:
Hãy nêu phương pháp loại bỏ khí có lẫn trong các khí khác và viết các phương trình hóa học.
a. CO2 có lẫn trong CO.
Sục hỗn hợp qua lượng dư dung dịch có tính bazơ như NaOH, KOH, Ca(OH)2, Ba(OH)2:
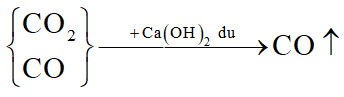
CO2 bị hấp thụ theo phản ứng sau:
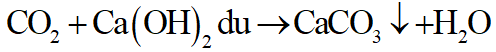
Thu khí thoát ra ta được CO.
Câu 3:
b. SO2 có lẫn trong C2H4.
Sục hỗn hợp qua lượng dư dung dịch có tính bazơ như NaOH, KOH, Ca(OH)2, Ba(OH)2:
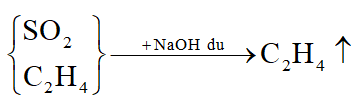
SO2 bị hấp thụ theo phản ứng sau:
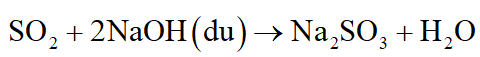
Thu khí thoát ra ta được C2H4.
Câu 4:
c. SO3 có lẫn trong SO2.
Sục hỗn hợp khí qua lượng dư dung dịch BaCl2 hoặc Ba(NO3)2:
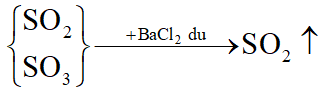
SO3 bị hấp thụ theo phản ứng sau:
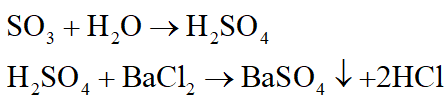
Thu khí thoát ra ta được SO2.
Câu 5:
Sục hỗn hợp khí qua lượng dư nước brom:
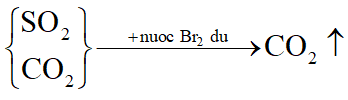
SO2 bị hấp thụ theo phản ứng sau:
Thu khí thoát ra ta được CO2.
Câu 6:
Có 3 ống nghiệm đựng 5 chất bột riêng biệt gồm: Mg(OH)2, Al(OH)3, BaCl2, Na2CO3, NaOH. Chỉ được dùng thêm H2O và CO2 hãy trình bày cách nhận biết các chất đó.
Hòa tan mỗi chất vào nước, 2 chất không tan là Mg(OH)2 và Al(OH)3.
Lấy 3 dung dịch trộn với nhau từng đôi một, 2 chất tạo kết tủa là BaCl2 và Na2CO3.
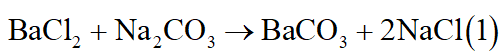
Lấy dung dịch NaOH đã biết cho vào 2 chất không tan, chất tan là Al(OH)3
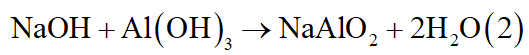
Lọc lấy kết tủa ở (1) cho vào nước rồi thổi CO2 dư
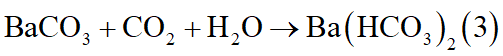
Lấy dung dịch Ba(HCO3)2 thu được ở (3) cho vào 2 dung dịch là BaCl2, Na2CO3, dung dịch có kết tủa là Na2CO3.
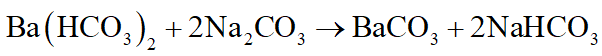
Hoặc thổi CO2 dư vào một trong 2 dung dịch BaCl2 hoặc Na2CO3 rồi rót vào dung dịch còn lại. Nếu không có kết tủa thì dung dịch đã thổi CO2 vào là Na2CO3.
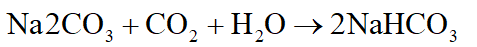
Nếu có kết tủa thì dung dịch đã thổi là BaCl2.
Câu 7:
Cho sơ đồ:
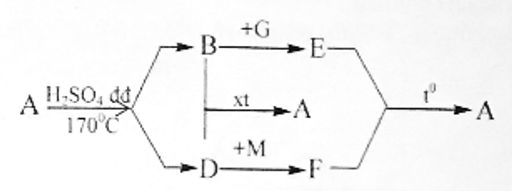
Xác định A, B, D, E, F, G, M (là ký hiệu các chất hữu cơ, vô cơ khác nhau), viết các phương trình phản ứng biết A có thể điều chế từ tinh bột và được dùng để pha chế xăng sinh học E5.
A có thể điều chế từ tinh bột và được dùng để pha chế xăng sinh học E5 nên suy ra A là C2H5OH:
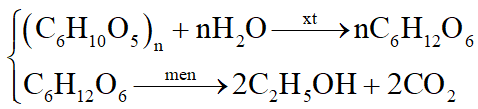
95% thể tích xăng truyền thống + 5% thể tích C2H5OH tạo ra xăng sinh học E5.
Các phương trình phản ứng:
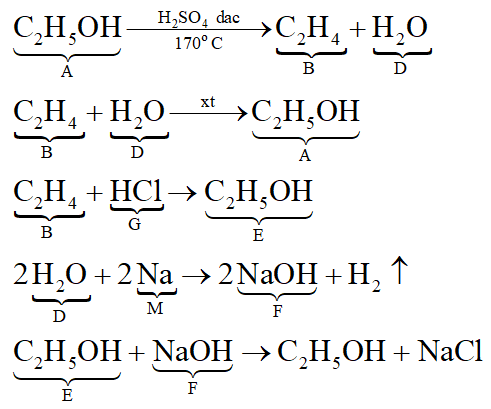
Câu 9:
Có các chất lỏng A, B, D, E, F không theo thứ tự gồm: Benzen, ancol etylic, axit axetic, dung dịch glucozơ, nước. Biết kết quả của những thí nghiệm như sau:
- Cho tác dụng với Na thì E không phản ứng.
- Cho tác dụng với CaCO3 thì chỉ có D phản ứng, có khí thoát ra.
- Cho tác dụng với dung dịch AgNO3/NH3 (hay Ag2O/NH3) thì B phản ứng tạo ra bạc.
- Khi đốt trong không khí thì A không cháy.
Xác định A, B, D, E, F (không cần viết các phương trình phản ứng).
E không tác dụng với Na nên E là benzen (C6H6).
D tác dụng với CaCO3 nên D là axit axetic (CH3COOH):
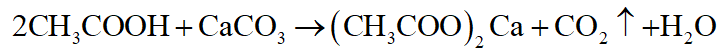
B có phản ứng tráng bạc nên B là glucozơ (C6H12O6):
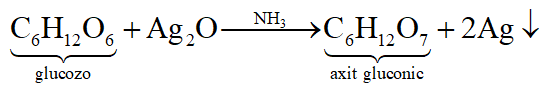
A không cháy nên A là H2O.
F là C2H5OH (ancol etylic)
*Nhận xét:
Tác dụng với Na đặc trưng cho hợp chất hiđro linh động như H2O, C2H5OH, CH3COOH,…:
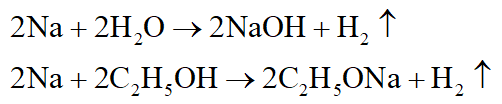
Tác dụng với CaCO3, Na2CO3,… đặc trưng cho hợp chất có tính axit như CH3COOH, C2H5OH, HOOC – COOOH,…:
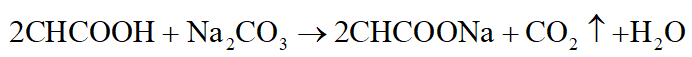
Tham gia phản ứng tráng bạc đặc trưng cho hợp chất có nhóm CHO như CH3CHO, glucozơ,…:
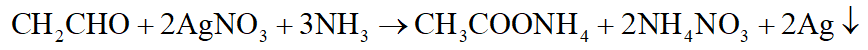
Câu 10:
Hòa hỗn hợp vào nước dư, lọc lấy riêng phần dung dịch và kết tủa Cu, Fe:
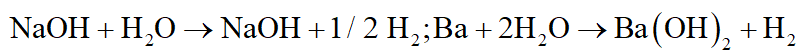
Thổi CO2 vào dung dịch thu được rồi đun sôi dung dịch, lọc lấy riêng kết tủa và dung dịch
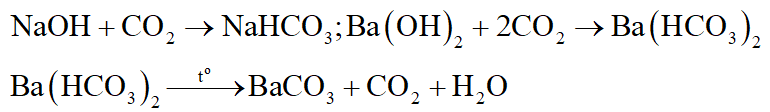
Cho riêng kết tủa và dung dịch tác dụng với dung dịch HCl dư, cô cạn 2 dung dịch rồi điện phân nóng chảy thu được Na, Ba riêng biệt.
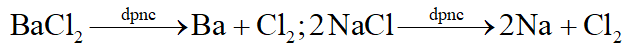
Hòa tan Cu, Fe bằng dung dịch HCl, lọc kết tủa thu được Cu. Điện phân dung dịch FeCl2 thu được Fe.
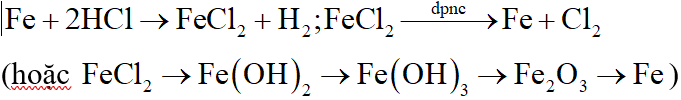
*Nhận xét:
Kim loại tác dụng với H2O ở điều kiện thường gồm kim loại kiềm (li, Na, K, Rb, Cs) và kim loại kiềm thổ (trừ Be, Mg) như Ca, Ba, Sr:
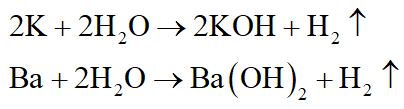
Cách duy nhất để điều chế kim loại kiềm, kiềm thổ và Al là điện phân nóng chảy hợp chất của chúng:
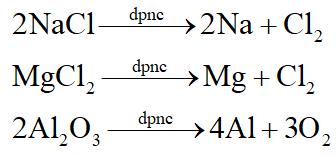
Để điều chế các kim loại sau Al trong dãy hoạt động hóa học có thể dùng C, CO, H2 khử oxit kim loại ở nhiệt độ cao hoặc điện phân dung dịch các muối của chúng.
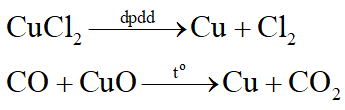
Câu 11:
A. Canxi
B. Cacbon
D: Oxi
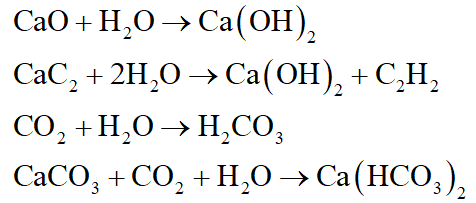
Câu 12:
Cho các chất Al2O3, Al(NO3)3, NaAlO2, Al2(SO4)3, Al(OH)3, Al. Hãy lựa chọn và sắp xếp các chất trên thành một dãy chuyển hóa (theo sơ đồ thẳn). Viết phương trình phản ứng minh họa (ghi rõ điều kiện nếu có).
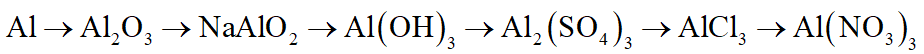
Các phương trình phản ứng:
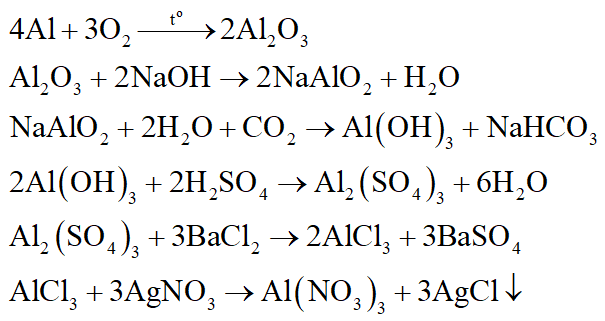
Câu 13:
Hỗn hợp X gồm M và R2O, trong đó M là kim loại thuộc nhóm IIA và R là kim loại kiềm. Cho m gam hỗn hợp X tan hết vào 400ml dung dịch HCl 2M (dư), thu được dung dịch Y chứa 38 gam các chất tan có cùng nồng độ mol.
a. Viết các phương trình phản ứng.
b. Xác định kim loại M và R.
Các phương trình phản ứng:
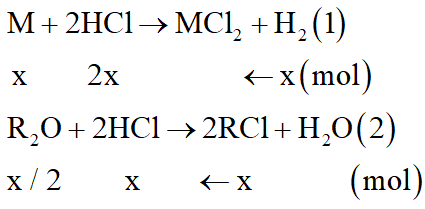
Dung dịch Y gồm MCl2, RCl và HCl dư
Các chất tan có cùng nồng độ mol
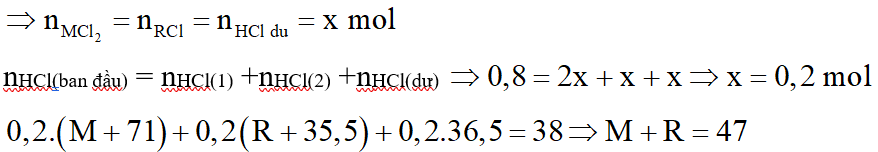
Vậy M = 24 (mg); R = 23 (Na) hoặc M = 40 (Ca); R = 7 (Li)
Câu 14:
Cho m gam Al2O3 tác dụng với dung dịch HCl dư thu được dung dịch X chứa 2 chất tan có cùng nồng độ mol. Rót từ từ dung dịch NaOH vào dung dịch X, đồ thị biến thiên số mol kết tủa theo số mol NaOH như sau:
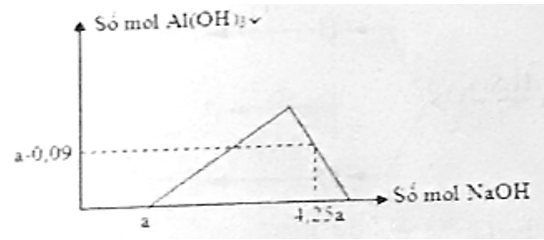
Viết các phương trình phản ứng, tính giá trị của m.
Al2O3 tác dụng với dung dịch HCl:
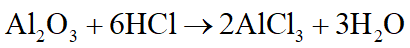
Dung dịch X gồm hai chất tan là AlCl3; HCl dư
Nhỏ từ từ dung dịch NaOH vào dung dịch X:
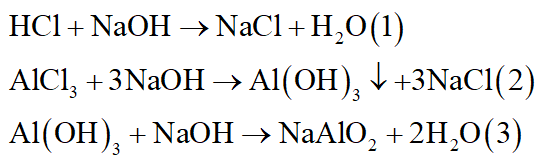
Tại thời điểm a mol NaOH, khi đó chỉ xảy ra
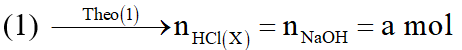
Các chất tan trong X cùng nồng độ mol
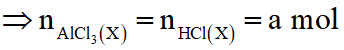
Xét tại thời điểm 4,25a mol NaOH:
Xảy ra cả (1), (2) và (3)
Sơ đồ phản ứng:
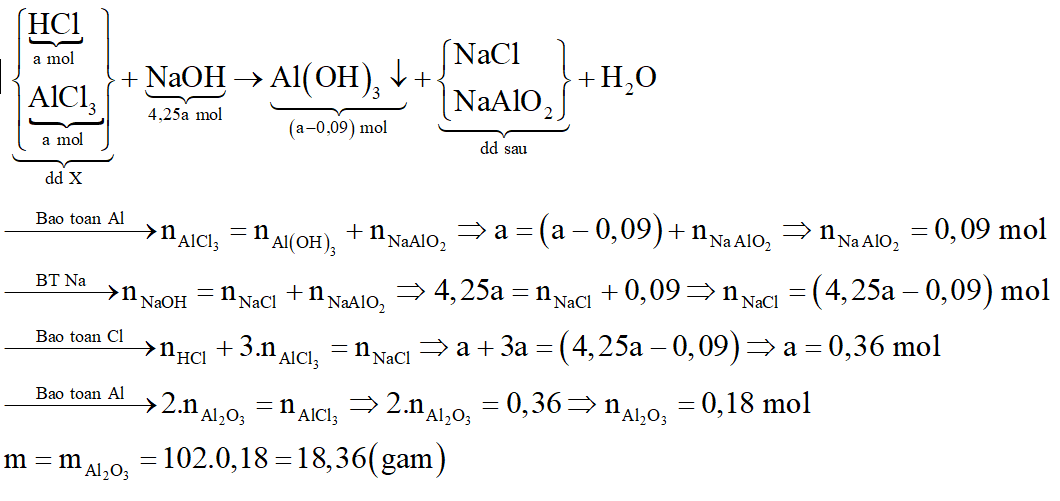
Câu 15:
Hỗn hợp A gồm ankin X, anken Y và hidrocacbon Z, đốt cháy hoàn toàn m gam A thu được 20,16 lít CO2 (đktc) và 16,2 gam H2O. Dẫn m gam A đi qua bình đựng dung dịch brom dư thấy có 0,4 mol Br2 phản ứng. Khí thoát ra khỏi bình brom đem đốt cháy hoàn toàn thu được 13,2 gam CO2 và 7,2 gam H2O. Xác định công thức phân tử của X, Y, Z, tính % thể tích của mỗi chất trong A.
Xét giai đoạn đốt cháy A:
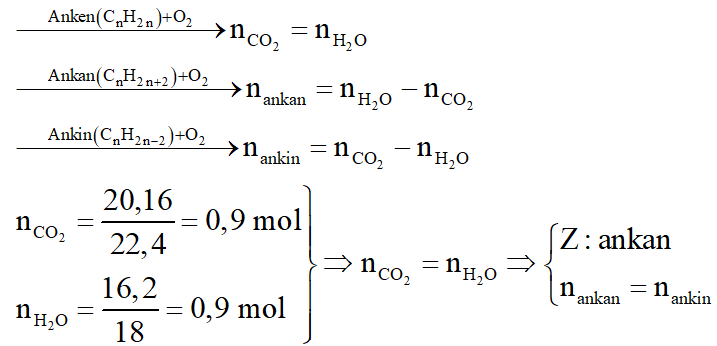
Khí thoát ra khỏi bình Br2 dư là X
Xét giai đoạn đốt Z:
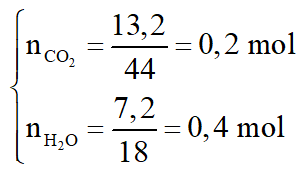
Sơ đồ phản ứng:
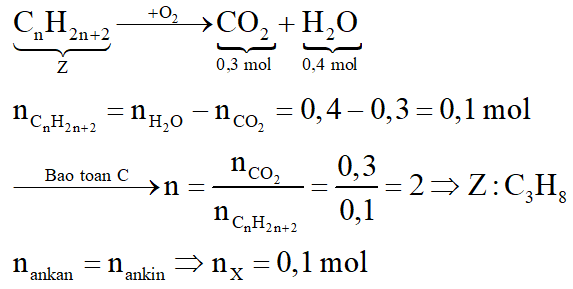
Xét giai đoạn A tác dụng với dung dịch brom:
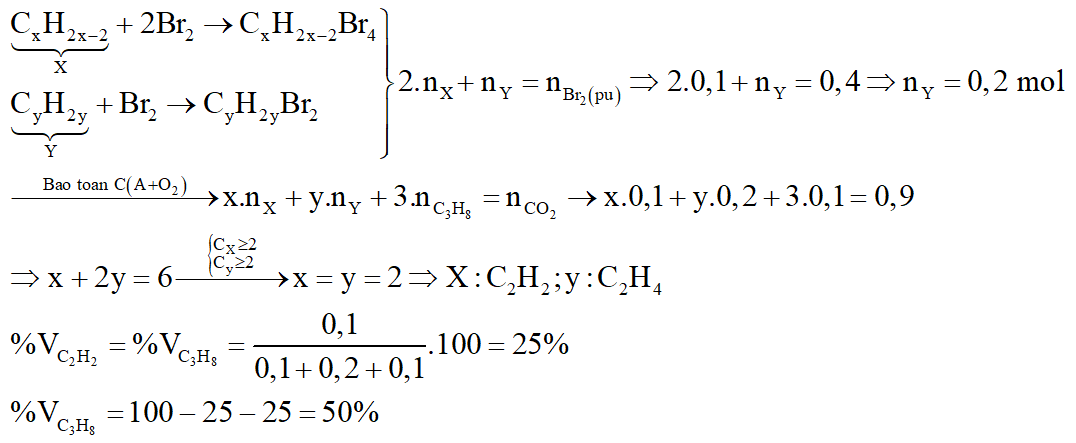
Câu 16:
Cho a gam hỗn hợp A gồm Fe2O3, Fe3O4, Cu vào dung dịch HCl dư thấy có 2 mol axit phản ứng, còn lại 0,264a gam chất rắn không tan. Mặt khác khử hoàn toàn a gam hỗn hợp A bằng H2 dư nung nóng, thu được 84 gam chất rắn.
a. Viết các phương trình phản ứng.
b. Tính % khối lượng Cu trong hỗn hợp A.
a. Đặt hỗn hợp là FeO, Fe2O3 số mol x, y
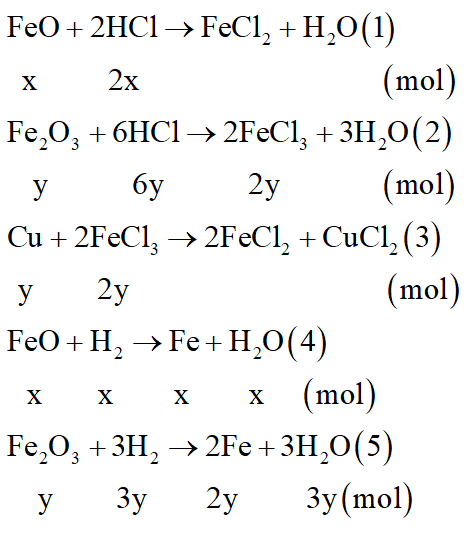
b. Theo (1), (2) và (4), (5)
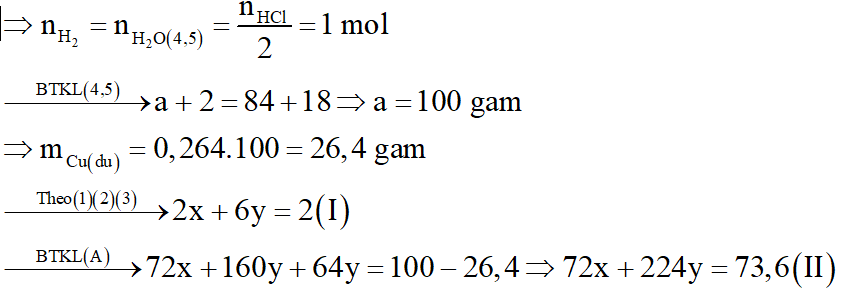
Tổ hợp (I) và (II) suy ra x = 0,4 mol; y = 0,2 mol