Đề kiểm tra học kì 1 chuyên đề Hóa 9 có đáp án_ đề 3
-
750 lượt thi
-
7 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Phương trình hóa học nào sau đây không đúng?
Đáp án C
Dung dịch NaCl không phản ứng với dung dịch H2SO4.
Câu 2:
Ngâm một lá Zn dư vào 200 ml dung dịch AgNO3 1M. Khi phản ứng kết thúc khối lượng Ag thu được là:
Đáp án D
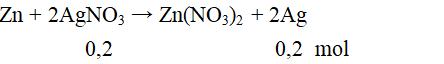
mAg = 0,2.108 = 21,6 gam.
Câu 3:
Có các chất đựng riêng biệt trong mỗi ống nghiệm sau đây: Al, Fe, CuO, CO2, FeSO4, H2SO4. Lần lượt cho dung dịch NaOH vào mỗi ống nghiệm trên. Dung dịch NaOH phản ứng với:
Đáp án A
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
CO2 + 2NaOH → Na2CO3 + 2H2O
FeSO4 + 2NaOH → Fe(OH)2 + Na2SO4
H2SO4 + 2NaOH → Na2SO4 + 2H2O
Câu 4:
Kim loại X có những tính chất hóa học sau:
- Phản ứng với oxit khi nung nóng.
- Phản ứng với dung dịch AgNO3.
- Phản ứng với dung dịch H2SO4 loãng giải phóng khí H2 và muối của kim loại hóa trị II. Kim loại X là:
Đáp án B
3Fe + 2O2 → Fe3O4
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe + H2SO4 → FeSO4 + H2
Câu 5:
Viết phương trình hóa học hoàn thành chuỗi biến hóa sau, ghi rõ điều kiện (nếu có)
Al -1→ Fe -2→ FeCl3 -3→ Fe(OH)3 -4→ Fe2O3
(1) 2Al + 3FeCl2 → 2AlCl3 + 3Fe
(2) 2Fe + 3Cl2 → 2FeCl3
(3) FeCl3 + 3KOH → Fe(OH)3 + 3KCl
(4) 2Fe(OH)3 → Fe2O3 + 3H2O
Câu 6:
Bằng phương pháp hóa học nhận biết các dung dịch sau: NaOH, H2SO4, Na2SO4, HCl. Viết phương trình hóa học (nếu có).
- Nhúng quỳ tím vào 4 mẫu thử:
+ 2 mẫu làm quỳ chuyển đỏ là H2SO4 và HCl
+ Mẫu làm quỳ chuyển xanh là NaOH
+ Mẫu không làm quỳ chuyển màu là là Na2SO4
- Nhỏ dd BaCl2 lần lượt vào 2 mẫu H2SO4 và HCl
+ Mẫu có kết tủa trắng là H2SO4
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
+ Mẫu còn lại là HCl
Câu 7:
Cho m gam hỗn hợp X gồm Fe và Cu vào dung dịch H2SO4 loãng, dư thu được 4,48 lít khí (đktc) và thấy còn 8,8 gam chất rắn không tan. Lấy phần chất rắn không tan ra thu được 250 ml dung dịch Y.
a. Xác định phần trăm về khối lượng các chất trong X.
b. Dung dịch Y tác dụng vừa đủ với BaCl2 thu được 69,9 gam kết tủa. Tính nồng độ mol các chất trong Y.
c. Nếu cho 12 gam X vào 300 ml dung dịch AgNO3 0,8M. Sau một thời gian thu được 28 gam chất rắn Z. Tính khối lượng của Ag có trong Z?
- Theo giả thiết ta có:
nH2 = 4,48/22,4 = 0,2 mol
- Phương trình hóa học: Fe + H2SO4 → FeSO4 + H2 (1)
Theo PTHH (1) ta có: nFe = nH2 = 0,2 mol
⇒ mFe = 0,2.56 ⇒ mFe = 11,2 (gam)
Suy ra, giá trị m là: m = 11,2 + 8,8 ⇒ m = 20 (gam)
a. Vậy thành phần phần trăm về khối lượng các chất trong X là:
%mFe = (11.2/20).100 = 56%
và %mCu = 100 - 56 = 44%
b. Theo bài ra dung dịch Y gồm FeSO4 và H2SO4 dư
Phương trình hóa học:
BaCl2 + FeSO4 → BaSO4 + FeCl2 (2)
BaCl2 + H2SO4 → BaSO4 + 2HCl (3)
Theo giả thiết, ta có:
nBaSO4 = 69,9/233 ⇒ nBaSO4 = 0,3 mol
Khi đó theo PTHH (1), (2), (3) ta có:
nFeSO4(Y) = 0,2 mol và nH2SO4(Y) = 0,1 mol
