Đề kiểm tra học kì 1 chuyên đề Hóa 9 có đáp án_ đề 5
-
753 lượt thi
-
11 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Ngâm hỗn hợp gồm các kim loại Al, Cu, Fe trong dung dịch AgNO3 (dư). Người ta thu được
Đáp án B
Al, Cu, Fe hoạt động mạnh hơn Ag đẩy được Ag ra khỏi dung dịch AgNO3.
Do AgNO3 dư nên Al, Cu, Fe tan hết. Chỉ thu được Ag.
Câu 2:
Công thức oxit cao nhất của 3 nguyên tố P, S, Cl là
Đáp án D
Công thức oxit cao nhất của 3 nguyên tố P, S, Cl là P2O5, SO3, Cl2O7.
Câu 3:
Đáp án C
Fe + H2SO4 → FeSO4 + H2
Câu 4:
Có các chất: brom, iot, clo, nito, oxi. Phi kim ở trang thái khí, khi ẩm có tính tẩy màu là
Đáp án C
Các chất: brom, iot, clo, nito, oxi.
Chỉ có clo là phi kim ở trạng thái khí, khi ẩm có tính tẩy màu.
Câu 5:
Kim loại nào sau đây tan được trong dung dịch NaOH?
Đáp án D
Câu 6:
Một quá trình không sinh ra khí CO2 là
Đáp án D
Phương trình hóa học của sự tôi vôi: CaO + H2O → Ca(OH)2.
Không sinh ra khí CO2.
Câu 7:
Khi cho KMnO4, MnO2 (số mol bằng nhau) lần lượt tác dụng hết với dung dịch HCl thu được khí clo có thể tích tương ứng là V1 và V2 (đktc). Biểu thức liên hệ giữa V1 và V2 là
Đáp án A
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O (1)
MnO2 + 4HCl to→ MnCl2 + Cl2 + 2H2O (2)
Tỉ lệ số mol Cl2 tạo ra ở phương trình (1) so với phương trình (2) là 2,5: 1 khi số mol KMnO4, MnO2 bằng nhau.
Câu 8:
Cho 1,008 m3 (đktc) hỗn hợp khí Co và H2 khử hoàn toàn Fe2O3 ở nhiệt độ thích hợp. Khối lượng sắt thu được sẽ là (Fe=56)
Đáp án D
Đổi 1,008 m3 = 1008 dm3 =1008 lít.
3CO + Fe2O3 to→ 2Fe + 3CO2 (1)
3H2 + Fe2O3 to→ 2Fe + 3H2O (2)
Theo phương trình (1), (2):
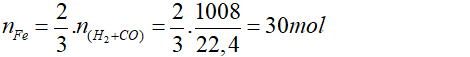
Khối lượng sắt thu được = 30 x 56 = 1680 gam hay 1,68kg.
Câu 9:
Có 4 lọ đựng 4 khí riêng biệt: oxi, hidro, clo và cacbon đioxit. Hãy nhận biết mỗi khí.
Đánh số thứ tự từng lọ chứa khí.
Dẫn lần lượt từng khí vào ống nghiệm đựng dung dịch nước vôi trong, khí làm đục dung dịch nước vôi là khí CO2.
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Dẫn các khí còn lại qua mẩu giấy màu ẩm, khí nào làm mất màu giấy là khí Clo.
Cho que đóm còn tàn đỏ vào lọ đựng hai khí còn lại, Khí làm que đóm bùng cháy là khí oxi.
Khí còn lại làm que đóm tắt là hiđro.
Câu 10:
Viết phương trình hóa học biểu diễn những chuyển đổi hóa học sau:
Fe2O3 (1)→ Fe (2)→ FeCl3 (3)→ Fe(OH)3 (4)→ Fe(NO3)3.
3CO + Fe2O3 to→ 2Fe + 3CO2
2Fe + 3Cl2 to→ 2FeCl3
FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
Fe(OH)3 + 3HNO3 → Fe(NO3)3 + 3H2O
Câu 11:
Nguyên tố R có công thức oxit là RO3. Trong RO3 oxi chiếm 60% về khối lượng.
a) Xác định tên nguyên tố R.
b) Cho biết tính chất hóa học cơ bản của R.
Viết phương trình hóa học để minh họa (O=16, S=32, Fe=56, Se=79).
% về khối lượng O = 60%
Ta có: 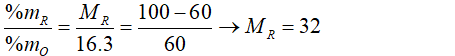
→ R là lưu huỳnh.
Lưu huỳnh là một phi kim hoạt động trung bình.
Tác dụng với oxi tạo oxit axit. Ví dụ:
S + O2 → SO2
Tác dụng với kim loại cho muối. Ví dụ:
Fe + S → FeS
Tác dụng với H2. Ví dụ:
H2 + S → H2S.
