Bộ đề kiểm tra định kì học kì 2 Hóa 9 có đáp án (Mới nhất) (Đề 31)
-
5103 lượt thi
-
22 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Thể tích không khí (chứa 20% thể tích oxi) ở đktc cần dùng để đốt cháy hết 3,2 gam khí metan là
Đáp án đúng là: C
Theo phương trình, ta có:
Câu 2:
Phát biểu đúng là:
Đáp án đúng là: C
Phương trình phản ứng este hóa giữa ancol etylic và axit axetic là:
Câu 3:
Phương trình phản ứng viết không đúng là:
Đáp án đúng là: A
Vì khi sắt tác dụng với khí clo sẽ tạo ra sắt (III) clorua.
Câu 4:
Trong phân tử etilen giữa hai nguyên tử cacbon có
Đáp án đúng là: B
Vì công thức cấu tạo của etilen là: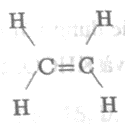
Ta thấy trong phân tử etilen có 1 liên kết đôi C=C.
Câu 6:
Cho 15 gam dung dịch CH3COOH tác dụng với 15 gam dung dịch KOH. Sai khi phản ứng kết thúc dung dịch chứa các chất tan là
Đáp án đúng là: A
Phương trình phản ứng:
Xét tỉ lệ:
Vậy CH3COOH phản ứng hết và KOH còn dư.
Vậy dung dịch sau phản ứng chứa các chất tan là CH3COOK và KOH.
Câu 7:
Khí oxi có lẫn tạp chất là khí clo, để loại bỏ tạp chất người ta dùng
Đáp án đúng là: C
Dẫn hỗn hợp khí qua dung dịch NaOH, khi đó chỉ có khí clo tác dụng với dung dịch NaOH tạo ra nước Javen. Khí oxi không phản ứng và thoát ra nên ta thu được oxi tinh khiết.
Phương trình phản ứng:
Câu 8:
Đốt cháy hoàn toàn 9,2 gam rượu etylic nguyên chất trong oxi (dư) thu được m gam CO2 và n gam H2O. Giá trị của m và n lần lượt là
Đáp án đúng là: B
Phương trình phản ứng cháy của C2H5OH là:
Theo phương trình ta có:
Câu 9:
Cặp chất có thể tác dụng được với nhau là
Đáp án đúng là: A
Đáp án B, C, D sai. Vì các cặp muối đó không thể tác dụng với nhau để tạo ra sản phẩm là chất không tan hoặc chất khí. Còn HCl và KHCO3 tác dụng được với nhau tạo ra khí CO2.
Câu 10:
Chất khi phản ứng với nước sinh ra khí axetilen là
Đáp án đúng là: B
Phương trình điều chế axetilen từ nước và canxi cacbua.
Câu 11:
Cho các phát biểu sau:
(a) Rượu etylic là chất lỏng, không màu, nặng hơn nước.
(b) Na có thể tác dụng với C2H5OH và CH3COOH.
(c) NaOH có tác dụng với C2H5OH.
(d) Axit axetic bị thủy phân khi đun nóng.
(e) Etyl axetat là chất lỏng, mùi thơm, ít tan trong nước.
Số phát biểu đúng là
Đáp án đúng là: B
(a) Sai. Vì nên rượu etylic nhẹ hơn nước.
(b) Đúng.
(c) Sai. Vì NaOH chỉ tác dụng được với C2H5OH.
(d) Sai. Vì axit axetic không bị thủy phân.
(e) Đúng.
Vậy có 2 phát biểu đúng.
Câu 12:
Phân tử khối của tinh bột khoảng 340200 (đvc). Số mắt xíc –C6H10O5− trong phân tử tinh bột là
Đáp án đúng là: D
Phân tử khối của tinh bột là:
Vậy số mắt xích –C6H10O5− trong phân tử tinh bột là 2100 mắt xích.
Câu 13:
Dẫn 4,5 lít hỗn hợp khí (ở đktc) gồm CH4 và C2H4 có tỉ lệ thể tích là 3 : 2 qua 20 gam dung dịch brom. Khối lượng dung dịch brom còn dư là
Đáp án đúng là: B
CH4 và C2H4 có tỉ lệ thể tích là 3 : 2 cũng chính là tỉ lệ về số mol.
Trong hỗn hợp khí chỉ có C2H4 tác dụng với dung dịch brom.
Vì dung dịch brom còn dư nên số mol brom đã phản ứng là:
Vậy khối lượng dung dịch brom còn dư là 4 gam.
Câu 14:
Khi đốt khí H2 với O2 sẽ gây nổ. Hỗn hợp nổ mạnh nhất khi tỉ lệ thể tích giữa H2 và O2 là
Đáp án đúng là: A
Câu 15:
Xenlulozơ không được ứng dụng để:
Đáp án đúng là: D
Vì sản xuất đường glucozơ là ứng dụng của tinh bột.
Câu 16:
Pentan là một hidrocacbon có tính chất tương tự metan và có công thức phân tử là C5H12.
Viết công thức cấu tạo mạch thẳng của pentan.
Công thức cấu tạo mạch thẳng của pentan:
CH3 – CH2 – CH2 – CH2 – CH3.
Câu 17:
Pentan là một hidrocacbon có tính chất tương tự metan và có công thức phân tử là C5H12.
Phương trình phản ứng đốt cháy pentan:
Câu 18:
Pentan là một hidrocacbon có tính chất tương tự metan và có công thức phân tử là C5H12.
Viết phương trình phản ứng pentan thế với clo tạo ta C5H11Cl.
Phương trình phản ứng pentan thế với clo tạo ra C5H11Cl:
Câu 19:
Không được dùng thêm thuốc thử nào khác, hãy nhận biết các dung dịch bằng phương pháp hóa học: Na2CO3, HCl, BaCl2.
Trích mẫu thử cho vào các ống nghiệm và đánh số thứ tự tương ứng (1), (2), (3).
Lần lượt cho một mẫu thử tác dụng với hai mẫu thử còn lại. Sau 6 lượt thí nghiệm ta có kết quả như bảng sau:
|
|
Na2CO3 |
HCl |
BaCl2 |
|
Na2CO3 |
|
|
Kết tủa trắng |
|
HCl |
|
|
Không phản ứng |
|
BaCl2 |
Kết tủa trắng |
Không phản ứng |
|
Dựa vào bảng trên, ta thấy ở thí nghiệm nào tạo khí CO2 và có tạo kết tủa BaCO3 trắng thì chứng tỏ chất đó là Na2CO3, mẫu thử chỉ tạo khí CO2 là HCl, mẫu thử nào chỉ tạo kết tủa BaCO3 trắng là BaCl2.
Phương trình phản ứng:
Câu 20:
Người ta lên men 1,62 kg tinh bột để điều chế rượu etylic. Tính khối lượng rượu etylic thu được biết hiệu suất của quá trình là 65%.
Sơ đồ phản ứng của quá trình lên men tinh bột để tạo thành rượu etylic:
Ta có số mol của tinh bột là:
Theo sơ đồ phản ứng ta có:
Mà hiệu suất của quá trình là 65% nên khối lượng rượu etylic thực tế thu được là:
Câu 21:
. Cho một hỗn hợp A gồm CH3COOH và C2H5OH chia thành 3 phần bằng nhau:
- Phần I tác dụng với natri dư thu được 11,2 lít khí (ở đktc).
- Phần II tác dụng với CaCO3 dư thu được 8,8 gam một chất khí.
Viết phương trình phản ứng xảy ra.
Các phương trình phản ứng:
Câu 22:
Cho một hỗn hợp A gồm CH3COOH và C2H5OH chia thành 3 phần bằng nhau:
- Phần I tác dụng với natri dư thu được 11,2 lít khí (ở đktc).
- Phần II tác dụng với CaCO3 dư thu được 8,8 gam một chất khí.
Tính khối lượng các chất trong hỗn hợp A.
Đun nóng phần III với axit H2SO4 đặc, tính khối lượng este tạo thành, biết hiệu suất phản ứng là 80%.
Số mol của khí H2 là:
Số mol của khí CO2 là:
Gọi x, y lần lượt là số mol của CH3COOH và C2H5OH có trong mỗi phần.
Từ phương trình phản ứng (1) và (2), ta có:
Từ phương trình phản ứng (3), ta có:
Từ (*) và (**) ta có hệ phương trình:
Số mol của CH3COOH và C2H5OH có trong mỗi phần lần lượt là 0,4 (mol) và 0,6 (mol)
Vì hỗn hợp được chia làm 3 phần bằng nhau nên số mol của CH3COOH và
C2H5OH có trong hỗn hợp là:
Khối lượng các chất trong hỗn hợp A là:
Phương trình phản ứng este hóa là:
Xét tỉ lệ:
Vậy CH3COOH phản ứng hết và C2H5OH còn dư nên số mol este và hiệu suất tính theo CH3COOH.
Theo phương trình phản ứng, ta có:
Mà hiệu suất của quá trình là 80% nên khối lượng este thực tế thu được là:
