Trắc nghiệm Hóa học 10 Bài 12: Liên kết hydrogen và tương tác van der waals có đáp án
Trắc nghiệm Hóa học 10 Bài 12: Liên kết hydrogen và tương tác van der waals có đáp án
-
255 lượt thi
-
15 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Liên kết hydrogen là
Đáp án đúng là: D
Liên kết hydrogen là liên kết yếu được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron riêng. Các nguyên tử có độ âm điện lớn thường gặp trong liên kết hydrogen là N, O, F.
Câu 2:
Những liên kết có lực liên kết yếu như
Đáp án đúng là: A
Các nguyên tử trong phân tử liên kết với nhau bằng những liên kết có lực liên kết mạnh như liên kết ion, liên kết cộng hóa trị. Các phân tử cũng có thể liên kết với nhau bằng những liên kết có lực yếu hơn như liên kết hydrogen, tương tác van der Waals.
Câu 3:
Liên kết hydrogen không được hình thành giữa hai phân tử nào sau đây?
Đáp án đúng là: C
Liên kết hydrogen là liên kết yếu được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron riêng. Các nguyên tử có độ âm điện lớn thường gặp trong liên kết hydrogen là N, O, F.
Nguyên tử H của phân tử H2O không tạo được liên kết hydrogen với nguyên tử C của CH4 vì nguyên tử C của phân tử CH4 không còn cặp electron riêng.
Câu 4:
Phát biểu nào sau đây không đúng?
Đáp án đúng là: C
Tính acid của một chất càng mạnh nếu chất đó càng dễ phân li thành ion H+.
Giữa các phân tử HF hay giữa phân tử HF và H2O có liên kết hydrogen, các liên kết này sẽ làm cho nguyên tử H bị giữ chặt hơn, khó tách ion H+ hơn so với HCl.
HF có tính acid yếu hơn rất nhiều so với HCl.
Câu 5:
Liên kết hydrogen và tương tác van der Waals làm
Đáp án đúng là: A
Liên kết hydrogen và tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất.
Câu 6:
Một loại liên kết rất yếu, hình thành do lực hút tĩnh điện giữa các cực trái dấu của phân tử, gọi là
Đáp án đúng là: C
Tương tác van der Waals là một loại liên kết rất yếu, hình thành do lực hút tĩnh điện giữa các cực trái dấu của phân tử.
Câu 7:
Phân tử nào sau đây không có cực?
Đáp án đúng là: D
Công thức cấu tạo của CO2: O=C=O.
Phân tử CO2 không có cực mặc dù liên kết C=O trong phân tử là liên kết cộng hóa trị có cực. Lí do bởi phân tử này có dạng thẳng, hai liên kết C=O lại có cực ngược chiều nhau nên triệt tiêu lẫn nhau khi xét cho cả phân tử.
Câu 8:
Trong dãy HX, các acid HCl, HBr, HI là axit mạnh nhưng HF là axit yếu. Đó là do
Đáp án đúng là: B
Do trong các phân tử HF có liên kết hydrogen làm giảm tính acid của HF nên HF là axit yếu.
Sơ đồ liên kết hydrogen giữa các phân tử hydrogen fluoride: …F-H…F-H…
Câu 9:
Nhiệt độ nóng chảy và nhiệt độ sôi của chất phụ thuộc chính vào yếu tố nào?
Đáp án đúng là: A
Nhiệt độ nóng chảy và nhiệt độ sôi của chất phụ thuộc chính vào hai yếu tố: khối lượng phân tử và liên kết giữa các phân tử.
Câu 10:
Số lượng liên kết giữa các phân tử càng nhiều, lực liên kết càng mạnh thì
B. nhiệt độ nóng chảy, nhiệt độ sôi của chất đó càng ổn định.
Đáp án đúng là: C
Số lượng liên kết giữa các phân tử càng nhiều, lực liên kết càng mạnh thì càng cần nhiều năng lượng để phá vỡ liên kết giữa chúng. Khi đó, nhiệt độ nóng chảy, nhiệt độ sôi của chất đó càng cao.
Câu 11:
Tại áp suất 1 bar, nước có nhiệt độ nóng chảy và nhiệt độ sôi tương ứng là 0oC và (xấp xỉ) 100oC, cao hơn so với nhiều chất có khối lượng phân tử lớn hơn nước. Tính chất này là do
Đáp án đúng là: C
Tại áp suất 1 bar, nước có nhiệt độ nóng chảy và nhiệt độ sôi tương ứng là 0oC và (xấp xỉ) 100oC, cao hơn so với nhiều chất có khối lượng phân tử lớn hơn nước. Tính chất này là do các phân tử nước liên kết khá chặt chẽ với nhau bởi các liên kết hydrogen.
Câu 12:
Cho các phát biểu sau:
(a) Quá trình chưng cất rượu, C2H5OH bay trước H2O mặc dù khối lượng phân tử C2H5OH lớn hơn khác nhiều khối lượng phân tử H2O.
(b) Khối lượng phân tử càng lớn thì nhiệt độ nóng chảy, nhiệt độ sôi càng thấp.
(c) Nhờ liên kết hydrogen, các phân tử nước có thể tập hợp với nhau, ngay cả ở thể hơi, thành một cụm phân tử.
(d) Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi các chất, nhưng ở mức độ ảnh hưởng mạnh hơn so với liên kết hydrogen.
Trong các phát biểu trên, số phát biểu đúng là
Đáp án đúng là: C
Phát biểu đúng: (a), (c).
Phát biểu (b) không đúng, vì: Khối lượng phân tử càng lớn thì nhiệt độ nóng chảy, nhiệt độ sôi càng cao.
Phát biểu (d) không đúng, vì: Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi các chất, nhưng ở mức độ ảnh hưởng yếu hơn so với liên kết hydrogen.
Câu 13:
Ảnh hưởng nào của liên kết hydrogen đến tính chất của các chất không đúng?
Đáp án đúng là: C
Liên kết hydrogen làm tăng độ tan của các chất.
Câu 14:
So sánh nhiệt độ sôi và nhiệt độ nóng chảy của các chất F2, Cl2, Br2, I2.
Đáp án đúng là: B
Theo dãy F2, Cl2, Br2, I2 thì kích thước và khối lượng tăng dần từ đầu đến cuối dãy nên lực van der Waals tăng dần do đó nhiệt độ sôi và nhiệt độ nóng chảy của các chất này tăng dần.
Câu 15:
Cho sơ đồ liên kết giữa hai phân tử acid CH3COOH:
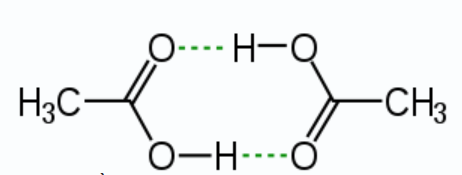
Trong sơ đồ trên, đường nét đứt đại diện cho
Đáp án đúng là: D
Liên kết hydrogen là liên kết yếu được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron riêng. Các nguyên tử có độ âm điện lớn thường gặp trong liên kết hydrogen là N, O, F.
Trong sơ đồ trên, đường nét đứt đại diện cho liên kết hydrogen.
