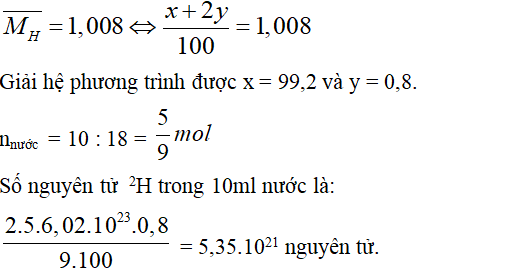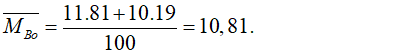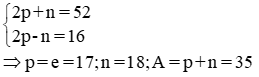Đề thi học kì 1 Hóa học 10 (Đề 4)
-
2010 lượt thi
-
19 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Các hạt cấu tạo nên hầu hết các nguyên tử là:
Chọn C
Các hạt cấu tạo nên hầu hết các nguyên tử là proton, nơtron và electron.
Câu 2:
Nguyên tố X thuộc chu kỳ 3, nhóm IVA trong bảng tuần hoàn. Cấu hình electron nguyên tử của X là:
Chọn B
X ở chu kỳ 3 nên X có 3 lớp electron; X thuộc nhóm IVA nên X có 4 electron lớp ngoài cùng. Cấu hình electron của nguyên tử X là:
Câu 4:
Nguyên tử của các nguyên tố thuộc chu kì 5 có số lớp electron là:
Chọn C
STT chu kỳ = số lớp electron.
Câu 6:
Hiđro có nguyên tử khối là 1,008. Hỏi có bao nhiêu nguyên tử của đồng vị trong 10 ml nước (biết trong nước chỉ có đồng vị và ; khối lượng riêng của nước là 1 g/ml).
Chọn B
Gọi % số nguyên tử của hai đồng vị và lần lượt là x và y
Ta có x + y = 100.
Ta lại có:
Câu 8:
Hòa tan hoàn toàn 0,3 gam hỗn hợp hai kim loại X và Y ở hai chu kì liên tiếp của nhóm IA vào nước thì thu được 0,224 lít khí hiđro ở đktc. Hai kim loại đó là (Biết Li = 7, Na = 23, K = 39, Rb = 85, Cs = 133).
Chọn A
Câu 9:
Trong tự nhiên Bo có 2 đồng vị là (81%) và (19%). Nguyên tử khối trung bình của Bo là:
Chọn D
Nguyên tử khối trung bình của Bo là:
Câu 11:
Chất nào sau đây chỉ chứa các liên kết cộng hóa trị?
Chọn D
tạo nên từ hai nguyên tố phi kim → phân tử chứa liên kết cộng hóa trị.
Câu 15:
Xác định vị trí của nguyên tố X, Q trong bảng tuần hoàn. Giải thích
Vị trí của X, Q trong bảng tuần hoàn: (1 điểm)
X: - Ô: 20 (vì Z = 20)
- Chu kì: 4 (vì có 4 lớp e)
- Nhóm: IIA (vì là nguyên tố s và có 2 electron lớp ngoài cùng)
Q: - Ô: 29 (vì Z = 29)
- Chu kì: 4 (vì có 4 lớp e)
- Nhóm: IB (vì là nguyên tố d và có 1 electron hoá trị)
Câu 16:
Nêu tính chất hóa học cơ bản của nguyên tố X, Y. Giải thích
Tính chất: (1 điểm)
* X - là kim loại vì có 2e lớp ngoài cùng.
- Hóa trị cao nhất với oxi là II, Hoá trị trong hợp chất khí với hiđro: không có vì là kim loại
- Công thức oxit cao nhất XO ⇒ là oxit bazo; CT hiđroxit tương ứng
⇒ là bazo
* Y - là phi kim vì có 5e lớp ngoài cùng.
- Hóa trị cao nhất với oxi là V, Hoá trị trong hợp chất khí với hiđro là III
- Công thức oxit cao nhất ⇒ là oxit axit; CT hiđroxit tương ứng
⇒ là axit
- CT hợp chất khí với hiđro là