125 câu trắc nghiệm Oxi - Lưu huỳnh nâng cao (P4)
-
13224 lượt thi
-
7 câu hỏi
-
25 phút
Danh sách câu hỏi
Câu 1:
Hình vẽ mô tả điều chế khí SO2 trong phòng thí nghiệm:
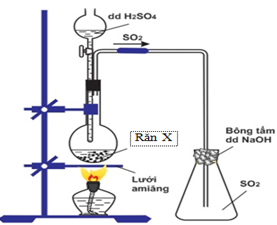
Điều nào sau đây là sai ?
Đáp án C.
Câu 2:
Hòa tan hoàn toàn 5,5 gam hỗn hợp gồm Al và Fe vào lượng dư dung dịch H2SO4 loãng, thu được 4,48 lít H2 (đktc). Thành phần phần trăm khối lượng của Fe trong hỗn hợp đầu là:
Đáp án A
=> mhh= mFe + mAl
Bảo toàn electron:
Câu 3:
Cho các phát biểu sau:
(a) Sục khí SO2 vào dung dịch NaOH dư tạo ra muối trung hòa Na2SO3.
(b) SO2 vừa có tính khử, vừa có tính oxi hóa.
(c) Khí SO2 là một trong những nguyên nhân chính gây ra mưa axit.
(d) Khí SO2 có màu vàng lục và rất độc.
Số phát biểu đúng là:
Đáp án A.
Các phát biểu đúng a,b,c
Câu 4:
Nung hỗn hợp bột kim loại gồm 11,2 gam Fe và 6,5 gam Zn với một lượng S dư (trong điều kiện không có không khí), thu được hỗn hợp rắn X. Hòa tan hoàn toàn X trong dung dịch HCl dư thu được khí Y. Hấp thụ toàn bộ Y vào dung dịch NaOH 1M. Thể tích dung dịch NaOH 1M tối thiểu để hấp thụ hết khí Y là:
Đáp án B.
nFe = 0,2 mol; nZn = 0,1 mol
NaOH + H2S→NaHS + H2O
Câu 5:
Cho 25,5 gam hỗn hợp X gồm CuO và Al2O3 tan hoàn toàn trong dung dịch H2SO4 loãng, thu được dung dịch chứa 57,9 gam muối. Phần trăm khối lượng của Al2O3 trong X là:
Đáp án D.
Câu 6:
Dẫn 3,36 lít khí H2S (đktc) vào 250ml dung dịch KOH 2M, sau khi phản ứng hoàn toàn thu được dung dịch X. Cô cạn dung dịch X thu được m gam rắn khan. Giá trị của m là:
Đáp án D.
Tạo K2S và KOH còn dư
H2S + 2KOH → K2S + 2H2O
0,15 0,3 0,15
