Kim loại kiềm thổ và hợp chất
-
339 lượt thi
-
30 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Nhận xét nào sau đây là không đúng ?
Trả lời:
Nhận xét không đúng là : Be, Mg, Ca, Sr, Ba đều phản ứng với nước ở nhiệt độ thường nên gọi là kim loại kiềm thổ.
Vì Be không phản ứng với nước, còn Mg phản ứng với nước ở nhiệt độ cao.
Đáp án cần chọn là: D
Câu 2:
Câu nào không đúng khi nói về canxi ?
Trả lời:
Câu không đúng là: Nguyên tử Ca bị khử khi Ca tác dụng với O2.
PTHH: 2Ca + O2 → 2CaO =>Ca bị oxi hóa khi tác dụng với O2.
Đáp án cần chọn là: C
Câu 3:
Mô tả nào sau đây không đúng về ứng dụng của Mg ?
Trả lời:
Mô tả không đúng là B. Mg dùng chế tạo dây dẫn điện
Đáp án cần chọn là: B
Câu 4:
So với nguyên tử canxi, nguyên tử kali có
Trả lời:
So với nguyên tử canxi, nguyên tử K có bán kính lớn hơn và độ âm điện nhỏ hơn
Đáp án cần chọn là: B
Câu 5:
Hãy chọn phản ứng giải thích sự xâm thực của nước mưa với đá vôi và sự tạo thành thạch nhũ trong các hang động?
Trả lời:
Phản ứng giải thích sự xâm thực của nước mưa với đá vôi và sự tạo thành thạch nhũ trong các hang động là quá trình phản ứng thuận nghịch:
CaCO3 + H2O + CO2 ⇆ Ca(HCO3)2 xảy ra trong 1 thời gian rất lâu
Đáp án cần chọn là: D
Câu 6:
Chất nào sau đây không bị nhiệt phân?
Trả lời:
Mg(OH)2 \[\mathop \to \limits^{t^\circ } \]MgO + H2O
CaCO3 \[\mathop \to \limits^{t^\circ } \]CaO + CO2
Ca(HCO3)2 \[\mathop \to \limits^{t^\circ } \] CaCO3 + CO2 + H2O
=>Chất không bị nhiệt phân là Ca(OH)2
Đáp án cần chọn là: B
Câu 7:
Để nhận biết Na, Ca, Al ta dùng lần lượt các chất sau:
Trả lời:
| Na | Ca | Al |
H2O | Tan, tạo khí | Tan, tạo khí | Không tan |
Na2CO3 | Không hiện tượng | Kết tủa trắng |
|
Đáp án cần chọn là: A
Câu 8:
Cho các dung dịch sau: Ba(OH)2, NaHSO4, K2CO3, Ba(HCO3)2. Đổ lần lượt các dung dịch vào nhau. Số phản ứng xảy ra là
Trả lời:
+) Ba(OH)2 phản ứng với NaHSO4, K2CO3, Ba(HCO3)2
+) NaHSO4 phản ứng với K2CO3, Ba(HCO3)2
+) K2CO3 phản ứng với Ba(HCO3)2
=>có tất cả 6 phản ứng
Đáp án cần chọn là: B
Câu 9:
Cho biết phản ứng nào không xảy ra ở nhiệt độ thường ?
Trả lời:
Phản ứng không xảy ra ở nhiệt độ thường là:
CaCl2 + NaHCO3 → CaCO3 + NaCl + HCl
Đáp án cần chọn là: D
Câu 10:
Chỉ dùng thêm thuốc thử nào dưới đây có thể nhận biết được 3 lọ mất nhãn chứa các dung dịch: H2SO4, BaCl2, Na2SO4 ?
Trả lời:
- dùng quỳ tím
| H2SO4 | BaCl2 | Na2SO4 |
Quỳ tím | Đỏ | Không đổi màu | Không đổi màu |
H2SO4 vừa nhận biết |
| Kết tủa trắng | Không hiện tượng |
- dùng bột kẽm
| H2SO4 | BaCl2 | Na2SO4 |
Zn | Xuất hiện bọt khí | Không hiện tượng | Không hiện tượng |
H2SO4 vừa nhận biết |
| Kết tủa trắng | Không hiện tượng |
- dùng Na2CO3
| H2SO4 | BaCl2 | Na2SO4 |
Na2CO3 | Xuất hiện khí | Kết tủa trắng | Không hiện tượng |
Đáp án cần chọn là: D
Câu 11:
Cho dãy các chất: KOH, Ca(NO3)2, SO2, SO3, NaHSO4, Na2SO3, K2SO4. Số chất trong dãy tạo thành kết tủa khi phản ứng với dung dịch BaCl2 là
Trả lời:
Các chất tạo kết tủa với dung dịch BaCl2 là: SO3, NaHSO4, Na2SO3, K2SO4
SO3 + H2O → H2SO4
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
BaCl2 + 2NaHSO4 → BaSO4↓ + 2HCl + Na2SO4
BaCl2 + Na2SO3 → 2NaCl + BaSO3↓
BaCl2 + K2SO4 → 2KCl + BaSO4↓
Đáp án cần chọn là: A
Câu 12:
Đun nóng đến khối lượng không đổi hỗn hợp X gồm Mg(OH)2, Ca(NO3)2, BaCl2 thu được hỗn hợp chất rắn Y. Thành phần của hỗn hợp Y là
Trả lời:
Đun nóng hỗn hợp X có 2 chất bị phân hủy
Mg(OH)2 \[\mathop \to \limits^{t^\circ } \]MgO + H2O
Ca(NO3)2 \[\mathop \to \limits^{t^\circ } \]Ca(NO2)2 + O2
BaCl2 không bị phân hủy
Đáp án cần chọn là: C
Câu 13:
Cho dd Ba(HCO3)2 lần lượt tác dụng với các dd sau: CaCl2, Ca(NO3)2, NaOH, NaHSO4, Ca(OH)2, H2SO4, HCl. Số phản ứng tạo ra kết tủa là
Trả lời:
Ba(HCO3)2 phản ứng với các chất sinh ra kết tủa là: NaOH, NaHSO4, Ca(OH)2, H2SO4
Ba(HCO3)2 + 2NaOH → BaCO3 ↓ + Na2CO3 + 2H2O
Ba(HCO3)2 + 2NaHSO4 → BaSO4 ↓ + Na2SO4 + 2CO2 + 2H2O
Ba(HCO3)2 + Ca(OH)2 → BaCO3 ↓ + CaCO3 ↓ + 2H2O
Ba(HCO3)2 + H2SO4 → BaSO4 ↓ + 2CO2 + 2H2O
Đáp án cần chọn là: B
Câu 14:
Cho sơ đồ biến hóa:
Ca → X → Y → Z → T → Ca.
Hãy chọn thứ tự đúng của các chất X, Y, Z, T là
Trả lời:
Sơ đồ biến hóa đúng là : Ca → CaO → CaCO3 → Ca(HCO3)2 → CaCl2 → Ca
PTHH: 2Ca + O2 → 2CaO
CaO + CO2 → CaCO3
CaCO3 + CO2 + H2O → Ca(HCO3)2
Ca(HCO3)2 + 2HCl → CaCl2 + 2CO2 + 2H2O
CaCl2 \[\mathop \to \limits^{dpnc} \]Ca + Cl2
Đáp án cần chọn là: B
Câu 15:
Từ hai muối X và Y thực hiện các phản ứng sau:
X → X1 + CO2
X1 + H2O → X2
X2 + Y → X + Y1 + H2O
X2 + 2Y → X + Y2 + H2O
Hai muối X và Y tương ướng là
Trả lời:
X phân hủy tạo CO2 =>X là CaCO3 hoặc BaCO3
=>X1 là oxit bazơ : MO =>X2 là bazơ M(OH)2
Ta thấy X2 + Y ->X =>Y phải là hợp chất cacbonat ( CO3 hoặc HCO3) mà X2 tác dụng với Y theo 2 tỉ lệ tạo 2 chất khác nhau
=>Y là NaHCO3
=>X là CaCO3
PTHH: Ca(OH)2 + NaHCO3 → CaCO3 + NaOH + H2O
Ca(OH)2 + 2NaHCO3 → CaCO3 + Na2CO3 + H2O
Đáp án cần chọn là: C
Câu 16:
Cho các sơ đồ chuyển hóa:
CaO + X → CaCl2;
CaCl2 + Y → Ca(NO3)2;
Ca(NO3)2 + Z → CaCO3.
Công thức của chất X, Y, Z lần lượt là
Trả lời:
PTHH:
CaO + 2HCl → CaCl2 + H2O
CaCl2 + 2AgNO3 → Ca(NO3)2 + 2AgCl↓
Ca(NO3)2 + (NH4)2CO3 → CaCO3 + 2NH4NO3
Loại A và D vì Cl2 không tác dụng với CaO
Loại C vì HNO3 không tác dụng với CaCl2
Đáp án cần chọn là: B
Câu 17:
Đốt môi sắt chứa kim loại M cháy ngoài không khí rồi đưa vào bình đựng khí CO2 như hình vẽ, thấy kim loại M vẫn tiếp tục cháy trong bình đựng CO2
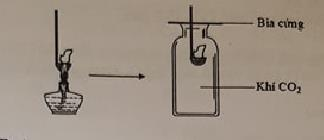
Kim loại M là
Trả lời:
Kim loại M là Mg vì 2Mg + O2 \[\mathop \to \limits^{t^\circ } \]2MgO
Mg + CO2 \[\mathop \to \limits^{t^\circ } \]MgO + C
Đáp án cần chọn là: D
Câu 18:
Hỗn hợp A gồm 2 kim loại M và M’ nằm ở 2 chu kì kế tiếp nhau. Lấy 3,1 gam hỗn hợp A hòa tan hết vào nước thu được 1,12 lít khí H2 (đktc). M và M’ là
Trả lời:
nH2 = 0,05 mol
Dựa vào các đáp án ta thấy hỗn hợp A gồm 2 kim loại kiềm
=>nKL = 2nH2 = 0,1 mol
\[{M_{KL}} = \frac{{3,1}}{{0,1}} = 31\]
=>2 kim loại là Na và K
Đáp án cần chọn là: B
Câu 19:
Hòa tan 11,5 gam kim loại kiềm R vào nước lấy dư được dung dịch D và 5,6 lít khí H2. Toàn bộ dung dịch D trung hòa vừa đủ V lít dung dịch H2SO4 0,5M và thu được m gam muối khan. Giá trị của V và m là
Trả lời:
\[{n_{{H_2}}} = 0,25mol\]
Ta có:
\[{n_{{H_2}S{O_4}}} = {n_{{H_2}}} = 0,25mol\]
\[ \to V = \frac{{0,25}}{{0,5}} = 0,5lit\]
mmuối khan = mkim loại + \[{m_{SO_4^{2 - }}}\]= 11,5 + 0,25.96 = 35,5g
Đáp án cần chọn là: A
Câu 20:
Hòa tan hoàn toàm m gam hỗn hợp Ba và một kim loại kiềm vào nước rồi pha loãng đến 1 lít dung dịch. Sau phản ứng thu được 1,12 lít khí H2 (đktc). Dung dịch thu được có pH bằng
Trả lời:
nH2 = 0,05 mol =>nOH- = 2nH2 = 0,1 mol
=>[OH-] = 0,1 / 1 = 0,1 M =>pOH = 1
=>pH = 13
Đáp án cần chọn là: C
Câu 21:
Cho m gam Na tan hết vào 500 ml dung dịch Ba(OH)2 0,04M được 500 ml dung dịch có pH = 13. Giá trị của m là :
Trả lời:
Gọi nNa = x mol =>nNaOH = x mol
\[ \Rightarrow \sum {n_{O{H^ - }}} = {n_{NaOH}} + 2{n_{Ba{{(OH)}_2}}} = X + 0,04mol\]
pH =13 =>pOH = 1 => [OH-] = 10-1 = 0,1M
=>(x + 0,04) / 0,5 = 0,1 =>x = 0,01
=>mNa = 0,23 gam
Đáp án cần chọn là: A
Câu 22:
Cho hỗn hợp gồm Na và Ba vào dung dịch chứa HCl 1M và H2SO4 0,6M. Sau khi kết thúc phản ứng thấy thoát ra 3,36 lít khí H2 (đktc) đồng thời thu được 13,98 gam kết tủa và dung dịch X có khối lượng giảm 0,1 gam so với dung dịch ban đầu. Cô cạn dung dịch X thu được m gam chất rắn. Giá trị của m là
Trả lời:
Đặt a và b là số mol của Na, Ba
=>a + 2b = 0,15.2 (1)
mdung dịch giảm = 23a + 137b – 13,98 – 0,15.2 = - 0,1 (2)
Từ (1) và (2) =>a = 0,14; b = 0,08
nBaSO4 = 0,06 mol =>Ba2+ còn dư 0,08 – 0,06 = 0,02 mol
=>nH2SO4 = 0,06 mol =>nHCl = 0,06.1/0,6 = 0,1
Dung dịch X chứa Ba2+ (0,02), Na+ (0,14 mol); Cl- (0,1 mol) và OH-
Bảo toàn điện tích =>nOH- = 0,08 mol
=>mrắn = 10,87 gam
Đáp án cần chọn là: A
Câu 23:
A là hỗn hợp 2 kim loại kiềm X và Y thuộc 2 chu kì kế tiếp. Nếu cho A tác dụng vừa đủ với dung dịch HCl thì thu được a gam 2 muối, còn nếu cho A tác dụng vừa đủ với dung dịch H2SO4 thì thu được 1,1807a gam hai muối. X và Y là
Trả lời:
Đặt công thức chung của hai kim loại kiềm là R, khối lượng mol trung bình là \[\overline R \]
Giả sử nR = 1 mol
+ nRCl = nR = 1 mol
=>mRCl = \[\overline R \]+35,5 = a (1)
+ nR2SO4 = 0,5.nR = 0,5 mol
=>0,5.(2.\[\overline R \]+ 96) = 1,1807a (2)
Từ (1) và (2) => \[\overline R \]= 33,67
=>X và Y là Na và K
Đáp án cần chọn là: B
Câu 24:
Hòa tan hết một lượng Na vào dung dịch HCl 10% thu được 46,88 gam dung dịch gồm NaCl và NaOH và 1,568 lít H2 (đktc). Nồng độ % NaCl trong dung dịch thu được là
Trả lời:
nH2 = 0,07 mol
Gọi nNaCl = x mol; nNaOH = y mol
Bảo toàn nguyên tử Na: nNa ban đầu = x + y mol
Bảo toàn e: nNa = 2nH2 =>x + y = 2.0,07 (1)
nHCl phản ứng = nNaCl = x mol
=>mdung dịch HCl = 36,5x.100 / 10 = 365x gam
=>mdd sau phản ứng = mNa + mdd HCl – mH2 = 23.(x + y) + 365x – 2.0,07 = 46,88 (2)
Từ (1) và (2) =>x = 0,12; y = 0,02 mol
\[ \Rightarrow C{\% _{NaCl}} = \frac{{0,12.58,5}}{{46,88}}.100\% = 14,97\% \]
Đáp án cần chọn là: A
Câu 25:
Cho m gam Na tan hết vào 300 ml dung dịch gồm (H2SO4 0,1M và HCl 1M) thu được 22,4 lít khí H2 (đktc). Khối lượng chất rắn thu được khi cô cạn là
Trả lời:
nH2SO4 = 0,03 mol; nHCl = 0,3 mol; nH2 = 1 mol
Ta thấy: nH+ = 0,03.2 + 0,3 = 0,36 mol < nH2
=>Na tan trong H+ và trong H2O tạo muối và bazơ
Ta có: nOH- = 2nH2 – nH+ = 2.1 – 0,36 = 1,64 mol
=>chất rắn thu được gồm Na2SO4 (0,03 mol); NaCl (0,3 mol); NaOH (1,64 mol)
=>mchất rắn = 87,41 gam
Đáp án cần chọn là: B
Câu 26:
Cho một lượng hỗn hợp X gồm Ba và Na vào 200 ml dung dịch Y gồm HCl 0,1M và CuCl2 0,1M. Sau phản ứng thu được 0,448 lít khí (đktc) và m gam kết tủa. Giá trị của m là
Trả lời:
nHCl = 0,2.0,1 = 0,02 mol; nCuCl2 = 0,2.0,1 = 0,02 mol
nH2 = 0,02 mol
Khi cho Na, Ba vào dung dịch chứa H+ thì H+ bị khử trước, hết H+ thì H2O mới bị khử
2H+ + 2e → H2
0,02 → 0,02 → 0,01
=>nH2 do khử H2O = 0,02 – 0,01 = 0,01 mol
nOH- = 2nH2 = 0,01.2 = 0,02 mol
Cu2+ + 2OH- → Cu(OH)2
0,01 0,02 0,01 (mol)
=>mkết tủa = 0,01.98 = 0,98 gam
Đáp án cần chọn là: C
Câu 27:
Cho hỗn hợp X gồm 0,2 mol Ba và 0,5 mol K tác dụng hết với 500 ml dung dịch Y gồm HCl 1,2M và CuSO4 0,4M, sau phản ứng thu được V lít khí H2 (đktc) và m gam kết tủa. Giá trị của V và m là
Trả lời:
nHCl = 0,6 mol; nCuSO4 = 0,2 mol
2K + 2HCl → 2KCl + H2
Ba + 2HCl → BaCl2 + H2
Ba + 2H2O → Ba(OH)2 + H2
Bảo toàn e: 2nBa + nK = 2nH2 =>nH2 = (0,2.2 + 0,5) / 2 = 0,45 mol
=>V = 10,08 lít
Kết tủa thu được gồm BaSO4 và Cu(OH)2
Ta thấy: nBaSO4 = nBa = nCuSO4 = 0,2 mol
Bảo toàn Ba: nBa(OH)2 = nBa ban đầu – nBaCl2 = 0,2 – 0,05 = 0,15 mol
Vì nBa(OH)2 = 0,15 mol < nCuSO4
= 0,2 mol =>số mol Cu(OH)2 tính theo Ba(OH)2 là 0,15 mol=>mkết tủa = mBaSO4 + mCuSO4 = 61,3 gam
Đáp án cần chọn là: C
Câu 28:
Hòa tan hoàn toàn m gam hỗn hợp X chứa Ba, Al, BaO, Al2O3 vào nước dư thu được 0,896 lít khí đktc và dung dịch Y. Hấp thụ hoàn toàn 1,2096 lít khí CO2 vào dung dịch Y thấy xuất hiện 4,302 gam kết tủa. Lọc kết tủa thu được dung dịch Z chỉ chứa một chất tan. Mặt khác nếu dẫn từ từ CO2 đến dư vào dung dịch Y thì thu được 3,12 gam kết tủa. Giá trị của m là
Trả lời:
Quy đổi X thành Ba: x mol; Al: y mol và O : z mol
Ba → Ba+2 +2e Al → Al+3 +3e
O + 2e → O-2
2H+ +2e → H2
→ 2x + 3y – 2z =2.0,04=0,08 (1)
Y +CO2 thì Ba(AlO2)2 + CO2 +3H2O → BaCO3 + 2Al(OH)3
Ba(OH)2 + CO2 → BaCO3 + H2O
BaCO3 + CO2 + H2O → Ba(HCO3)2
Nếu CO2 dư thì nkết tủa = nAl(OH)3 = 3,12 : 78 = 0,04 mol
→ nBa(AlO2)2 = 0,02 mol
Bảo toàn Al : y = 0,04 mol( = nAl(OH)3) (2)
Khi CO2 :
0,054 mol thì nAl(OH)3 = 0,04 mol
→ nBaCO3 = 0,006 mol < ½ nAl(OH)3
→ phản ứng tạo tối đa BaCO3 rồi tan
Bảo toàn C có :
nCO2 = nBaCO3 + 2nBa(HCO3)2
→ 0,054 = 0,006 + 2nBa(HCO3)2
→ nBa(HCO3)2 = 0,024 mol
Bảo toàn Ba có:
x = nBaCO3 + nBa(HCO3)2 = 0,006 + 0,024 =0,03 mol(3)
Từ (1) (2) và (3) → z = 0,05 mol
→ m = 5,99 g
Đáp án cần chọn là: D
Câu 29:
Cho m gam hỗn hợp gồm Na, Na2O, K2O vào H2O dư, thu được 50 ml dung dịch X và 0,02 mol H2. Cho 50 ml dung dịch HCl 3M vào X, thu được 100 ml dung dịch Y có pH = 1. Cô cạn Y thu được 9,15 gam chất rắn khan. Giá trị của m gần nhất với giá trị nào sau đây?
Trả lời:
Bước 1: Tính số mol các chất trong hỗn hợp
Quy đổi hỗn hợp thành Na (a), K (b), O (c).
- BTe: nNa + nK = 2nO + 2nH2 → a + b = 2c + 2.0,02 (1)
- nOH- = nNaOH + nKOH = a + b (mol)
→ nH+dư = nH+ (bđ) - nOH- → 0,1.10-1 = 0,05.3 - (a + b) (2)
- Chất rắn sau cô cạn gồm: NaCl (a) và KCl (b)
→ 58,5a + 74,5b = 9,15 (3)
Giải (1), (2), (3) được a = 0,08; b = 0,06; c = 0,05.
Bước 2: Tính giá trị của m hỗn hợp ban đầu
- mhh = 0,08.23 + 0,06.39 + 0,05.16 = 4,98 gam gần nhất với 5 gam.
Đáp án cần chọn là: C
Câu 30:
Hỗn hợp X gồm K, K2O, Ba, BaO. Lấy m gam X hòa tan vào H2O dư thu được 0,07 mol H2 và dung dịch Y. Hấp thụ hết 0,18 mol CO2 vào Y thu được 3,94 gam kết tủa và dung dịch Z. Nhỏ từ từ dung dịch NaOH 1M vào Z đến khi kết tủa lớn nhất thì cần ít nhất 30 ml dung dịch NaOH 1M. Giá trị của m gần nhất với giá trị nào sau đây?
Trả lời:
Bước 1: Xác định thành phần các chất trong Z.
- Do thêm NaOH vào vẫn thu được kết tủa nên dung dịch Z chứa Ba(HCO3)2 và KHCO3.
Bước 2: Tính nK (X), nBa (X), nO (X)
Coi hỗn hợp X gồm K, Ba, O
- Để kết tủa lớn nhất cần ít nhất NaOH thì xảy ra phản ứng:
Ba(HCO3)2 + NaOH → BaCO3 ↓ + NaHCO3 + H2O
0,03 0,03
- nCO2 = 0,18 mol; nBaCO3 = 0,02 mol; nBa(HCO3)2 = 0,03 mol
- Tính nK (X), nBa (X), nO (X):
+ Bảo toàn Ba: nBa (X) = nBaCO3 + nBa(HCO3)2 = 0,05 mol
+ Bảo toàn C: nCO2 = nBaCO3 + 2nBa(HCO3)2 + nKHCO3 ⟶ nKHCO3 = 0,1 mol ⟶ nK (X) = 0,1 mol
+ Bảo toàn e ⟶ nK + 2nBa = 2nO (X) + 2nH2 ⟶ nO (X) = 0,03 mol
Bước 3: Tính mX
- mX = 0,1.39 + 0,05.137 + 0,03.16 = 11,23 gam.
Đáp án cần chọn là: B
