- Đề số 1
- Đề số 2
- Đề số 3
- Đề số 4
- Đề số 5
- Đề số 6
- Đề số 7
- Đề số 8
- Đề số 9
- Đề số 10
- Đề số 11
- Đề số 12
- Đề số 13
- Đề số 14
- Đề số 15
- Đề số 16
- Đề số 17
- Đề số 18
- Đề số 19
- Đề số 20
- Đề số 21
- Đề số 22
- Đề số 23
- Đề số 24
- Đề số 25
- Đề số 26
- Đề số 27
- Đề số 28
- Đề số 29
- Đề số 30
- Đề số 31
- Đề số 32
- Đề số 33
- Đề số 34
- Đề số 35
- Đề số 36
Bộ đề kiểm tra định kì học kì 1 Hóa 9 có đáp án (Mới nhất) - Đề 33
-
5792 lượt thi
-
20 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Trường hợp nào sau đây có phản ứng tạo sản phẩm là kết tủa màu xanh?
Đáp án đúng là: D
Đồng (II) oxit là kết tủa màu xanh lam
Câu 3:
Chọn một hóa chất để phân biệt các dung dịch riêng biệt đựng trong các lọ mất nhãn sau: NaOH, H2SO4, HCl, Na2CO3
Đáp án đúng là: D
Cho BaCl2 vào 4 dung dịch trên, có 2 dung dịch cho kết tủa là H2SO4 và Na2CO3
Lấy một trong các dung dịch còn lại lần lượt tác dụng với 2 kết tủa nêu trên, nếu kết tủa tan là BaCO3 và dung dịch đã lấy là HCl. Nếu kết tủa không tan là BaSO4 và dung dịch đã lấy là NaOH
Câu 4:
Tính chất đặc biệt của H2SO4 đặc, nóng là tác dụng được với các chất trong dãy nào sau đây mà H2SO4 loãng không tác dụng?
Đáp án đúng là: D
Axit sunfuric đặc, nóng có tính háo nước và tính oxi hóa mạnh nên tác dụng được với Cu, S, đường saccarozơ (hút nước và tác dụng với C)
Câu 5:
Từ Zn, dung dịch H2SO4 loãng, CaCO3, KMnO4 có thể điều chế trực tiếp những khí nào sau đây?
Đáp án đúng là: B
Câu 6:
Cho các khí sau: SO2, H2S, Cl2, CO, CO2, O2, N2. Dãy gồm các khí gây ô nhiễm môi trường là:
Đáp án đúng là: A
Câu 7:
Cho các cặp chất sau: (1) CuCl2 + BaS; (2) AgNO3 + KCl; (3) HCl + FeS; (4) CO2 + Ca(OH)2 dư; (5) Fe + H2SO4. Số cặp chất phản ứng với nhau tạo kết tủa là:
Đáp án đúng là: C
Câu 8:
Nung nóng bình kín chứa m gam hỗn hợp Fe, Cu và 6,4 gam O2 sau một thời gian thu được 18,5 gam hỗn hợp chất rắn và 2,9 gam O2 dư. Giá trị của m là:
Đáp án đúng là: B
Khối lượng O2 đã phản ứng là:
Khối lượng kim loại là:
Câu 11:
Chỉ dùng một thuốc thử nào có thể phân biệt được các khí Cl2, HCl, O2?
Đáp án đúng là: B
2 n
Số mol H2 là:
Từ phương trình
Lập bảng giá trị của n:
|
n |
1 |
2 |
3 |
|
M |
32,5 (loại) |
65 (chọn) |
97,5 (loại) |
Vậy kim loại M là Zn
Câu 12:
Cho 6,5 gam kim loại R hóa trị n tác dụng hoàn toàn với dung dịch HCl dư thì thu được 2,24 lít khí (đktc). R là kim loại nào?
Đáp án đúng là: A
Câu 14:
Cặp chất nào sau đây không thể cùng tồn tại trong một dung dịch?
Đáp án đúng là: C
Cặp chất phản ứng với nhau thì không tồn tại trong cùng một dung dịch.
Câu 15:
Trong phòng thí nghiệm có thể điều chế khí lưu huỳnh đioxit bằng cách
Đáp án đúng là: D
Trong phòng thí nghiệm, điều chế lưu huỳnh đioxit bằng cách cho muối sunfit (dạng rắn) tác dụng với axit (HCl, H2SO4), thu khí SO2 vào lọ bằng cách đẩy không khí.
Câu 16:
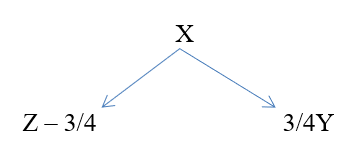
Hoàn thành sơ đồ phản ứng sau và viết các phương trình hóa học tương ứng:
Các chất rắn A, B, C theo thứ tự là SO2, SO3, H2SO4
Các phương trình phản ứng xảy ra:
Câu 17:
Nêu và giải thích hiện tượng xảy ra khi cho từ từ dung dịch NaOH vào dung dịch AlCl3 đến dư. Viết các phương trình phản ứng.
Khi cho dung dịch NaOH từ từ vào dung dịch AlCl3, ban đầu ta thấy tạo kết tủa trắng keo do xảy ra phản ứng tạo Al(OH)3.
Sau đó khi kết tủa không tạo thêm được nữa, nếu tiếp tục cho dung dịch NaOH vào thì thấy kết tủa tan dần đến hết, tạo dung dịch trong suốt không màu, do NaOH dư tiếp tục tác dụng với Al(OH)3 tạo dung dịch muối tan.
Câu 18:
Chỉ dùng giấy quỳ tím, nhận biết các dung dịch trong suốt không màu sau: NaOH, H2SO4, Ba(NO3)2, K2SO4, NaCl
Nhận biết các chất theo bảng dưới đây:
|
|
NaOH |
H2SO4 |
Ba(NO3)2 |
K2SO4 |
NaCl |
|
Quỳ tím |
Hóa xanh |
Hóa đỏ |
Không đổi màu |
Không đổi màu |
Không đổi màu |
|
H2SO4 |
|
|
Kết tủa trắng |
Không hiện tượng |
Không hiện tượng |
|
Ba(NO3)2 |
|
|
|
Kết tủa trắng |
|
Các phương trình hóa học xảy ra:
Câu 19:
Nung nóng 42,4 gam hỗn hợp Fe và S trong môi trường không có không khí, thu được hỗn hợp X. Cho X vào dung dịch HCl dư thu được 11,2 lít hỗn hợp khí Y (đktc). Biết các phản ứng xảy ra hoàn toàn.
a) Viết các phương trình hóa học xảy ra.
a)
Câu 20:
b) Tính thành phần phần trăm theo khối lượng mỗi chất trong hỗn hợp ban đầu.
b) Vì khi tác dụng với HCl thu được hỗn hợp khí nên trong hỗn hợp X còn Fe dư
Gọi x, y lần lượt là số mol Fe và S trong hỗn hợp ban đầu.
Theo phương trình (1), số mol Fe phản ứng là y mol
Vậy số mol Fe dư sau phản ứng (1) là: x – y )mol
Khối lượng chất ban đầu là:
56x + 32y = 42,4 (g) (*)
Số mol khí thu được là:
Mà
Kết hợp với (*) suy ra y = 0,45 mol
Thành phần phần trăm về khối lượng của hỗn hợp ban đầu là: