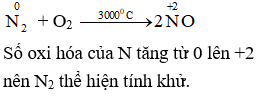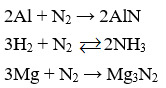15 câu trắc nghiệm Nitơ cực hay có đáp án
-
4013 lượt thi
-
15 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 2:
Khi có tia lửa điện hoặc ở nhiệt độ cao, nitơ tác dụng trực tiếp với oxi tạo ra hợp chất X. Công thức của X là
Chọn C
![]()
Câu 6:
Nung nóng 4,8 gam Mg trong bình phản ứng chứa 1 mol khí . Sau một thời gian, đưa bình về nhiệt độ ban đầu, thấy áp suất khí trong bình giảm 5% so với áp suất ban đầu. Thành phần phần trăm Mg đã phản ứng là
Chọn D
Trong bình phản ứng cùng thể tích, nhiệt độ do đó áp suất tỉ lệ với số mol, áp suất bình giảm 5% so với ban đầu => nN2 pư = 5% ban đầu = 0,05 mol
nMg = 3nN2 = 0,15
Câu 7:
Hỗn hợp và trong bình phản ứng ở nhiệt độ không đổi. Sau thời gian phản ứng, áp suất các khí trong bình thay đổi 5% so với áp suất ban đầu. biết rằng số mol đã phản ứng là 10%. Thành phần phần trăm số mol trong hỗn hợp ban đầu là
Chọn B
Áp suất thay đổi 5% so với áp suất ban đầu =>
Giả sử trước phản ứng có 1 mol => sau phản ứng có 0,95 mol
ntrước – nsau = 2nN2 pư = 0,05 mol
è nN2 ban đầu = 0,025:10% = 0,25 =>%nN2 = 25%
Câu 9:
Hiệu suất của phản ứng giữa tạo thành tăng nếu
Chọn D
N2 + 3H2 2NH3 ∆H <0
Chiều thuận của phản ứng có tổng số mol khí giảm => muốn tăng hiệu suất thì tăng áp suất
Chiều thuận của phản ứng là chiều tỏa nhiệt => tăng hiệu suất thì giảm nhiệt độ
Câu 10:
Hỗn hợp khí X gồm có tỉ khối hơi so với He bằng 1,8. Đun nóng trong bình kín một thời gian (có bột Fe làm xúc tác) thu được hỗn hợp khí Y có tỉ khối hơi so với He bằng 2. Hiệu suất phản ứng tổng hợp là
Chọn C
MX = 4.1,8 = 7,2
Xét 1 mol hỗn hợp gồm a mol N2 và b mol H2:
a + b = 1; 28a + 2b = 7,2 Þ a = 0,2; b = 0,8 (mol)
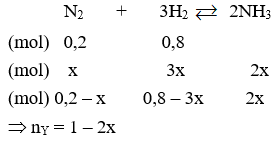
Mà MY = 4.2 = 8; mY = mX = 7,2 Þ nY = 0,9 = 1 – 2x
x=0,05 mol
Câu 12:
Trong phản ứng nào sau đây, nitơ thể hiện tính khử ?
Chọn C
+ O2
Số oxi hóa của N tăng từ 0 lên +2 nên N2 thể hiện tính khử.
Câu 14:
Hỗn hợp X gồm có . Dẫn X đi qua bình đựng bột Fe rồi nung nóng biết hiệu suất tổng hợp đạt 40% thì thu được hỗn hợp Y. có giá trị là :
Chọn C
Áp dụng sơ đồ đường chéo cho hỗn hợp N2 và H2 ta có :
Với tỉ lệ trên suy ra H2 thiếu, hiệu suất phản ứng tính theo H2.
Trong hỗn hợp X ta chọn
Số mol H2 phản ứng là 3.40% = 1,2 mol, suy ra số mol N2 phản ứng là 0,4 mol, số mol NH3 sinh ra là 0,8 mol. Sau phản ứng số mol khí giảm là (1,2 + 0,4) – 0,8 = 0,8 mol.
Sau phản ứng số mol khí giảm là 0,8 mol nên :
Theo định luật bảo toàn khối lượng ta có :
Vậy
Câu 15:
Một bình kín có thể tích là 0,5 lít chứa 0,5 mol và 0,5 mol , ở nhiệt độ . Khi ở trạng thái cân bằng có 0,2 mol tạo thành. Hằng số cân bằng của phản ứng tổng hợp là :
Chọn B
Theo giả thiết ta thấy ban đầu .
Thực hiện phản ứng tổng hợp NH3 đến thời điểm cân bằng
Phương trình phản ứng hoá học :
Theo (1) tại thời điểm cân bằng [NH3] = 0,8M; [H2] =0,4M; [NH3] = 0,4M.
Vậy hằng số cân bằng của phản ứng tổng hợp NH3 là :