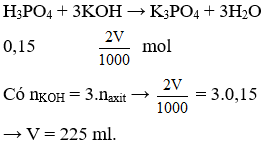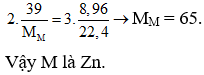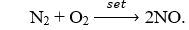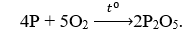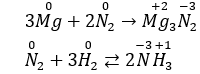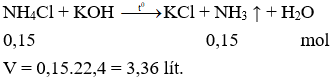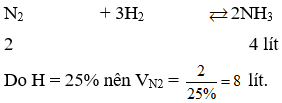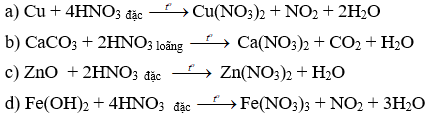Đề thi Hóa học lớp 11 Giữa kì 1 có đáp án (Đề 1)
-
1422 lượt thi
-
19 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Phần I: Trắc nghiệm
Trung hòa 100ml dung dịch 1,5M cần Vml dung dịch KOH 2M. Giá trị của V là
Chọn C
Câu 3:
Muối amoni là chất điện li thuộc loại nào?
Chọn B
Tất cả các muối amoni đều dễ tan trong nước và khi tan điện li hoàn toàn thành các ion.
Câu 4:
Cho 39 gam kim loại M phản ứng hoàn toàn với dung dịch thu được 8,96 lit khí NO (là sản phẩm khử duy nhất ở đktc). Kim loại M là
Chọn A
Theo các đáp án xác định được số e nhường ở các trường hợp là bằng nhau và bằng 2. Áp dụng định luật bảo toàn electron có :
Câu 9:
Nitơ đóng vai trò là chất oxi hóa trong phản ứng với
Chọn D
đóng vai trò là chất oxi hóa khi tác dụng với kim loại và hiđro.
Vd:
Câu 12:
Khi dung dịch axit đặc tác dụng với kim loại thì thông thường sẽ sinh khí nào sau đây?
Chọn C
Câu 14:
Cho dung dịch KOH dư vào 150ml dd 1M. Đun nhẹ thu được thể tích khí thoát ra ở (đktc) là
Chọn B
Câu 16:
Để điều chế 4 lít từ và với hiệu suất 25% thì thể tích cần dùng ở cùng điều kiện là:
Chọn A
Câu 18:
Bằng phương pháp hoá học hãy nhận biết các dung dịch mất nhãn sau:
Đánh số thứ tự từng lọ, trích mỗi lọ một ít sang ống nghiệm đánh số tương ứng.
- Cho vào mỗi ống nghiệm một mẩu quỳ tím
+ Quỳ tím không đổi màu → .
+ Quỳ tím chuyển sang màu đỏ → , HCl (nhóm I).
- Phân biệt nhóm I dùng
+ Không hiện tượng →
+ Có kết tủa trắng → HCl
Câu 19:
Cho 4,9 gam hỗn hợp Fe và Cu (trong đó Cu chiếm 60% khối lượng) vào một lượng dung dịch khuấy đều đến phản ứng hoàn toàn thấy còn lại 2,3 gam chất rắn không tan. Xác định khối lượng muối tạo thành sau phản ứng.
Theo bài ra ta có:
→ Sau phản ứng còn 2,3 gam < → chất rắn không tan là Cu, dung dịch sau phản ứng chứa và .
Có ;
= 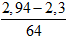
→ = 0,035.180 + 0,01. 188 = 8,18 gam.