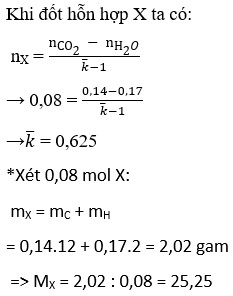Trắc nghiệm : Nguồn hidrocacbon thiên nhiên có đáp án ( vận dụng)
-
543 lượt thi
-
10 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Đốt cháy hoàn toàn một thể tích hơi hợp chất hữu cơ A cần 10 thể tích oxi (đo cùng điều kiện nhiệt độ và áp suất), sản phẩm thu được chỉ gồm CO2 và H2O với tỉ lệ khối lượng là 44 : 9. Biết MA < 150. A có công thức phân tử là :
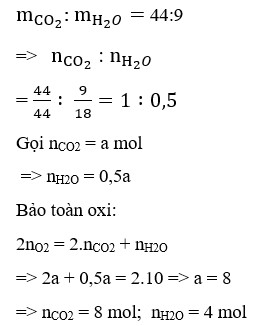
=> A: C8H8
Đáp án cần chọn là: C
Câu 2:
Ba hiđrocacbon X, Y, Z kế tiếp nhau trong dãy đồng đẳng, trong đó khối lượng phân tử Z gấp đôi khối lượng phân tử X. Đốt cháy 0,1 mol chất Y, sản phẩm khí hấp thụ hoàn toàn vào dung dịch Ca(OH)2 dư, thu được số gam kết tủa là:
Gọi CTPT của X là CxHy
Do X, Y, Z kế tiếp nhau trong dãy đồng đẳng nên Z hơn X hai nhóm –CH2
=> MY = MX + 14 và Mz = MX +28
Vì Mz = 2MX => MX +28 = 2.MX
=> MX = 28
=> X là C2H4 , Y là C3H6, Z là C4H8
C3H6 + O2 3CO2 + 3H2O
0,1 0,3
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
0,3 0,3
=> mkết tủa = 0,3.100 = 30 (gam)
Đáp án cần chọn là: C
Câu 3:
Cho hiđrocacbon X phản ứng với brom (trong dung dịch) theo tỉ lệ mol 1 : 1, thu được chất hữu cơ Y (chứa 74,08% Br về khối lượng). Khi X phản ứng với HBr thì thu được hai sản phẩm hữu cơ khác nhau. Tên gọi của X là :
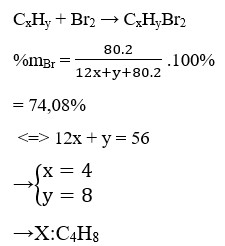
X phản ứng với HBr thu được 2 sản phẩm hữu cơ => X có cấu tạo bất đối xứng
=> X là CH2=CH-CH2-CH3
CH2=CH-CH2-CH3 + HBr → CH3-CHBr-CH2-CH3 (spc) + CH2Br-CH2-CH2-CH3 (spp)
Đáp án cần chọn là: A
Câu 5:
Dẫn 1,68 lít hỗn hợp khí X gồm hai hiđrocacbon vào bình đựng dung dịch brom (dư). Sau khi phản ứng xảy ra hoàn toàn, có 4 gam brom đã phản ứng và còn lại 1,12 lít khí. Nếu đốt cháy hoàn toàn 1,68 lít X thì sinh ra 2,8 lít khí CO2. Biết các thể tích khí đều đo ở đktc. Công thức phân tử của hai hiđrocacbon là:


Đáp án cần chọn là: C
Câu 6:
Hidrocacbon mạch hở X (26 < MX < 58). Trộn m gam X với 0,52 gam stiren thu được hỗn hợp Y. Đốt cháy hoàn toàn Y thu được 2,24 lít khí CO2 đktc và 0,9 gam H2O. Mặt khác, toàn bộ lượng Y trên làm mất màu tối đa a gam Br2 trong dung dịch. Giá trị của a là
nC8H8 = 0,005 mol
nCO2 = 0,1 mol; nH2O = 0,05 mol
Y + O2 :
C8H8 + 10 O2 → 8CO2 + 4H2O (1)
0,005 → 0,04 0,02 mol
CxHy + O2 xCO2 + H2O
0,06 0,03 mol
→ = = =2→ x = y → CTPT CxHx → 28 < 13x < 58 → 2,15 < x < 4,46
Chọn x = 4 vì x chẵn →X là C4H4 : 0,015 mol
Y + Br2 : C6H5CH=CH2 + Br2 → C6H5-CHBr – CH2Br
C4H4 + 3Br2 → C4H4Br6
→ nBr2 = 0,005 + 0,015.3 = 0,05 mol → mBr2 = 8 gam
Đáp án cần chọn là: D
Câu 7:
Hỗn hợp X có tỉ khối so với H2 là 21,2 gồm propan, propen và propin. Khi đốt cháy hoàn toàn 0,1 mol X, tổng khối lượng của CO2 và H2O thu được là:
Lời giải:
X gồm C3H8, C3H6, C3H4
=> Gọi chung công thức X là C3Hx
dx/H2 = 21,2 → X = 21,2 .2 = 42,4 = 12 . 3 + x
=> x = 6,4
=> Công thức X là C3H6,4
PTHH: C3H6,4 + 4,6 O2 3CO2 + 3,2H2O
0,1 → 0,3 →0,32
→ + = 0,3.44 + .18 = 18,96 g
Đáp án cần chọn là: C
Câu 8:
Hỗn hợp khí X gồm 0,3 mol H2 và 0,1 mol vinylaxetilen. Nung X một thời gian với xúc tác Ni thu được hỗn hợp khí Y có tỉ khối so với không khí là 1. Nếu cho toàn bộ Y sục từ từ vào dung dịch brom (dư) thì có m gam brom tham gia phản ứng. Giá trị của m là
BT khối lượng: mX = mY=0,3.2 + 0,1.52 = 5,8 gam
=> nY = = 0,2 mol
PTHH: C4H4 +H2 → C4H6
C4H4 +H2 → C4H6
Ta thấy chênh lệch giữa số mol X và Y là số mol H2 phản ứng
= nX – nY = 0,1 + 0,3 − 0,2 = 0,2 mol
Bảo toàn liên kết π: Do H2 và Br2 đều phản ứng vào liên kết π nên =>
=-= 0,1.3 − 0,2 = 0,1 mol → = 0,1.160 = 16 gam
Đáp án cần chọn là: A
Câu 10:
Dẫn V lít (ở đktc) hỗn hợp X gồm axetilen và hiđro đi qua ống sứ nung nóng, thu được khí Y. Dẫn Y vào lượng dư AgNO3 (hoặc Ag2O) trong dung dịch NH3 thu được 12 gam kết tủa. Khí đi ra khỏi dung dịch phản ứng vừa đủ với 16 gam brom và còn lại khí Z. Đốt cháy hoàn toàn khí Z thu được 2,24 lít khí CO2 (ở đktc) và 4,5 gam nước. Giá trị của V bằng:
C2H2 + H2 thu được Y => Y gồm C2H2, C2H4, C2H6 và H2 dư.
Y tác dụng với AgNO3/NH3:
HC ≡ CH + 2AgNO3 + NH3 → AgC ≡ CAg↓ + NH4NO3 + H2O
n↓ = 0,05mol => = 1,3 gam
=> Khí bay ra khỏi bình AgNO3/NH3 là C2H4, C2H6 và H2 dư
Cho qua bình đựng nước brom thì chỉ có C2H4 phản ứng được với brom
= = 0,1 mol => = 0,1.28 = 2,8 gam
Sau cho bình brom còn lại Z gồm C2H6 và H2 dư
Trong Z có:
Bảo toàn nguyên tố C: → mZ = mC + mH = 0,1.12 + 0,25.2 = 1,7 gam
= 0,05 + 0,1+ =0,2 mol → = 0,2.26 = 5,2 gam
Bảo toàn khối lượng ban đầu:
mX = 2,8 + 1,7 + 1,3 = 5,8 gam → = 5,8 – 5,2 = 0,6 gam
→ mol
Tổng thể tích khí:VX =22,4. (0,2 + 0,3) = 11,2 lít
Đáp án cần chọn là: A