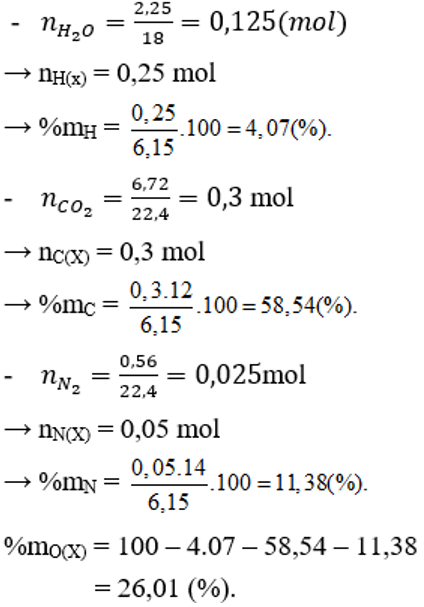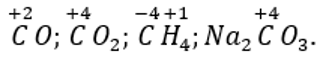Trắc nghiệm Chuyên đề Hóa 11 Đề kiểm tra học kì 1 (có đáp án) - Đề 4
-
797 lượt thi
-
22 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Trộn lẫn 300ml dung dịch NaOH 0,001M vào 300ml dung dịch HCl 0,003M thu được dung dịch X có giá trị pH là?
Đáp án C
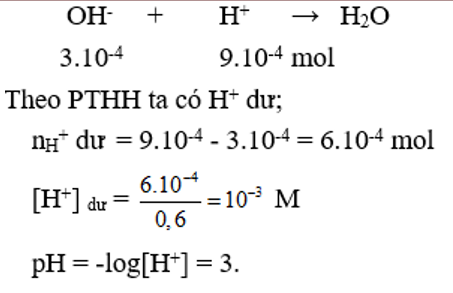
Câu 2:
Hiện tượng quan sát được khi cho lượng dư CO2 vào dung dịch nước vôi trong là ?
Đáp án A
CO2 + Ca(OH)2 → CaCO3 (↓ trắng) + H2O
CO2 dư + H2O + CaCO3 (↓ trắng) → Ca(HCO3)2 dd
Câu 3:
Chất nào sau đây không thể phản ứng với NH3 ?
Đáp án C
NH3 không thể phản ứng với NaOH.
Câu 4:
Trong dung dịch X có chứa : 0,15 mol Ca2+, 0,3 mol Na+, x mol SO42- và y mol NO3-. Cô cạn dung dịch thu được 45,9 gam chất rắn. Giá trị x, y lần lượt là
Đáp án C
Bảo toàn điện tích:
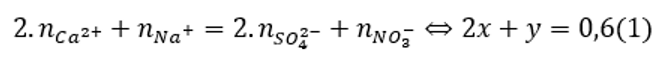
Bảo toàn khối lượng:
mmuối = ∑mion ↔ 96x + 62y = 45,9 – 0,15.40 – 0,3.23 = 33 (2)
Từ (1) và (2) có: x = 0,15 và y = 0,3.
Câu 5:
Cho khí CO dư qua hỗn hợp FeO, CuO, MgO, Al2O3 . Sau phản ứng chất rắn thu được chứa ?
Đáp án A
CO chỉ khử được oxit của các kim loại đứng sau Al trong dãy hoạt động hóa học của kim loại.
Vậy chất rắn thu được sau phản ứng là: Fe, Cu, MgO, Al2O3.
Câu 6:
Cho các chất sau đây: HCl, NaOH, NaCl, C2H5OH, H3PO4, C6H6, H2O. Số chất điện ly mạnh là ?
Đáp án B
Chất điện li mạnh gồm axit mạnh, bazơ mạnh và hầu hết các muối.
→ Các chất điện li mạnh là: HCl, NaOH, NaCl.
Câu 7:
HNO3 có thể oxi hóa được chất nào sau đây ?
Đáp án B
Trong FeO, nguyên tố Fe chưa đạt số oxi hóa cao nhất nên FeO bị oxi hóa bởi HNO3.
Câu 8:
Xét phương trình: NaOH + HCl → NaCl + H2O có phương trình thu gọn là
Đáp án C
Phương trình ion rút gọn là: H+ + OH- → H2O.
Câu 9:
Khi nhiệt phân muối rắn nào sau đây sinh ra oxit kim loại ?
Đáp án B
Muối nitrat của Mg, Zn, Fe, Pb, Cu … bị phân hủy tạo ra oxit kim loại tương ứng, NO2 và O2.
Câu 11:
Hấp thụ hoàn toàn 8,96(l) CO2 (đktc) vào 400ml dung dịch Ba(OH)2 1M thu được a(g) kết tủa. Giá trị của a là
Đáp án D
Ta có:
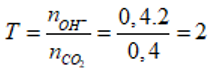 nên sau phản ứng thu được muối trung hòa, hai chất tham gia phản ứng hết.
nên sau phản ứng thu được muối trung hòa, hai chất tham gia phản ứng hết.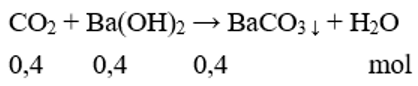
a = 0,4.197 = 78,8 gam.
Câu 13:
Nhiệt phân hoàn toàn m(g) muối Cu(NO3)2 một thời gian thấy khối lượng chất rắn giảm 1,08(g). Giá trị của m là
Đáp án A
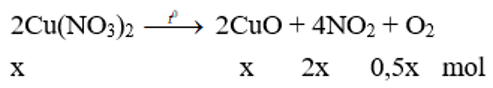
Khối lượng chất rắn giảm chính là khối lượng khí
→ 92x + 16x = 1,08 → x = 0,01 (mol)
m = 0,01.188 = 1,88 gam.
Câu 15:
Phát biểu nào sau đây là đúng ?
Đáp án B
A sai vì photpho trắng không tan trong nước, rất độc.
C sai vì photpho đỏ kém hoạt động hóa học hơn photpho trắng.
D sai vì photpho đỏ không phát quang trong bóng tối.
Câu 16:
Chất nào sau đây có thể hòa tan CaCO3 ?
Đáp án B
CaCO3 + 2HCl → CaCl2 + CO2 + H2O.
Câu 18:
Cho luồng khí CO dư qua 9,1g hỗn hợp CuO, MgO đến khi phản ứng hoàn toàn thu được 8,3g chất rắn. Khối lượng CuO có trong hỗn hợp là
Đáp án C
Cho CO qua hỗn hợp CuO và MgO chỉ có CuO phản ứng:
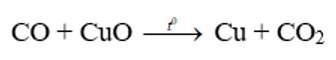
Khối lượng chất giảm chính là khối lượng O trong CuO.
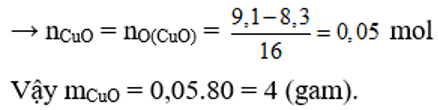
Câu 19:
Hai chất CH3COOH và CH2=CH-COOH giống nhau về ?
Đáp án C
Hai chất đều có nhóm chức – COOH.
Câu 20:
Cho các phát biểu sau đây:
1- Liên kết trong hợp chất hữu cơ chủ yếu là liên kết cộng hóa trị.
2- CuSO4 khan dùng để phát hiện nước lẫn trong hợp chất hữu cơ.
3- Hợp chất hữu cơ được chia làm 3 loại cơ bản : hiđrocabon, dẫn xuất hiđrocacbon, hợp chất có oxi.
4- Các chất hữu cơ thường kém bền nhiệt, dễ cháy.
Số phát biểu sai là
Đáp án A
Phát biểu 3 sai vì hợp chất hữu cơ được chia thành 2 loại cơ bản là hiđrocabon và dẫn xuất hiđrocacbonCâu 21:
Hòa tan hoàn toàn 12,84g hỗn hợp Al, Cu vào lượng dư dung dịch HNO3 loãng, nóng thu được 4,928 (lít) NO là sản phẩm khử duy nhất ở điều kiện tiêu chuẩn và dung dịch X. Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Gọi số mol Al và Cu trong hỗn hợp lần lượt là x và y (mol)
mKL = 12,84 gam → 27x + 64y = 12,84 (1)
PTHH:
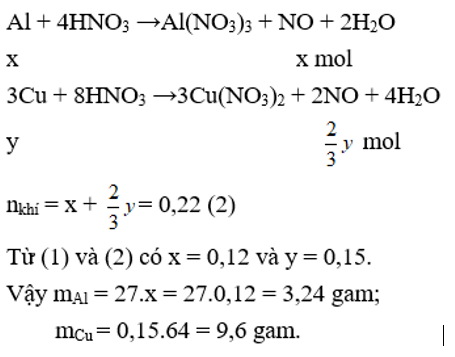
Câu 22:
Đốt cháy hoàn toàn 6,15g chất hữu cơ X thu được 2,25g H2O; 6,72(l) CO2 và 0,56(l) N2 (đktc). Tính % khối lượng các chất trong X.
Đốt cháy hoàn toàn X thu được H2O, CO2 và N2 nên X chứa C, H, N và có thể có O.