Đề thi Hóa 11 giữa kì 1 có đáp án (Đề 6)
-
1450 lượt thi
-
31 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 1:
Chất nào sau đây không dẫn điện được?
Đáp án A
Do KCl rắn, khan tồn tại dưới dạng mạng tinh thể ion, rất bền vững. Không phân li ra được ion dương và ion âm (di chuyển tự do) nên không có khả năng dẫn điện.
Câu 2:
Chất nào sau đây thuộc loại chất điện li mạnh?
Đáp án D
Loại A vì: C2H5OH không phải là chất điện li.
Loại B vì: H2O là chất điện li yếu: H2OH+ + OH–.
Loại C vì: CH3COOH là chất điện li yếu: CH3COOH CH3COO– + H+.
Loại D vì: BaCl2 là chất điện li mạnh: BaCl2 Ba2+ + 2Cl–.
Câu 4:
Phương trình điện li nào dưới đây được viết đúng?
Đáp án B
Phương trình điện li đúng: H2CO3 2H+ + CO32-.
A và D sai vì CuSO4, NaOH là các chất điện li mạnh.
C sai vì H2S là chất điện li yếu.
Câu 5:
Dung dịch chất nào sau đây (có cùng nồng độ) dẫn điện tốt nhất?
Đáp án B
Dung dịch dẫn điện tốt nhất là dung dịch có tổng nồng độ ion lớn nhất.
Nhận thấy 4 đáp án đều là chất điện li mạnh.
Phương trình điện li:
K2SO4 → 2K+ + SO42-
KOH → K+ + OH–
NaCl → Na+ + Cl-
KNO3 → K+ + NO3-
Suy ra cùng nồng độ chất tan nhưng lượng ion do K2SO4 phân li sẽ là lớn nhất.
Vậy dung dịch K2SO4 dẫn điện tốt nhất.
Câu 6:
Dung dịch chất nào sau đây làm quỳ tím hóa đỏ?
Đáp án A
Dung dịch làm quỳ tím hóa đỏ là axit HCl.
Câu 7:
Đối với dung dịch axit yếu H3PO4 0,10M, nếu bỏ qua sự điện li của nước thì đánh giá nào về nồng độ mol ion sau đây là đúng?
Đáp án D
Ta có phương trình điện li:
Từ phương trình ta thấy:
[H+] < 3[H3PO4] suy ra [H+] < 0,30M.
Câu 9:
Đặc điểm phân li Zn(OH)2trong nước là
Đáp án B
Đặc điểm phân li Zn(OH)2trong nước là vừa theo kiểu axit vừa theo kiểu bazơ.
Zn(OH)2⇄ Zn2++ 2OH-
Zn(OH)2⇄ 2H++ ZnO22-
Câu 10:
Dung dịch NaOH 0,001M có pH bằng:
Đáp án C
NaOH là chất điện li mạnh suy ra [OH-] = CM (NaOH)= 0,001M
⇒ pOH = -log[OH-] = -log(0,001) = 3 ⇒ pH = 14 – 3 = 11.
Câu 11:
Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ có thể xảy ra khi có ít nhất một trong các điều kiện nào sau đây ?
Đáp án D
Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất một trong các chất sau:
- Chất kết tủa.
- Chất điện li yếu.
- Chất khí.
Câu 12:
Phương trình ion rút gọn H++ OH-→ H2O biểu diễn bản chất của phản ứng hoá học nào dưới đây?
Đáp án A
Phương trình ion rút gọn H++ OH-→ H2O biểu diễn bản chất của phản ứng hoá học HCl + NaOH → H2O + NaCl.
Loại B vì: OH-+ HCO3-→ CO32-+ H2O
Loại C vì: Ba2++ SO42-→ BaSO4↓
Loại D vì: Mg(OH)2+ 2H2+→ Mg2++ 2H2O
Câu 13:
Cặp dung dịch nào sau đây phản ứng với nhau tạo thành chất khí?
Đáp án C
Loại A vì : 2HCl +Na2HPO4→ 2NaCl + H3PO4
Loại B vì: Ba(OH)2 + 2HNO3→ Ba(NO3)2 + 2H2O
Chọn C vì: Na2CO3+ H2SO4→ Na2SO4+ CO2↑ + H2O
Loại D vì: 2NaOH + CaCl2→ Ca(OH)2↓ + 2NaCl
Câu 14:
Xét pH của bốn dung dịch có nồng độ mol/lít bằng nhau là dung dịch HCl, pH = a; dung dịch H2SO4, pH = b; dung dịch NaCl, pH = c và dung dịch NaOH pH = d. Nhận định nào dưới đây là đúng?
Đáp án D
Giá trị pH tỉ lệ nghịch với nồng độ H+, suy ra chất càng phân li ra nhiều H+ thì chất đó có pH càng nhỏ.
Vậy b< a< c< d.
Câu 15:
Muối nào sau đây là muối axit?
Đáp án B
+ Muối axit là muối mà gốc axit còn hidro có khả năng phân li ra H+
+ Trong các muối đã cho, muối axit là: Ca(HSO4)2.
Ca(HSO4)2→ Ca2++ 2HSO4-.
HSO4-→ H++ SO42-.
Câu 16:
Dung dịch nào dưới đây dùng để phân biệt dung dịch NaCl với dung dịch Na2SO4?
Đáp án B
Dùng dung dịch BaCl2 vì cho vào dung dịch Na2SO4 có kết tủa trắng, còn cho vào dung dịch NaCl thì không có hiện tượng gì.
Phương trình phản ứng: Na2SO4 + BaCl2 → BaSO4 (↓ trắng)+ 2NaCl
Câu 17:
Muốn thu khí NH3vào bình thì có thể thu theo cách nào sau đây?
Đáp án A
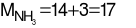 g/mol, Mkk= 29
g/mol, Mkk= 29
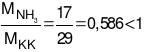
Suy ra khí NH3 nhẹ hơn không khí
Vậy ta nên đặt úp bình vì khí NH3 nhẹ hơn sẽ được đẩy lên trên còn không khí sẽ chìm xuống vì nặng hơn.
Không thu NH3bằng cách đẩy nước vì NH3tan nhiều trong nước.
Câu 18:
Để tạo độ xốp cho một số loại bánh, có thể dùng muối nào sau đây:
Đáp án C
Để tạo độ xốp cho một số loại bánh, có thể dùng muối: NH4HCO3.
NH4HCO3 NH3↑ + CO2↑ + H2O
NH3↑ + CO2↑ + H2O
Khi sử dụng bột nở này, khí NH3 và CO2 thoát ra làm cho bánh căng phồng và xốp.
Câu 19:
Cho khí NH3tác dụng với khí Cl2thấy có:
Đáp án C
2NH3 + 3Cl2 → N2 + 6HCl
NH3 khí + HClkhí → NH4Cl (khói trắng)
Câu 20:
Thành phần của dung dịch amoniac nào sau đây đúng?
Đáp án A
Trong dung dịch NH3 tồn tại cân bằng:
NH3 + H2O ⇆ NH4+ + OH-
Vậy nên trong dung dịch NH3 gồm có: NH4+; OH-; H2O; NH3
Câu 21:
Nhiệt phân muối nào sau đây không thu được khí NH3?
Đáp án D
Phương trình phản ứng:
NH4NO2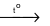 N2+ 2H2O
N2+ 2H2O
Câu 22:
Chất nào sau đây khôngphải là sản phẩm khử của HNO3?
Đáp án C
Chất không phải là sản phẩm khử của HNO3là: NH3.
Câu 23:
Nhóm các kim loại đều không phản ứng được với HNO3:
Đáp án B
Các kim loại Au, Pt là những kim loại hoạt động hóa học rất yếu, không phản ứng với HNO3.
Câu 24:
Phương trình phản ứng nào sau đây không thể hiện tính khử của NH3?
Đáp án A
NH3+ HNO3→ NH4NO3
Do số oxi hóa của nguyên tố nitơ không tăng sau phản ứng nên phản ứng không thể hiện tính khử của NH3.
Câu 25:
Sản phẩm của phản ứng nhiệt phân nào dưới đây là không đúng?
Đáp án D
Sửa lại: NH4NO3 2H2O + N2O
2H2O + N2O
Câu 27:
Cho kim loại đồng vào dung dịch HNO3thu được sản phẩm khử duy nhất là khí X màu nâu. Khí X là ?
Đáp án B
Phương trình phản ứng:
Cu + 4HNO3(đặc) → Cu(NO3)2+ 2NO2+ 2H2O
NO2là khí có màu nâu đỏ.
Câu 28:
Cho phản ứng: Cu + HNO3→ Cu(NO3)2+ NO + H2O. Hệ số của HNO3trong phản ứng trên là:
Đáp án A
Phương trình phản ứng:
3Cu + 8HNO3→ 3Cu(NO3)2+ 2NO + 4H2O
Câu 29:
Viết phương trình điện li và phân loại các chất sau: NaOH, HClO, Na2SO4, Zn(OH)2. (1 điểm)
Phương trình điện li và phân loại:
- Bazơ: NaOH → Na++OH-
- Axit: HClO ⇄ H++ ClO-
- Muối: Na2SO4→ 2Na++ SO42-
- Hiđroxit lưỡng tính: Zn(OH)2:
+ Sự phân li theo kiểu bazơ: Zn(OH)2⇄ Zn2++ 2OH-
+ Sự phân li theo kiểu axit: Zn(OH)2⇄ 2H++ ZnO22-
Câu 30:
Dung dịch B chứa 0,2 mol Na+, 0,2 mol Cl-, x mol K+và y mol CO32-. Cô cạn B thì thu được 25,5 gam muối khan. Tìm giá trị của x và y? (1 điểm)
Áp dụng định luật bảo toàn điện tích ta có:
0,2 + x = 0,2 + 2y hay x – 2y = 0 (1)
Có mmuối= 0,2.23 + 0,2. 35,5 + 39x + 60y = 25,5
Suy ra 39x + 60y = 13,8 (2)
Từ (1) và (2) suy ra x = 0,2 và y = 0,1
Câu 31:
Hoà tan hoàn toàn m gam nhôm trong dung dịch HNO3dư ta thu được 3,36 lít khí N2O là sản phẩm khử duy nhất ở (đktc). Tìm giá trị của m cần dùng. (1 điểm)
Số mol của N2O là: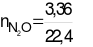 = 0,15 mol
= 0,15 mol
Phương trình phản ứng:

Suy ra m = mAl= 0,4.27 = 10,8 gam.
( Cho Al=27; Na=23;K=39; Cl=35,5; C=12;O=16;N=14)


 = 0,45M
= 0,45M