Đề thi Hóa 11 giữa kì 1 có đáp án (Đề 9)
-
1453 lượt thi
-
31 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 1:
Dung dịch chất nào sau đây không dẫn điện?
Đáp án A
Khi tan trong nước các dung dịch: CuSO4, NaCl, KBr có khả năng phân li ra ion.
CH3OH trong dung dịch không có khả năng phân li ion nên không dẫn điện.
Câu 2:
Chất nào sau đây là chất điện li yếu?
Đáp án C
Chất điện li yếu: CH3COOH.
Phương trình điện li: CH3COOHCH3COO-+ H+
Câu 3:
Sự điện li là
Đáp án B
Sự điện li là sự phân li các chất thành ion khi tan trong nước.
Câu 4:
Phương trình điện li viết đúng là
Đáp án D
Phương trình điện li viết đúng là Ca(OH)2→ Ca2++ 2OH-
A sai vì NaCl → Na++ Cl-
B sai vì CH3COOH là chất điện li yếu.
C sai vì C2H5OH là chất không điện li.
Câu 5:
Các dung dịch sau đây có cùng nồng độ 1M, dung dịch nào dẫn điện tốt nhất
Đáp án B
Dung dịch có nồng độ các ion càng lớn thì độ dẫn điện càng tốt.
Nồng độ mol các dung dịch là 1M.
Ý A. NH4NO3 → NH4+ + NO3–suy ra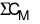 ion = 2M.
ion = 2M.
Ý B. Al2(SO4)3 → 2Al3+ + 3SO42– suy ra 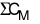 ion = 5M.
ion = 5M.
Ý C. Ba(OH)2 → Ba2+ + 2OH– suy ra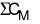 ion = 3M.
ion = 3M.
Ý D. H2SO4 → 2H+ + SO42– suy ra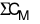 ion = 3M.
ion = 3M.
Vậy dung dịch Al2(SO4)3 dẫn điện tốt nhất
Câu 6:
Theo thuyết Areniut thì chất nào sau đây là bazơ?
Đáp án C
Theo thuyết Areniut thì bazơ là chất khi tan trong nước phân li ra OH-.
Vậy chất là bazơ là: LiOH
Câu 7:
Đối với dung dịch axit mạnh HNO30,10M, nếu bỏ qua sự điện li của nước thì đánh giá nào về nồng độ mol ion sau đây là đúng?
Đáp án A
HNO3 là một axit mạnh nên khi hòa tan trong nước bị phân li hoàn toàn thành ion.
HNO3→ H++ NO3-
Vậy [H+] = 0,1M.
Câu 8:
Nồng độ mol của anion Cl-trong dung dịch FeCl30,45M là
Đáp án C

Vậy nồng độ mol của anion Cl-trong dung dịch FeCl30,45M là 1,35M.
Câu 9:
Chất nào sau đây không có tính lưỡng tính?
Đáp án B
Chất không có tính lưỡng tính là: Na2CO3.
Na2CO3→ 2Na++ CO32-
Câu 10:
Dung dịch NaOH 0,01M có pH bằng:
Đáp án D
NaOH là chất điện li mạnh suy ra [OH-] = CM(NaOH)= 0,01M
⇒ pOH = -log[OH-] = -log(0,01) = 2
⇒ pH = 14 - pOH = 14 - 2 = 12
Câu 11:
Phương trình ion rút gọn của phản ứng cho biết
Đáp án C
Phương trình ion rút gọn của phản ứng cho biết: Bản chất của phản ứng trong dung dịch các chất điện li
Câu 12:
Phản ứng hóa học nào sau đây có phương trình ion rút gọn: H+ + OH- H2O
Đáp án A
KOH + HNO3 KNO3 + H2O
Có phương trình ion rút gọn: H+ + OH- H2O
Câu 13:
Cặp dung dịch nào sau đây phản ứng với nhau không tạo thành kết tủa?
Đáp án D
2NaOH + H2SO4→ Na2SO4+ 2H2O
Câu 14:
Các dung dịch NaCl, NaOH, NH3, Ba(OH)2có cùng nồng độ mol. Giá trị pH của các dung dịch được sắp xếp theo chiều tăng dần từ trái sang phải là:
Đáp án B
+ NaCl: môi trường trung tính, NH3: bazơ yếu, NaOH, Ba(OH)2: bazơ mạnh và giá trị pH tỉ lệ thuận với nồng độ OH- suy ra chất càng phân li ra nhiều OH- thì chất đó có pH càng lớn
+ Giá trị pH của các dung dịch được sắp xếp theo chiều tăng dần từ trái sang phải là: NaCl, NH3, NaOH, Ba(OH)2
Câu 15:
Muối nào sau đây là muối axit?
Đáp án A
+ Muối axit là muối mà gốc axit còn H có khả năng phân li ra H+
+ Trong các muối đã cho, muối axit là: NaHSO4.
NaHSO4→ Na++ HSO4-
HSO4-→ H++ SO42-
Câu 16:
Dung dịch nào dưới đây dùng để phân biệt dung dịch KCl với dung dịch K2SO4?
Đáp án C
Sử dụng BaCl2:
+ K2SO4phản ứng với BaCl2 tạo kết tủa trắng.
K2SO4+ BaCl2→ 2KCl + BaSO4 (↓)
+ KCl không phản ứng với BaCl2
Câu 17:
Khí nitơ tương đối trơ ở nhiệt độ thường là do
Đáp án D
Khí nitơ tương đối trơ ở nhiệt độ thường là do trong nguyên tử N2có liên kết ba bền.
Câu 18:
Cặp công thức của liti nitrua và nhôm nitrua là
Đáp án C
+ Khi liên kết với kim loại nitơ dễ nhận thêm 3e (nên có số oxi hóa -3); còn Li dễ nhường 1e và Al dễ nhường 3e (nên lần lượt có số oxi hóa là +1 và +3)
+ Cặp công thức của liti nitrua và nhôm nitrua là Li3N và AlN.
Câu 19:
Cho vài giọt phenolphtalein vào dung dịch NH3thì dung dịch chuyển thành
Đáp án B
Dung dịch NH3 là bazơ làm hồng phenolphtalein.
Câu 20:
Khí không màu hóa nâu ngoài không khí là:
Đáp án A
Khí không màu hóa nâu ngoài không khí là: NO.
2NO(không màu)+ O2→ 2NO2 (nâuđỏ)
Câu 21:
Dung dịch muối NH4Cl có môi trường?
Đáp án B
Dung dịch muối NH4Cl có môi trường: Axit.
NH4Cl → NH4++ Cl-
NH4++ H2O → NH3+ H3O+
Câu 22:
Hợp chất nào sau đây của nitơ không được tạo ra khi cho HNO3tác dụng với kim loại?
Đáp án D
N2O5 là oxit cao nhất của nitơ. Trong N2O5thì N số oxi hóa +5 nên không thể tạo ra khi cho kim loại tác dụng với HNO3.
Câu 23:
Các kim loại đều tác dụng được với dung dịch HCl nhưng không tác dụng với dung dịch HNO3đặc, nguội:
Đáp án A
Các kim loại đều tác dụng được với dung dịch HCl nhưng không tác dụng với dung dịch HNO3đặc, nguội: Fe, Al, Cr
Phương trình phản ứng:
Fe + 2HCl → FeCl2+ H2
2Al + 6HCl → 2AlCl3+ 3H2
Cr + 2HCl → CrCl2+ H2
Câu 24:
Trong các phản ứng sau, phản ứng nào NH3 đóng vai trò là chất khử?
Đáp án C
Phản ứng NH3 đóng vai trò là chất khử là: 8NH3+ 3Cl2→ 6NH4Cl + N2
Vì số oxi hóa của N tăng từ -3 lên 0 sau phản ứng.
Câu 25:
Hãy cho biết phản ứng nào sau đây không có trong quá trình sản xuất HNO3trong công nghiệp?
Đáp án D
Quá trình sản xuất HNO3:
NH3→ NO → NO2→ HNO3
Câu 26:
Thuốc nổ đen là hỗn hợp nào sau đây?
Đáp án D
Thành phần của thuốc nổ đen KNO3(74,64%), C (13,51%), S (11,85%)
2KNO3+ 3C + S → K2S + N2+ 3CO2
Câu 27:
Hợp chất nào sau đây nitơ có số oxi hóa cao nhất?
Đáp án A
Trong hợp chất N2O5 thì N có số oxi hóa cao nhất (+5).
Câu 28:
Cho phản ứng: FeO + HNO3→ Fe(NO3)3+ NO + H2O. Hệ số của HNO3trong phản ứng trên là:
Đáp án B
3FeO + 10HNO3→ 3Fe(NO3)3+ NO + 5H2O
Câu 29:
Viết phương trình điện li và phân loại các chất sau: NaOH, HClO, Na2SO4, Zn(OH)2.
Phương trình điện li và phân loại:
- Bazơ: NaOH → Na+ +OH-
- Axit: HClO ⇄ H+ + ClO-
- Muối: Na2SO4 → 2Na+ + SO42-
- Hiđroxit lưỡng tính: Zn(OH)2:
+ Sự phân li theo kiểu bazơ: Zn(OH)2 ⇄ Zn2+ + 2OH-
+ Sự phân li theo kiểu axit: Zn(OH)2 ⇄ 2H+ + ZnO2
Câu 30:
Dung dịch B chứa 0,2 mol Na+, 0,2 mol Cl-, x mol K+và y mol CO32-. Cô cạn B thì thu được 25,5 gam muối khan. Tìm giá trị của x và y? (1 điểm)
Áp dụng định luật bảo toàn điện tích ta có: 0,2 + x = 0,2 + 2y suy ra x – 2y = 0 (1)
Có mmuối= 0,2.23 + 0,2. 35,5 + 39x + 60y = 25,5
Suy ra 39x + 60y = 13,8 (2)
Từ (1) và (2) suy ra x = 0,2 và y = 0,1
Câu 31:
Hoà tan hoàn toàn m gam nhôm trong dung dịch HNO3dư ta thu được 3,36 lít khí N2O là sản phẩm khử duy nhất ở (đktc). Tìm giá trị của m cần dùng. (1 điểm)
Số mol của N2O là: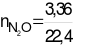 = 0,15 mol
= 0,15 mol
Phương trình phản ứng:

Suy ra m = mAl= 0,4.27 = 10,8 gam.
( Cho Al=27; Na=23;K=39; Cl=35,5; C=12;O=16; N=14)
