Bộ 30 đề thi học kì 1 Hóa 11 có đáp án (Đề 20)
-
4708 lượt thi
-
21 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Một học sinh đã điều chế và thu khí NH3 theo sơ đồ sau đây, nhưng kết quả thí nghiệm không thành công. Lí do chính là:
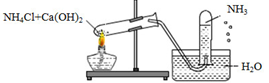
Chọn đáp án B
Phương pháp giải:
Dựa vào tính tan của NH3
Giải chi tiết:
NH3 tan nhiều trong nước nên ta không sử dụng phương pháp đẩy nước để thu khí.
Câu 2:
Chọn đáp án D
Phương pháp giải:
Ghi nhớ cách đánh giá độ dinh dưỡng của một số loại phân:
Đạm: %N
Lân: %P2O5
Kali: %K2O
Giải chi tiết:
Độ dinh dưỡng của phân lân được đánh giá bằng hàm lượng của P2O5
Câu 3:
Chọn đáp án A
Phương pháp giải:
Xét 2 trường hợp:
TH1: Ca(OH)2 dư, kết tủa chưa bị hòa tan
TH2: Kết tủa bị hòa tan một phần
Giải chi tiết:
TH1: Ca(OH)2 dư, kết tủa chưa bị hòa tan
BTNT "C": nCO2 = nCaCO3 = 0,1 mol
=> VCO2 = 2,24 lít
TH2: Kết tủa bị hòa tan một phần
BTNT "Ca" => nCa(HCO3)2 = nCa(OH)2 – nCaCO3 = 0,2 – 0,1 = 0,1 mol
BTNT "C" => nCO2 = nCaCO3 + 2nCa(HCO3)2 = 0,1 + 2.0,1 = 0,3 mol
=> VCO2 = 6,72 lít
Câu 5:
Chọn đáp án C
Phương pháp giải:
Do Fe dư nên tạo thành muối Fe2+
Sử dụng định luật bảo toàn e: 2nFe = 3nNO => nNO = ?
Giải chi tiết:
Do Fe dư nên tạo thành muối Fe2+
nFe = (20 – 3,2)/56 = 0,3 mol
BTe ta có: 2nFe = 3nNO => nNO = 2.0,3/3 = 0,2 mol
=> V = 4,48 lít
Câu 6:
Chọn đáp án A
Các chất vừa tác dụng với NaOH và HCl là: Al, NaHCO3, (NH4)2CO3, Al2O3, Zn
Câu 8:
Chọn đáp án D
P trắng được bảo quản bằng cách ngâm trong nước
Câu 9:
Chọn đáp án B
Câu 10:
Chọn đáp án A
Phương pháp giải:
Chỉ những oxit của KL đứng sau Al trong dãy hoạt động hóa học bị khử bởi CO hoặc H2
Giải chi tiết:
CuO và Fe2O3 bị CO khử ở nhiệt độ cao theo PTHH:
CuO + CO → Cu + CO2
Fe2O3 + 3CO → 2Fe + 3CO2
Như vậy chất rắn thu được sau phản ứng gồm: Al2O3, Cu, MgO, Fe
Câu 12:
Chọn đáp án B
Công thức phân tử của đạm urê là: (NH2)2CO.
Câu 13:
Chọn đáp án B
Phương pháp giải:
Trong một dung dịch ta luôn có: [H+][OH-] = 10-14
- Tính [H+]
- Tính pH = -log[H+]
+ pH = 7: môi trường trung tính
+ pH > 7: môi trường kiềm
+ pH < 7: môi trường axit
Giải chi tiết:
[H+] = 10-14/[OH-] = 10-14/(2,5.10-10) = 4.10-5 mol/l
=> pH = -log[H+] = 4,4 < 7
=> Môi trường axit
Câu 14:
Chọn đáp án A
Phương pháp giải:
Ghi nhớ một số KL bị thụ động với HNO3 đặc nguội như Al, Fe, Cr
Giải chi tiết:
Al, Fe là những kim loại bị thụ động với HNO3 đặc nguội
Câu 16:
Chọn đáp án B
Phương pháp giải:
Áp dụng định luật bảo toàn điện tích: ∑n(+) = ∑n(-)
Giải chi tiết:
Áp dụng định luật bảo toàn điện tích cho dung dịch X ta có:
nNa+ + 2nMg2+ = nCl- + 2nSO42-
=> a + 2b = c + 2d
Câu 17:
Chọn đáp án C
Khi cho từ từ (NH4)2SO4 vào dung dịch Ba(OH)2 có phản ứng hóa học xảy ra theo phương trình sau:
(NH4)2SO4 + Ba(OH)2 → BaSO4↓ + 2NH3↑ + 2H2O
Câu 18:
Chọn đáp án D
Phương pháp giải:
a = nOH- : nH3PO4
+ a > 3 => Bazo dư, sau phản ứng thu được muối PO43- và OH-
+ a = 3 => thu được muối PO43-
+ 2< a < 3 => thu được HPO42- và PO43-
+ a = 2 => thu được HPO42-
+ 1 < a < 2 => thu được HPO42- và H2PO4-
+ a = 1 => thu được H2PO4-
+ a < 1 => axit dư, sau phản ứng thu được H2PO4-và H+
Giải chi tiết:
nNaOH = 0,5 mol
nH3PO4 = 0,4 mol
1 < nNaOH : nH3PO4 = 0,5:0,4 = 1,25 < 2
=> Tạo thành 2 muối: NaH2PO4 (x mol) và Na2HPO4 (y mol)
BT “Na”: x + 2y = nNaOH = 0,5
BT “P”: x + y = nH3PO4 = 0,4
=> x = 0,3 và y = 0,1
mNaH2PO4 = 0,3.120 = 36 (g)
mNa2HPO4 = 0,1.142 = 14,2 (g)
Câu 19:
Viết phương trình hóa học theo sơ đồ sau, ghi rõ điều kiện (nếu có):
(1) N2 + O2 2NO
(2) 2NO + O2 → 2NO2
(3) 4NO2 + O2 + 2H2O → 4HNO3
(4) 6HNO3 + Fe2O3 → 2Fe(NO3)3 + 3H2O
Câu 20:
Khi cho 3,32 gam hỗn hợp Fe và Cu tác dụng hoàn toàn với 400 ml dung dịch HNO3 0,5M thu được 1,008 lít khí NO duy nhất (đktc).
a) Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu ?
Phương pháp giải:
Dựa vào dữ kiện đề bài lập hệ phương trình:
+ Phương trình về khối lượng
+ Phương trình về bảo toàn e
Giải chi tiết:
nHNO3 bđ = 0,4.0,5 = 0,2 mol
nNO = 1,008/22,4 = 0,045 mol
Đặt nFe = x mol và nCu = y mol
a) Khối lượng của hỗn hợp là 3,32 gam nên ta có: 56x + 64y = 3,32 (1)
Ta có quá trình cho – nhận e:
Fe0 – 3e → Fe+3
x → 3x (mol)
Cu0 – 2e → Cu+2
y → 2y (mol)
N+5 + 3e → N+2
0,135←0,045 (mol)
Theo định luật bảo toàn e ta có: 3x + 2y = 0,135 (2)
Từ (1) và (2) ta có hệ phương trình:
Câu 21:
b) Tính nồng độ mol của axit HNO3 trong dung dịch sau phản ứng ? Biết thể tích dung dịch không đổi.
b) BT “N”: nHNO3 sau pư = nHNO3 bđ – 3nFe(NO3)3 – 2nCu(NO3)2 – nNO
= 0,2 – 3.0,025 – 2.0,03 – 0,045 = 0,02 mol
=> CM HNO3 sau pư = n/V = 0,02/0,4 = 0,05 M
