Bộ 30 đề thi học kì 1 Hóa 11 có đáp án (Đề 26)
-
4709 lượt thi
-
40 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 1:
Chọn đáp án A
X là khí có màu nâu đỏ → X là NO2
Câu 2:
Chọn đáp án A
Phương pháp giải:
Đặt số oxi hóa của M khi phản ứng với HNO3 là +n (1 ≤ n ≤ 3)
QT cho - nhận e:
M → M+n + n e
2N+5 + 10e → N2
Bảo toàn electron: n.nM = 10nN2 => nM => Mối liên hệ giữa R và n.
Biện luận với n = 1, 2, 3 để tìm giá trị R, n phù hợp.
Giải chi tiết:
Đặt số oxi hóa của M khi phản ứng với HNO3 là +n (1 ≤ n ≤ 3)
QT cho - nhận e:
M → M+n + n e
2N+5 + 10e → N2
Bảo toàn e: n.nM = 10.nN2 → → M = 12n
Với n = 2 và M = 24 (Mg) thỏa mãn.
Câu 3:
Chọn đáp án A
Phương pháp giải:
Một số hidroxit lưỡng tính thường gặp: Al(OH)3, Zn(OH)2, Cr(OH)3
Giải chi tiết:
Hợp chất có tính lưỡng tính là Al(OH)3.
Câu 4:
Chọn đáp án D
Phương pháp giải:
Giải chi tiết:
Phương trình hoá học sai là: Fe2O3 + 8HNO3 → 2Fe(NO3)3 + 2NO2 ↑ + 4H2O
Sửa lại: Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
Câu 5:
Chọn đáp án D
Phương pháp giải:
Xét tỉ lệ nNaOH : nH3PO4 = a
NaOH + H3PO4 → NaH2PO4 + H2O
2NaOH + H3PO4 → Na2HPO4 + 2H2O
3NaOH + H3PO4 → Na3PO4 + 3H2O
+ Nếu a ≤ 1 thì phản ứng chỉ tạo ra NaH2PO4
+ Nếu 1 < a < 2 thì phản ứng tạo 2 muối NaH2PO4 và Na2HPO4
+ Nếu a = 2 thì phản ứng chỉ tạo Na2HPO4
+ Nếu 2 < a < 3 thỉ phản ứng tạo 2 muối Na2HPO4 và Na3PO4
+ Nếu a ≥ 3 nên phản ứng tạo muối Na3PO4
Giải chi tiết:
nNaOH = 1,1 mol và nH3PO4 = 0,4 mol
Ta thấy: nNaOH : nH3PO4 = 2,75 nên phản ứng tạo 2 muối Na3PO4 và Na2HPO4
3NaOH + H3PO4 → Na3PO4 +3 H2O
3x x x mol
2NaOH + H3PO4 → Na2HPO4 + 2H2O
2y y y mol
Ta có:
Câu 6:
Chọn đáp án A
Phương pháp giải:
X có hai khí không màu không hóa nâu ngoài không khí và MX = 37,6 nên X có 2 khí là N2 và N2O
→ Số mol N2O và N2
Nếu phản ứng không tạo ra NH4+:
QT nhận e: 2N+5 + 8e → 2N+1 2N+5 + 10e → N2
→ nNO3 (muối) = ne nhận = 8nN2O + 10nN2
→ mmuối = mKL + mNO3(muối) ≠ mmuối thực tế
=> Phản ứng có tạo muối NH4+
Đặt số mol của NH4NO3 là x mol
QT nhận e:
2N+5 + 8e → 2N+1
2N+5 + 10e → N2
N+5 + 8e → N-3
Bảo toàn e có ne nhận = ne nhường = nNO3(muối kim loại)
→ mmuối = mKL + mNH4NO3 + mNO3 (kim loại) = 174,04 → x
Bảo toàn nguyên tố N: nHNO3 = nNO3(muối kim loại) + 2nNH4NO3 + 2nN2 + 2nN2O
Giải chi tiết:
X có hai khí không màu không hóa nâu ngoài không khí và MX = 37,6 nên X có 2 khí là N2 (a mol) và N2O (b mol)
Ta có: a + b = 0,25 và 28a + 44b = 0,25.37,6 => a = 0,1 và b = 0,15
Nếu phản ứng không tạo ra NH4+:
QT nhận e:
2N+5 + 8e → 2N+1
2N+5 + 10e → N2
→ nNO3 (muối) = ne nhận = 8nN2O + 10nN2 = 8.0,15 + 10.0,1 = 2,2 mol
→ mmuối = mKL + mNO3(muối) = 29 + 2,2.62 = 165,4 gam ≠ 174,04 gam
=> Phản ứng có tạo muối NH4+
Đặt số mol của NH4NO3 là x mol
QT nhận e:
2N+5 + 8e → 2N+1 (N2O)
2N+5 + 10e → N2 (N2)
N+5 + 8e → N-3 (NH4+)
Bảo toàn e: ne nhận = ne nhường = nNO3(muối kim loại) = 8nN2O + 10nN2 + 8nNH4+ = 8x + 2,2 (mol)
→ mmuối = mKL + mNH4NO3 + mNO3 (kim loại) → 29 + 80x + 62(8x + 2,2) = 174,04 → x = 0,015
Bảo toàn nguyên tố N: nHNO3 = nNO3(muối kim loại) + 2nNH4NO3 + 2nN2 + 2nN2O = 2,85 mol
→ V = 2,85 : 1,5 = 1,9 lít
Câu 7:
Cho các phản ứng sau:
(1) 2NH3 + H2SO4 → (NH4)2SO4.
(2) 4NH3 + 3O2 → 2N2 + 6H2O.
(3) 2NH3 + 3Cl2 → N2 + 6HCl.
(4) 3NH3 + 3H2O + Al(NO3)3 → Al(OH)3 +3NH4NO3.
(5) 4NH3 + 5O2 → 4NO + 6H2O.
(6) 2NH3 + 3CuO → 3Cu + 3N2 + 3H2O
Các phản ứng trong đó NH3 có tính khử là
Chọn đáp án C
Phương pháp giải:
Chất khử là chất nhường electron → Số oxi hóa tăng
Giải chi tiết:
(1) sai vì số oxi hóa của nguyên tố N không đổi (trước và sau pư đều là -3)
(2) đúng vì N-3 → N0
(3) đúng vì N-3→ N0
(4) sai vì số oxi hóa của nguyên tố N không đổi (trước và sau pư đều là -3)
(5) đúng vì N-3 → N+2
(6) đúng vì N-3 → N0
Câu 8:
Chọn đáp án C
Phương pháp giải:
Giải chi tiết:
Dùng dd AgNO3:
+ Kết tủa vàng => Na3PO4
PTHH: AgNO3 + H3PO4 → Ag3PO4
+ Không hiện tượng => NaNO3
Câu 9:
Chọn đáp án B
Phương pháp giải:
CO chỉ khử được các oxit của KL đứng sau Al trong dãy hoạt động hóa học.
Giải chi tiết:
CO chỉ khử được các oxit của KL đứng sau Al trong dãy hoạt động hóa học.
Như vậy, khi dẫn luồng khí CO dư qua ống sứ chứa hỗn hợp Al2O3, CuO, MgO, Fe2O3 đun nóng các phản ứng xảy ra là:
3CO + Fe2O3 3CO2 + 2Fe
CO + CuO CO2 + Cu
Al2O3 và MgO không phản ứng
→ Chất rắn thu được sau phản ứng gồm: Fe, Cu, MgO, Al2O3
Câu 10:
Chọn đáp án D
Phương pháp giải:
Bảo toàn điện tích: Trong một dung dịch ta luôn có n(+) = n(-)
Giải chi tiết:
Áp dụng định luật bảo toàn điện tích: n(+) = n(-) => nNH4+ + 2nMg2+ = 2nSO42- + nHCO3- => a + 2b = 2c + d
Câu 11:
Chọn đáp án B
PTHH: NH4NO2 N2 + H2O → Khí X là N2
Câu 12:
Chọn đáp án C
Phương pháp giải:
Theo Arenius, dung dịch có tính axit là dung dịch có khả năng phân li ra ion H+.
Giải chi tiết:
Ta có: H2SO4 → 2H+ + SO42-
→ Theo thuyết Arenius thì H2SO4 phân li ra H+ nên H2SO4 là axit.
Câu 13:
Chọn đáp án D
Tác nhân chủ yếu gây "hiệu ứng nhà kính" là do sự tăng nồng độ trong khí quyển của CO2.
Câu 14:
Chọn đáp án C
Phương pháp giải:
Cách chuyển đổi các phương trình phân tử sang phương trình ion rút gọn:
+ Chuyển tất cả các chất vừa dễ tan, vừa điện li mạnh thành ion, các chất khí, kết tủa, điện li yếu để nguyên dưới dạng phân tử thu được phương trình ion đầy đủ.
+ Lược bỏ những ion không tham gia phản ứng ta được phương trình ion rút gọn.
Giải chi tiết:
Phương trình ion thu gọn ứng với phản ứng trên là: 2H+ + CO32- → CO2 + H2O.
Câu 15:
Tiến hành các thí nghiệm sau:
1. Cho dung dịch NH3 vào dung dịch AlCl3.
2. Cho dung dịch AgNO3 vào dung dịch Na3PO4.
3. Cho dung dịch AgNO3 vào dung dịch H3PO4.
4. Cho dung dịch NaOH cho đến dư vào dung dịch Ca(HCO3)2.
5. Cho dung dịch (NH4)2SO4 vào dung dịch NaOH đun nhẹ.
6. Cho dung dịch (NH4)2SO4 vào dung dịch Ba(OH)2 đun nhẹ.
7. Cho dung dịch Fe2(SO4)3 vào dung dịch Ba(OH)2.
8. Cho dung dịch H2SO4 vào dung dịch Ba(HCO3)2.
Sau khi kết thúc thí nghiệm, số trường hợp thu được kết tủa là
Chọn đáp án C
Phương pháp giải:
Giải chi tiết:
1. 3NH3 + AlCl3 + 3H2O → 3NH4Cl + Al(OH)3 → Kết tủa Al(OH)3
2. AgNO3 + Na3PO4 → Ag3PO4 + NaNO3 → Kết tủa Ag3PO4
3. AgNO3 + H3PO4 → không phản ứng
4. 2NaOH + Ca(HCO3)2 → Na2CO3+ CaCO3 + H2O → Kết tủa CaCO3
5. (NH4)2SO4 + 2NaOH → 2Na2SO4 + 2NH3 + H2O
6. (NH4)2SO4 + Ba(OH)2 → BaSO4 + 2NH3 + H2O → Kết tủa BaSO4
7. Fe2(SO4)3 + 3Ba(OH)2 → 3BaSO4 + 2Fe(OH)3 → Kết tủa BaSO4 và Fe(OH)3
8. H2SO4 + Ba(HCO3)2 → BaSO4 + 2H2O + 2CO2 → Kết tủa BaSO4
Sau khi kết thúc thí nghiệm, số trường hợp thu được kết tủa là 6
Câu 16:
Chọn đáp án C
Phương pháp giải:
- Au không tác dụng với cả HNO3 đặc nguội và đặc nóng
- Fe, Al, Cr không tác dụng với HNO3 đặc nguội vì bị thụ động
Giải chi tiết:
Kim loại tác dụng được với dung dịch HNO3 đặc nguội là Mg, Cu, Ag, Zn, Ca.
Câu 17:
Chọn đáp án D
Phương pháp giải: pH = -log[H+]
Giải chi tiết:
Ta có: pH = 2 → [H+] = 0,01 M → nH+ = 0,6.0,01 = 0,006 mol
H2SO4 → 2H+ + SO42-
0,003 ← 0,003 (mol)
→ mH2SO4 = 0,003.98 = 0,294 gam
Câu 18:
Cho phương trình phản ứng: Mg + HNO3 → Mg(NO3)2 + NO + H2O.
Tổng hệ số cân bằng (số nguyên tối giản) của các chất trong phản ứng trên là
Chọn đáp án C
Phương pháp giải:
Cân bằng phương trình oxi hóa - khử theo phương pháp thăng bằng electron.
Giải chi tiết:
3Mg + 8HNO3 → 3Mg(NO3)2 + 2NO + 4H2O.
Tổng hệ số cân bằng (số nguyên tối giản) của các chất trong phản ứng trên là 20.
Câu 19:
Chọn đáp án A
Phương pháp giải:
Vì HNO3 và NaOH đều là chất điện li mạnh nên ta có: nH+ = nHNO3 và nOH- = nNaOH
PT ion: OH- + H+ → H2O
Tính theo PT ion.
Giải chi tiết:
Vì HNO3 và NaOH đều là chất điện li mạnh nên ta có: nH+ = nHNO3 = 0,02 mol và nOH- = nNaOH = 0,06 mol
PTHH: OH- + H+ → H2O
Bđ: 0,02 0,06 mol
Pư: 0,02 → 0,02 mol
Sau: 0 0,04 mol
→ [OH-] = 0,04 : 0,4 = 0,01 mol → pOH = - log[OH-] = 2 → pH = 14 - pOH = 12
Câu 20:
Chọn đáp án B
Phương pháp giải:
Na3PO4 là chất điện li mạnh nên khi hòa tan vào nước phân li hoàn toàn thành ion.
Viết phương trình phân li của Na3PO4. Từ nồng độ của Na3PO4 suy ra nồng độ Na+ và PO43-.
Giải chi tiết:
Na3PO4 là chất điện li mạnh nên khi hòa tan vào nước phân li hoàn toàn thành ion.
PT phân li: Na3PO4 → 3Na+ + PO43-
1 → 3 → 1 (M)
Vậy [Na+] = 3M và [PO43-] = 1M
Câu 21:
Chọn đáp án C
Phương pháp giải:
Giải chi tiết:
Ca(OH)2 có thể phản ứng với CO2 trong không khí tạo CaCO3 lấp đầy những lỗ nhỏ li ti đó.
PTHH: Ca(OH)2 + CO2 → CaCO3 ↓ + H2O.
Câu 22:
Chọn đáp án B
Phương pháp giải:
Từ tỉ lệ mol và khối lượng hỗn hợp ta tính được số mol của Zn, Mg.
X + NaNO3 + NaHSO4 → muối trung hòa + khí Z
Khí Z chứa khí không màu hóa nâu là NO. Dựa vào tỉ khối của Z so với H2 suy ra khí còn lại là H2
→ tìm số mol từng khí trong Z
Các bán phản ứng:
4H+ + NO3- + 3e → NO + 2H2O Zn → Zn+2+ 2e
2H+ + 2e → H2 Mg → Mg+2 + 2e
So sánh: ne nhường = 2nZn + 2nMg và ne nhận = 3nNO + nH2 nếu bằng thì không tạo NH4+
Nếu e nhường nhiều hơn e nhận thì còn phản ứng tạo ra NH4+: 10H+ + NO3- + 8e → NH4++ 3H2O → nNH4+
Bảo toàn H+ tìm số mol NaHSO4
Bảo toàn N thì tìm nNaNO3
Giải chi tiết:
Đặt nZn = x mol và nMg = y mol thì ta có hệ phương trình sau:
X + NaNO3 + NaHSO4 → muối trung hòa + khí Z
Xét khí Z có nZ = 0,21 mol và Z có 1 khí không màu hóa nâu ngoài không khí → Z có khí NO
Vì MZ = 13.2 = 26 < MNO nên Z còn 1 khí không màu có M < 26 → khí này là H2
Ta có:
Các bán phản ứng:
4H+ + NO3- + 3e → NO + 2H2O Zn → Zn+2+ 2e
2H+ + 2e → H2 Mg → Mg+2 + 2e
Vì ne nhường = 2nZn + 2nMg = 2.0,3 + 2.0,18 = 0,96 mol > ne nhận = 3nNO + nH2 = 3.0,18 + 2.0,03 = 0,6 mol
→ còn phản ứng tạo ra NH4+: 10H+ + NO3- + 8e → NH4++ 3H2O
→ nNH4+ = (0,96 - 0,6) : 8 = 0,045 mol
Vì dung dịch thu được toàn muối trung hòa nên: nNaHSO4 = nH+phản ứng = 4.0,18 + 2.0,03 + 10.0,045 = 1,23 mol
Bảo toàn N: nNaNO3 = nNH4+ + nNO = 0,045 + 0,18 = 0,225 mol
→ Dung dịch thu được sau phản ứng có
→ mmuối = mion = 176,175 gam
→ mmuối gần nhất với 176 gam
Câu 23:
Chọn đáp án C
Phương pháp giải:
Bảo toàn điện tích: 2nFe2+ + 3nAl3+ = nCl- + 2nSO42-
Giải chi tiết:
Bảo toàn điện tích: 2nFe2+ + 3nAl3+ = nCl- + 2nSO4 2- → 2.0,1 + 3.0,2 = 0,3 + 2x → x = 0,25
Câu 24:
Chọn đáp án A
Phương pháp giải:
Bảo toàn điện tích: nNa+ + 2nMg2+ = nCl- + nNO3-
Khối lượng muối sau khi cô cạn: mmuối = ∑mion
Giải chi tiết:
Bảo toàn điện tích: nNa+ + 2nMg2+ = nCl- + nNO3- → 0,3 + 2.0,1 = 0,2 + x → x = 0,3 mol
Ta có mmuối = ∑mion = 0,3.23 + 0,1.24 + 0,2.35,5 + 0,3.62 = 35 gam
Câu 25:
Các hình vẽ bên dưới mô tả một số phương pháp thu khí thường tiến hành ở phòng thí nghiệm. Cho biết từng phương pháp (1), (2), (3) có thể áp dụng để thu được khí nào trong các khí sau: O2, Cl2, HCl, NH3, SO2, H2(biết rằng một chất khí có thể thu bằng nhiều phương pháp)?
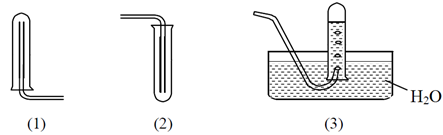
Chọn đáp án B
Phương pháp giải:
Một số cách thu khí trong phòng thí nghiệm:
- Thu bằng cách đẩy không khí úp bình với khí nhẹ hơn không khí
- Thu bằng đẩy không khí ngửa bình với khí nặng hơn không khí
- Thu bằng cách đẩy nước với các khí cần không tan trong nước/không phản ứng với nước
Giải chi tiết:
(1) thu bằng cách đẩy không khí úp bình với khí nhẹ hơn không khí
(2) thu bằng đẩy không khí ngửa bình với khí nặng hơn không khí
(3) thu bằng cách đẩy nước nên khí cần không tan trong nước và không phản ứng với nước
A. sai vì khí thu bình (1) là O2 nặng hơn không khí
B. đúng
C. sai vì khí thu bằng cách (3) là NH3 và HCl tan nhiều trong nước
D. sai vì khí thu bằng cách (3) có HCl tan nhiều trong nước
Câu 26:
Chọn đáp án D
Phương pháp giải:
Muối axit là muối chứa nguyên tử H có khả năng phân li ra ion H+.
Giải chi tiết:
Muối axit là muối Ca(HCO3)2
Câu 27:
Chọn đáp án A
A. đúng
B. sai vì tạo ra 2H+ không phải H2+
C. sai vì tạo ra 3Na+ không phải Na3+
D. sai vì tạo ra 2Cl- không phải Cl2-
Câu 28:
Chọn đáp án A
Phương pháp giải:
Từ CM NaOH → [OH-] → pOH = - log[OH-] → pH = 14 - pOH
Giải chi tiết:
NaOH là chất điện li mạnh, tan trong nước điện li hoàn toàn thành ion:
NaOH → Na+ + OH-
0,01M → 0,01M
→ [OH- ] = 0,01M → pOH = -log[OH-] = 2
→ pH = 14 - pOH = 14 - 2 = 12
Câu 29:
Chọn đáp án A
Phương pháp giải:
Tính theo PTHH: 2Cu(NO3)2 2CuO + 4NO2 + O2
Giải chi tiết:
Ta có: nkhí = 0,24 mol
PTHH: 2Cu(NO3)2 2CuO + 4NO2 + O2
x 2x 0,5x
→ nkhí = nNO2 + nO2 → 2x + 0,5x = 0,24 → x = 0,096 mol
→ mCu(NO3)2 = 188.0,096 = 18,048 gam
Câu 30:
Chọn đáp án C
Phương pháp giải:
Viết các quá trình cho - nhận electron. Áp dụng định luật bảo toàn electron.
Giải chi tiết:
QT cho - nhận electron:
Al → Al3+ + 3e N+5 + 3e → N+2
Áp dụng định luật bảo toàn e: 3.nAl = 3.nNO
→ nAl = nNO = 0,15 mol
→ m = 0,15.27 = 4,05 gam
Câu 31:
Chọn đáp án B
Phương pháp giải:
Nhiệt phân muối nitrat M(NO3)n
- Nếu M là [K, ..., Ca] thì nhiệt phân thu được muối M(NO2)n và O2
- Nếu M là [Mg, ..., Cu] thì nhiệt phân thu được M2On, NO2, O2
Ngoại lệ: 2Fe(NO3)2 → Fe2O3 + 4NO2 + 0,5O2
- Nếu M là [Ag, ...] thì nhiệt phân thu được M, NO2, O2
Giải chi tiết:
Khi nhiệt phân hoàn toàn muối KNO3 thu được sản phẩm là KNO2 và O2.
PTHH: 2KNO3 2KNO2 + O2
Câu 32:
Chọn đáp án B
Các mức số oxi hóa có thể có của cacbon là: -4; 0; +2; +4.
Câu 33:
Cho các sơ đồ phản ứng sau:
1. C + O2 CO2. 4. C + H2 CH4.
2. C + CuO Cu + CO. 5. C + H2SO4 (đặc) SO2 + CO2 + H2O.
3. C + Ca CaC2. 6. C + H2O CO + H2.
Các phản ứng cacbon thể hiện tính oxi hóa là
Chọn đáp án B
Phương pháp giải:
Chất thể hiện tính oxi hóa là chất nhận electron (số oxi hóa giảm).
Giải chi tiết:
(1) sai vì số oxi hóa của C tăng từ 0 lên +4
(2) sai vì số oxi hóa của C tăng từ 0 lên +2
(3) đúng vì số oxi hóa của C giảm từ 0 xuống -1
(4) đúng vì số oxi hóa của C giảm từ 0 xuống -4
(5) sai vì số oxi hóa của C tăng từ 0 lên +4
(6) sai vì số oxi hóa của C tăng lên từ 0 đến +2
Câu 34:
Chọn đáp án D
Phương pháp giải:
Bảo toàn e: 3nNO = 2nCu → mCuO
Giải chi tiết:
Ta có: nNO = 0,3 mol
Bảo toàn e: 3nNO = 2nCu → nCu = 0,3.3 : 2 = 0,45 mol
→ mCuO = mhỗn hợp - mCu = 32 - 0,45.64 = 3,2 gam
Câu 35:
Chọn đáp án B
Phương pháp giải:
Chất điện li mạnh là chất là axit mạnh, bazo mạnh và hầu hết các muối.
Giải chi tiết:
Chất điện li mạnh là chất là axit mạnh, bazo mạnh và hầu hết các muối.
Trong các chất đề bài cho thì NaCl là một chất điện li mạnh.
Câu 36:
Chọn đáp án A
Phương pháp giải:
Bảo toàn nguyên tố Fe.
Giải chi tiết:
nFe2O3 = 0,03 mol
Bảo toàn Fe ta có: nFe = 2nFe2O3 = 0,06 mol → m = 0,06.56 = 3,36 gam
Câu 37:
Chọn đáp án D
Phương pháp giải:
Giải chi tiết:
Chất khí độc dẫn đến tử vong nhẹ hơn không khí là CO do CO có ái tính với hemoglobin trong máu mạnh hơn, ngăn cản hemoglobin vận chuyển oxi trong máu.
→ Biện pháp: Không dùng trong phòng kín mà phải để cửa thoáng.
Câu 38:
Chọn đáp án B
HF có thể ăn mòn SiO2 là thành phần chính của thủy tinh nên được dùng để khắc chữ lên thủy tinh.
PTHH: SiO2 + 4HF → SiF4 + 2H2O.
Câu 39:
Chọn đáp án D
Phương pháp giải:
Chất không dẫn điện là chất khi hòa tan trong nước không điện li ra ion.
Chất điện li gồm có axit, bazo, muối.
Giải chi tiết:
Chất không dẫn điện khi hòa tan trong nước là C6H12O6 (glucozơ).
Câu 40:
Chọn đáp án A
Phương pháp giải:
Tính theo PTHH: N2 + 3H2 2NH3
→ Tỉ lệ về thể tích tương tự về số mol → VNH3 lý thuyết
H = Vtt : Vtt . 100% → Vtt
Giải chi tiết:
PTHH: N2 + 3H2 2NH3
Lý thuyết 10 → 20 lít
Thể tích NH3 thực tế thu được là: VNH3 = 20.(75/100) = 15 lít
