Trắc nghiệm chuyên đề Hoá 12 Chủ đề 5: Bài toán về phản ứng thuỷ phân
-
336 lượt thi
-
13 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
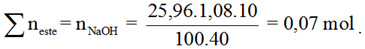
Phương trình phản ứng:
CH3COOC2H5 + NaOH → CH3COONa + C2H5OH (1)
HCOOC2H5 + NaOH → HCOONa + C2H5OH (2)
Theo giả thiết và các phản ứng ta có hệ phương trình :
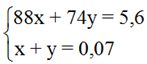
⇒ x = 0,03 và y = 0,04.
⇒ % mCH3COOC2H5 = 47,14%.
Câu 2:
Đặt công thức của X là RCOOR’.
Theo giả thiết ta có :
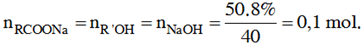
MR’OH = R’+ 17 = 32 R’= 15 (CH3–) và MRCOONa = R + 67 = 96
R = 29(C2H5–).
Vậy công thức của X là C2H5COOCH3.
Đáp án B.Câu 3:
Đáp án C
Este có công thức dạng RCOOR’, muối tạo thành là RCOONa.
Phương trình phản ứng :
RCOOR’ + NaOH → RCOONa + R’OH
Vì số mol este bằng số mol muối, nên tỉ lệ về khối lượng của chúng cũng là tỉ lệ về khối lượng mol.
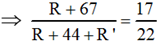
⇒ 17R’ - 5R = 726 (1).
Mặt khác Meste = 4.22 = 88 ⇒ R + 44 + R’ = 88 ⇒ R + R’ = 44 (2).
Từ (1) và (2) ta có : R = 1 (H-); R’ = 43 (C3H7-). Vậy tên este là iso-propyl fomat
Câu 4:
Ta có: nCH3COOC2H5 = 5,5/88 = 0,1 (mol)
Và nNaOH ban đầu = 0,2 .0,2 = 0,04 (mol)
Este dư, NaOH hết
CH3COOC2H5 + NaOH → CH3COONa + C2H5OH (1)
Từ (1) ⇒ nCH3 COONa = nNaOH = 0,04 (mol)
mCH3 COONa = 0,04 .82 = 3,28(gam)
Câu 5:
Đáp án D
Theo giả thiết ta cho biết X là este hai chức của etylen glicol và axit hữu cơ đơn chức; X có 4 nguyên tử O và có 5 nguyên tử C.
Vậy công thức của X là : HCOOC2H4OOCCH3
Phương trình phản ứng :
HCOOC2H4OOCCH3 + 2NaOH → HCOONa + CH3COONa + C2H4(OH)2
Theo giả thiết và (1) ta có : nHCOOC2H4OOCCH3 = 1/2 nNaOH = 1/2 . 10/40 = 0,125 mol
Vậy mX = 0,125.132 = 16,5 gam.
Câu 6:
Đáp án: A
Gọi công thức của este no, đơn chức là CnH2nO2
Khi xà phòng hóa thì : neste = nNaOH
neste = 0,3 .0,5 = 0,15 (mol) ⇒ Meste = 17,4/0,15 = 116
14n + 32 = 116 ⇒ n = 6Câu 7:
Đáp án: C
Gọi công thức este đơn chức X là RCOOR'
Ta có: nKOH = 0,1*1 = 0,1(mol)
RCOOR' + KOH → RCOOK + R'OH (1)
Từ (1) ⇒ nR'OH = 0,1(mol) ⇒ MR'OH = 4,6/0,1 = 46
⇒ R' = 29 ⇒ C2H5-
Y: C2H5OH ⇒ X là CH3COOC2H5( vì MX = 88) : etyl axetatCâu 8:
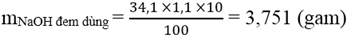
⇒ ME = 88 gam ⇔ R + 44 + R’ = 88 ⇒ R + R’ = 44
- Khi R = 1 ⇒ R’ = 43 (C3H7) ⇒ CTCT (E): HCOOC3H7(propyl fomiat)
- Khi R = 15 ⇒ R’ = 29 ⇒ CTCT (E): CH3COOC2H5 (etyl axetat)
Câu 9:
Đáp án: C
Gọi công thức của este no, đơn chức là CnH2nO2
⇒ neste = nNaOH
⇒ neste = 0,3 x 0,5 = 0,15 (mol) ⇒ Meste = 17,4/0,15 = 116
⇒ 14n + 32 = 116 ⇒ n = 6
Vậy công thức phân tử của este là C6H12O2.Câu 10:
Đáp án: A
o-CH3COO–C6H4–COOH + 3KOH → CH3COOK + o-KO–C6H4–COOK + H2O (1)
⇒ nKOH = 3.no-CH3COO–C6H4–COOH = 3 . 43,2/180 = 0,72 molCâu 11:
Đáp án: A
nEste = n = 0NaOH,3 mol; mmuối theo lí thuyết = 20,492/94 . 100 = 21,8 gam.
Meste = 22,2/0,3 = 74 gam/mol ⇒ công thức phân tử của 2 este có dạng C3H6O2. Vậy công thức cấu tạo của hai este là HCOOC2H5 và CH3COOCH3.
Gọi x là mol của HCOOC2H5 và y là số mol của CH3COOCH3. Ta có hệ
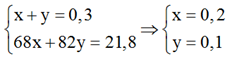
Câu 12:
Đáp án: D
Đặt công thức trung bình của lipit X là C3H5(OOCR)3.
C3H5(OOCR)3 + 3NaOH → C3H5(OH)3 + 3RCOONa (1)
Theo giả thiết ta có
⇒ Do đó trong 94,6 gam chất rắn có 0,1 mol NaOH dư và 0,3 mol RCOONa.
⇒ 0,1.40 + (R + 67).0,3 = 94,6 ⇒ R = 235 ⇒ R là C17H31–
Câu 13:
Đáp án: D