Bộ đề thi học kì 2 Hóa 12 có đáp án (Mới nhất) - Đề số 6
-
1170 lượt thi
-
30 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Cho Fe tác dụng với hơi nước ở nhiệt độ cao hơn 5700C thì thu được sản phẩm là
Chọn đáp án D.
Câu 5:
Chọn đáp án A.
Câu 6:
Sử dụng thuốc thử là dung dịch NaOH nhận biết được 4 dung dịch vì:
- AlCl3 tạo kết tủa trắng keo tan trong kiềm dư
- FeCl3 tạo kết tủa nâu đỏ Fe(OH)3
- CuCl2 tạo kết tủa xanh Cu(OH)2
- FeCl2 tạo kết tủa trắng xanh, để trong không khí một thời gian chuyển nâu đỏ
Chọn đáp án B.
Câu 7:
Để chế tạo thép không gỉ, người ta thêm vào thành phần của thép thường kim loại
Chọn đáp án C.
Câu 8:
Hai kim loại đều phản ứng được với dung dịch CuSO4 giải phóng Cu là
Chọn đáp án D.
Câu 9:
Chọn đáp án D.
Câu 10:
Chọn đáp án C.
Câu 11:
Cho từ từ 2ml dung dịch FeCl2 vào ống nghiệm chứa 3 ml dung dịch NaOH, hiện tượng quan sát được là
Chọn đáp án C.
Câu 12:
Có thể dùng thùng nhôm để chuyên chở axit HNO3 đặc, nguội hoặc H2SO4 đặc, nguội vì
Chọn đáp án A.
Câu 18:
Nhỏ từ từ đến dư dung dịch NaOH vào ống nghiệm chứa khoảng 2ml dung dịch AlCl3. Hiện tượng xảy ra là
Chọn đáp án A.
Câu 19:
Để nhận biết 2 chất khí CO2 và SO2 ta chỉ cần dùng một thuốc thử là
SO2 làm mất màu dd brom
Chọn đáp án D.
Câu 21:
Sử dụng dung dịch NaOH:
- Có khí và kết tủa trắng keo, sau tan trong kiềm dư là Al
- Có kết tủa trắng keo, sau tan trong kiềm dư là Al2O3
- Không hiện tượng là Mg
Chọn đáp án C.
Câu 22:
Cho 1,05 gam hỗn hợp gồm hai kim loại ở 2 chu kỳ liên tiếp thuộc nhóm IIA (phân nhóm chính nhóm II) tác dụng hết với dung dịch HCl (dư), thoát ra 0,672 lít khi H2 (ở đktc). Hai kim loại đó
Gọi công thức chung của hai kim loại là X
![]()
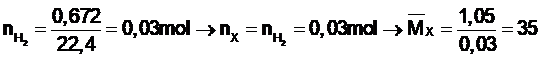
Mà hai kim loại ở 2 chu kỳ liên tiếp thuộc nhóm IIA → 2 kim loại đó là Ca và Mg
Chọn đáp án B.
Câu 23:
Cho 2,24 gam bột sắt vào 200 ml dung dịch chứa hỗn hợp gồm AgNO3 0,1M và Cu(NO3)2 0,5M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và m gam chất rắn Y. Giá trị của m là
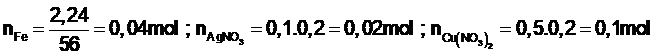
![]()
0,01←0,02 → 0,02
![]()
0,03 < 0,1 → 0,03
→ mrắn = mAg + mcu =0,02 . 108 + 0,03 . 64 = 4,08 (g)
Chọn đáp án C.
Câu 24:
Thực hiện các thí nghiệm sau:
(1) Cho bột Fe vào dung dịch AgNO3 dư.
(2) Đốt bột Fe trong O2 dư, hòa tan chất rắn sau phản ứng trong lượng vừa đủ dung dịch HCl.
(3) Nhúng nhanh Fe trong dung dịch HNO3 loãng.
(4) Nhúng nhanh Mg trong dung dịch Fe2(SO4)3.
(5) Thổi khí H2S đến dư vào dung dịch FeCl3.
(6) Đốt cháy bột Fe (dùng dư) trong khí Cl2, hòa tan chất rắn sau phản ứng trong nước cất.
Sau khi kết thúc thí nghiệm, dung dịch thu được chỉ chứa muối Fe(II) là
(1)Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe(NO3)2 + AgNO3 dư → Fe(NO3)3 + Ag
(2) 3Fe + 2O2 → Fe3O4
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O
(3) Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
Fe dư + 2Fe(NO3)3 → 3 Fe(NO3)2
(4) Mg + Fe2(SO4)3 →MgSO4 + 2FeSO4
Mg dư + FeSO4 → MgSO4 + Fe
(5) H2S + 2FeCl3 → 2FeCl2 + 2HCl + S
(6) 2Fe + 3Cl2 → 2FeCl3
Fe dư + 2FeCl3 → 3FeCl2
→ Sau khi kết thúc thí nghiệm (3) (6) chỉ thu được muối Fe(II)
Chọn đáp án D.
Câu 25:
Hòa tan hoàn toàn 14,4 kim loại M hóa trị II vào dung dịch ![]() đặc dư thu được 26,88 lit
đặc dư thu được 26,88 lit ![]() (dktc) là sản phẩm khử duy nhất. Kim loại M là:
(dktc) là sản phẩm khử duy nhất. Kim loại M là:
(*) Phương pháp: Bảo toàn electron
Bảo toàn![]()
![]() Magie
Magie
Chọn đáp án D.
Câu 26:
Cặp chất nào sau đây không cùng tồn tại trong một dung dịch
BaCl2 và Na2CO3 không cùng tồn tại trong dung dịch vì
BaCl2+ Na2CO3 → 2NaCl+ BaCO3
Chọn đáp án C.
Câu 27:
Cho 4 lọ dung dịch riêng biệt X, Y, Z, T chứa các chất khác nhau trong số 4 chất: (NH4)2CO3, NaHCO3, NaNO3, NH4NO3. Thực hiện nhận biết bốn dung dịch trên bằng dung dịch Ba(OH)2 thu được kết quả sau:
|
Chất |
X |
Y |
Z |
T |
|
Hiện tượng |
Kết tủa trắng |
Khí mùi khai |
Không hiện tượng |
Kết tủa trắng, khí mùi khai |
Nhận xét nào sau đây đúng?
X + Ba(OH)2 → Kết tủa trắng
=> X là NaHCO3.
2NaHCO3 + Ba(OH)2 → BaCO3↓ + Na2CO3 + 2H2O
• Y + Ba(OH)2 → khí mùi khai
=> Y là NH4NO3 => A sai, B sai.
2NH4NO3 + Ba(OH)2 → Ba(NO3)2 + 2NH3↑ + 2H2O
• Z + Ba(OH)2 → không hiện tượng.
=> Z là NaNO3 => C sai.
• T + Ba(OH)2 → Kết tủa trắng, khí mùi khai.
=> T là (NH4)2CO3 => D đúng.
(NH4)2CO3 + Ba(OH)2 → BaCO3↓ + 2NH3↑ + 2H2O
Chọn đáp án D.
Câu 28:
Thực hiện thí nghiệm điều chế khí X, khí X được thu vào bình tam giác theo hình vẽ sau:
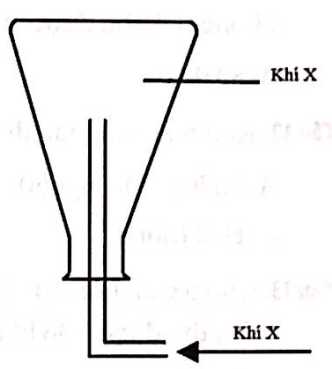
Thí nghiệm đó là:
![]()
![]()
![]()
![]()
Vì bình khí úp ngược nên khí thu được nhẹ hơn không khí (MX < 29) => X là H2.
Chọn đáp án C.
Câu 29:
Hòa tan hoàn toàn 12 gam hỗn hợp Fe, Cu (tỉ lệ mol 1:1) bằng axit HNO3, thu được V lít (đktc) hỗn hợp khí X (gồm NO và NO2) và dung dịch Y (chỉ chứa hai muối và axit dư). Tỉ khối của X đối với H2 bằng 19. Giá trị của V là:
Áp dụng sơ đồ đường chéo cho hỗn hợp NO2 và NO ta có :
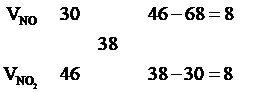
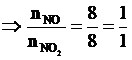
![]()
Đặt nFe = nCu = 0,1 mol.
Bảo toàn e
![]()
![]()
Chọn đáp án C.
Câu 30:
Hỗn hợp X gồm: Al, Fe3O4 và CuO, trong đó oxi chiếm 25% khối lượng. Cho 1,344 lít khí CO (đktc) đi qua m gam X nung nóng, sau một thời gian thu được chất rắn Y và hỗn hợp khí Z có tỉ khối so với H2 bằng 18. Hoà tan hoàn toàn Y trong dung dịch HNO3 loãng (dư), thu được dung dịch chứa 3,08m gam muối và 0,896 lít khí NO (ở đktc, là sản phẩm khử duy nhất). Giá trị của m gần nhất với giá trị nào sau đây:
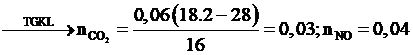
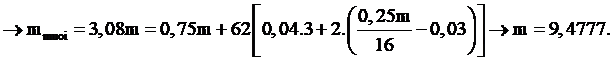
Chọn đáp án A.
