Đề kiểm tra học kì 1 Hóa 12 có đáp án (Mới nhất) (Đề 9)
-
1296 lượt thi
-
30 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Đáp án D
Ancol etylic: C2H5OH
Axit axetic: CH3COOH
Câu 2:
Số nguyên tử hiđro trong phân tử glucozơ là
Đáp án D
Công thức phân tử của glucozơ là C6H12O6.
→ Số nguyên tử hiđro trong phân tử glucozơ là 12
Câu 3:
Chất nào sau đây không có phản ứng thủy phân?
Đáp án A
Glucozơ là monosaccarit, không có phản ứng thủy phân.
Câu 4:
Glucozơ lên men thành ancol etylic theo phương trình phản ứng sau:
Để thu được 92 gam C2H5OH cần dùng m gam glucozơ. Biết hiệu suất của quá trình lên men là 60%. Giá trị của m là
Đáp án B
Khối lượng glucozơ tính theo lí thuyết là mglucozơ = 1.180 = 180 gam
Do hiệu suất phản ứng 60% → khối lượng thực mà glucozơ cần dùng là:
Câu 5:
Amin no, đơn chức, mạch hở có công thức tổng quát là
Đáp án C
Amin no, đơn chức, mạch hở có công thức tổng quát là CnH2n+3N.a
Câu 6:
Chất có tính bazơ mạnh nhất là
Đáp án C
Thứ tự tăng dần tính bazơ là: amin thơm < NH3 < amin no
Amin bậc 2 có tính bazơ mạnh hơn amin bậc 1
→ Chất có tính bazơ mạnh nhất là (CH3)2NH.
Câu 7:
Dung dịch chất nào sau đây làm quỳ tím chuyển thành màu xanh?
Đáp án C
A, B, D không làm quỳ tím đổi màu vì đều có 1 nhóm NH2 và 1 nhóm COOH
C. lysin làm quỳ chuyển sang màu xanh vì có 2 nhóm NH2 và 1 nhóm COOH
Câu 8:
Hợp chất nào dưới đây thuộc loại amino axit
Đáp án D
Amino axit là hợp chất hữu cơ tạp chất hữu cơ tạp chức mà trong phân tử chứa đồng thời nhóm amino (NH2) và nhóm cacboxyl (COOH).
→ Hợp chất thuộc loại amino axit là H2NCH2COOH
A là este, B là muối, C là amin
Câu 9:
Chất X vừa tác dụng được với axit, vừa tác dụng được với bazơ. Chất X là
Đáp án D
Glyxin: H2NCH2COOH là chất lưỡng tính, tác dụng được với cả axit và bazơ:
H2NCH2COOH + HCl → ClH3NCH2COOH
H2NCH2COOH + NaOH → H2NCH2COONa + H2O
Câu 10:
Chất nào dưới đây tạo phức màu tím với Cu(OH)2?
Đáp án C
A sai vì đipeptit không có phản ứng màu biure với Cu(OH)2
B sai vì glucozơ tạo phức màu xanh đặc trưng với Cu(OH)2 ở nhiệt độ thường.
C đúng vì từ tripeptit trở lên đều tạo phức màu tím với Cu(OH)2
D sai vì metylamin không phản ứng với Cu(OH)2
Câu 11:
Phân tử khối của peptit Ala-Gly là
Đáp án D
Phân tử khối của peptit Ala-Gly là:
(g/mol)
Câu 12:
Polime nào sau đây thuộc loại polime thiên nhiên?
Đáp án D
Polime thiên nhiên là xenlulozơ, tơ tằm, cao su thiên nhiên
Câu 13:
Chất nào sau đây không có khả năng tham gia phản ứng trùng hợp?
Đáp án D
Toluen có công thức là C6H5CH3 → không tham gia phản ứng trùng hợp vì vòng benzen chứa liên kết bội nhưng rất bền.
Câu 14:
Polime X là chất rắn trong suốt có khả năng cho ánh sáng truyền qua tốt nên được dùng chế tạo thuỷ tinh hữu cơ plexiglas. Tên gọi của X là
Đáp án C
Thủy tinh hữu cơ hay còn gọi là poli(metyl metacrylat).
Phương trình điều chế:
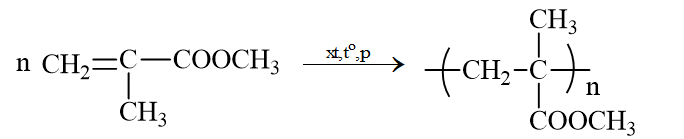
Câu 15:
PVC là chất rắn vô định hình, cách dẫn điện tốt, bền với axit, được dùng làm vật liệu cách điện, ống dẫn nước, vải che mưa,... PVC được tổng hợp trực tiếp từ monome nào sau đây?
Đáp án A
PVC là viết tắt của Poli(vinyl clorua).
→ PVC được tổng hợp từ monome vinyl clorua (CH2=CHCl).
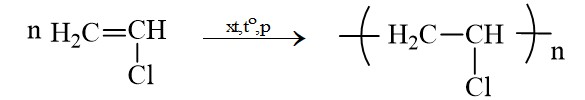
Câu 16:
Polime X có phân tử khối là 336000 và hệ số trùng hợp là 12000. Vậy X là
Đáp án A
Phân tử khối của một mắt xích trong X là đvC
→ Mắt xích là -CH2-CH2-
→ X là PE (polietilen)
Câu 17:
Cho các nhận xét sau:
(1) Tinh bột và xenlulozơ là hai đồng phân cấu tạo của nhau.
(2) Hai đồng phân amino axit của C3H7NO2 tạo ra tối đa 3 đipeptit.
(3) Khi đun nóng glucozơ (hoặc fructozơ) với dung dịch AgNO3 trong NH3 thu được Ag.
(4) Thủy phân hoàn toàn tinh bột và xenlulozơ mỗi chất chỉ cho 1 loại monosaccarit duy nhất.
(5) Nồng độ glucozơ trong máu người bình thường khoảng 5%.
(6) Tất cả các dung dịch protein đều có phản ứng màu biure.
(7) Dung dịch lòng trắng trứng có phản ứng màu biure.
Số nhận xét đúng là
Đáp án B
(1) sai vì tinh bột và xenlulozơ không phải là đồng phân cấu tạo của nhau.
(2) sai vì peptit tạo bởi -amino axit → Chỉ có 1 peptit là Ala-Ala.
(5) sai vì nồng độ glucozơ trong máu người bình thường khoảng 0,1%.
Câu 18:
Bán kính nguyên tử các nguyên tố: Na, Li, Be, B. Xếp theo chiều tăng dần là:
Đáp án A
Li và Na thuộc cùng nhóm IA và ZLi < ZNa→ Bán kính Na > Li
Li, Be và B thuộc cùng chu kỳ 2 và ZLi < ZBe < ZB → Bán kính: Li > Be > B
Chiều tăng dần bán kính: B < Be < Li < Na
Câu 19:
Cho Fe tác dụng với dung dịch HNO3 đặc, nóng thu được khí X có màu nâu đỏ. Khí X là
Đáp án D
N2: Không màu nhẹ hơn không khí
N2O: Không màu nặng hơn không khí
NO: Không màu, hóa nâu ngoài không khí
NO2: Màu nâu đỏ
Câu 20:
Câu 20:
Đáp án B
nCuO = 0,4 mol
nCO phản ứng = nO trong oxit = 0,4 mol
→ V = 0,4.22,4 = 8,96 lít
Câu 21:
Có các phản ứng như sau :
1. Fe + 2H+→ Fe2++ H2
2. Fe + Cl2→FeCl2
3. AgNO3 + Fe(NO3)2 → Fe(NO3)3 + Ag
4. Ca + FeCl2 dung dịch → CaCl2 + Fe
5. Zn + 2FeCl3 ZnCl2 + 2FeCl2
6. 3Fe dư + 8HNO3 loãng → 3Fe(NO3)2 + 2NO + 4H2O
Trong các phản ứng trên, số phản ứng viết không đúng là
Đáp án B
2. Sửa lại thành: 2Fe + 3Cl2 2FeCl3
4. Ca phản ứng với nước trong dung dịch trước
Ca + 2H2O → Ca(OH)2 + H2
Ca(OH)2 + FeCl2 dung dịch → CaCl2 + Fe(OH)2
→ Phản ứng 2,4 không đúng
Chú ý: Phản ứng 6 là gộp của 2 phản ứng:
Fe + 4HNO3→ Fe(NO3)3 + NO + 2H2O
Fe dư + 2Fe(NO3)3 → 3Fe(NO3)2
Câu 22:
Cho một mẫu hợp kim K-Na tác dụng với nước dư, thu được dung dịch X và 3,36 lít H2 (đktc). Thể tích dung dịch axit HCl 2M cần dùng để trung hòa dung dịch X là
Đáp án A
= 0,15 mol
= 2. = 0,3 mol
= 0,3 mol
→ VHCl = 0,3 : 2 = 0,15 lít = 150 ml
Câu 23:
Có 3 mẫu hợp kim: Fe - Al; K - Na; Cu - Mg. Hoá chất có thể dùng để phân biệt 3 mẫu hợp kim trên là
Đáp án A
Sử dụng NaOH để phân biệt
- Hợp kim tan một phần trong NaOH dư: Fe-Al
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
- Hợp kim tan hoàn toàn trong NaOH dư: K-Na
2K + 2H2O → 2KOH + H2
2Na + 2H2O → 2NaOH + H2
- Hợp kim không tan trong NaOH dư: Cu-Mg
Câu 24:
Đáp án C
Bào toàn nguyên tố H:
= 0,6 mol
→ mKL + mHCl = m muối +
→ 15,4 + 36,5.0,6 = m muối + 2.0,3
→ m muối = 36,7 gam
Câu 25:
Khi đốt cháy hoàn toàn một amin đơn chức X, thu được 1,344 lít khí CO2, 0,224 lít khí N2 (các thể tích khí đo ở đktc) và 1,62 gam H2O. Công thức của X là
Đáp án D
Amin đơn chức →
Số nguyên tử cacbon là: C =
Số nguyên tử hiđro là: H =
→ Công thức phân tử của amin X là C3H9N
Câu 26:
Amino axit X chứa một nhóm -NH2. Cho 15 gam X tác dụng với axit HCl (dư), thu được 22,3 gam muối khan. Công thức cấu tạo thu gọn của X là
Đáp án A
Gọi công thức của amino axit X có dạng H2N-R-(COOH)a
Bảo toàn khối lượng ta có:
Công thức của X là H2N-CH2-COOH.
Câu 27:
Người ta sản xuất cao su buna từ gỗ theo sơ đồ sau:
Gỗ glucozơ ancol etylic Butađien-1,3 Cao su Buna.
Tính lượng gỗ cần thiết để sản xuất được 1 tấn cao su, giả sử trong gỗ chứa 50% xenlulozơ?
Đáp án A
(C6H10O5)n → nC6H12O6 → 2n C2H5OH → n butađien-1,3 → caosu buna
→
Khối lượng gỗ cần dùng là:
tấn
Câu 28:
Khi thủy phân hết 3,28 gam hỗn hợp X gồm hai este đơn chức, mạch hở thì cần vừa đủ 0,05 mol NaOH, thu được một muối và hỗn hợp Y gồm hai ancol cùng dãy đồng đẳng. Đốt cháy hết Y trong O2 dư, thu được CO2 và m gam H2O. Giá trị của m là
Đáp án A
nX = nNaOH = 0,05 mol →
→ Trong X chứa este HCOOCH3 (M = 60)
Sản phẩm chỉ có 1 muối là HCOONa (0,05).
Bảo toàn khối lượng:
Quy đổi ancol thành CH3OH (0,05 mol) và CH2 (0,02 mol)
Bảo toàn nguyên tố H:
Câu 29:
cdùng ít nhất V lít dung dịch HNO3 97,67% (D = 1,52 g/ml) phản ứng với lượng dư xenlulozơ.
Giá trị của V là
Đáp án C
[C6H7O2(OH)3]n + 3nHNO3 [C6H7O2(ONO2)3]n +3nH2O
Phản ứng với lượng dư xenlulozơ → Hiệu suất tính theo axit HNO3.
Khối lượng axit HNO3 cần dùng thực tế là:
28,29 lít
Câu 30:
Hỗn hợp E gồm hai amin X (CnHmN), Y (CnHm+1N2, với n ≥ 2) và hai anken đồng đẳng kế tiếp. Đốt cháy hoàn toàn 0,08 mol E, thu được 0,03 mol N2, 0,22 mol CO2 và 0,30 mol H2O. Phần trăm khối lượng của X trong E là
Đáp án B
Nhận thấy X và Y có cùng số pi
→ amin no hoặc là amin không no 1 nối đôi
Nếu 2 amin không no 1 nối đôi thì = 0,08 mol
→ x + y = 0,08 (loại). Vì x + y + z = 0,08
→ các amin đều no
Ta có: nE = x + y + z = 0,08 (1)
Theo định luật bảo toàn nguyên tố N:
x + 2y = 0,06 (2)
(3)
Từ (1), (2) và (3)
→ x = 0,04 mol; y = 0,01 mol và z = 0,03 mol
Anken có dạng công thức trung bình là CaH2a
Bảo toàn nguyên tố C:
→ n = 3 và a = 7/3 là nghiệm duy nhất
→ E gồm C3H9N 0,04 mol và C3H10N2 0,01 mol và C7/3H14/3 0,03 mol
→ % C3H9N = 57,84%
