Đề kiểm tra giữa học kì 2 Hóa 12 có đáp án (Mới nhất) (Đề 14)
-
2401 lượt thi
-
40 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Đáp án đúng là: C
Nếu M là nguyên tố nhóm IA thì oxit cao nhất của nó có công thức là M2O.
Câu 2:
Đáp án đúng là: B
Phương pháp nhiệt luyện là phương pháp sử dụng các chất khử C, CO, H2, Al,...khử oxit kim loại sau Al ở nhiệt độ cao thành kim loại đơn chất.
Câu 3:
Đáp án đúng là: D
Nguyên tắc chung để điều chế kim loại là khử ion kim loại thành nguyên tử kim loại.
Câu 4:
Dẫn khí CO2 vào dung dịch NaOH dư, khi phản ứng kết thúc thu được dung dịch Y. Dung dịch Y có chứa
Đáp án đúng là: A
CO2 + 2NaOH → Na2CO3 + H2O
Do NaOH dư nên sau khi phản ứng kết thúc thu được dung dịch chứa NaOH dư và Na2CO3.
Câu 5:
Đáp án đúng là: D
Quặng đolomit có thành phần chính là CaCO3.MgCO3
Câu 6:
Nguyên liệu chính dùng để sản xuất nhôm là
Đáp án đúng là: D
Nguyên liệu chính dùng để sản xuất nhôm là quặng boxit.
Câu 8:
Đáp án đúng là: B
CO2 + Ca(OH)2 → CaCO3↓ + H2O
CO2 + CaCO3 + H2O → Ca(HCO3)2
Câu 9:
Đáp án đúng là: B
Trong phòng thí nghiệm Na bảo quản bằng cách ngâm trong dầu hỏa.
Câu 10:
Phèn chua có công thức hóa học nào sau đây?
Đáp án đúng là: B
Phèn chua có công thức hóa học là: K2SO4. Al2(SO4)3.24H2O
Câu 11:
Đáp án đúng là: C
Phương pháp thủy luyện dùng để điều chế những kim loại trung bình và yếu như Cu, Ag...
Câu 12:
Đáp án đúng là: A
Những chất tan trong nước cho dung dịch bazơ là: CaO, Na, K2O
Câu 13:
Nồng độ phần trăm của dung dịch thu được khi cho 3,9 gam kali vào 136,2 gam H2O là
Đáp án đúng là: C
2K + 2H2O → 2KOH + H2
0,1 0,1 0,05
Ta có: mct = mKOH = 0,1.56 = 5,6 gam
Áp dụng định luật bảo toàn khối lượng:
mdd = mK + mnước - mkhí = 3,9 + 136,2 – 2.0,05 = 140 gam
Câu 14:
Đáp án đúng là: D
Bảo toàn nguyên tố Fe:
→ mFe = 0,06.56 = 3,36 gam
Câu 15:
Đáp án đúng là: B
Chất CsOH có tính bazơ mạnh nhất trong các chất đã cho.
Câu 16:
Cho các phát biểu sau về nước cứng:
(a) Khi đun sôi ta có thể loại được độ cứng tạm thời của nước.
(b) Có thể dùng Na2CO3 để loại cả độ cứng tạm thời và độ cứng vĩnh cửu của nước.
(c) Dung dịch HCl hòa tan được CaCO3, MgCO3 nên dùng HCl để làm mềm nước cứng.
(d) Có thể dùng Ca(OH)2 với lượng vừa đủ để làm mềm nước cứng toàn phần.
Số phát biểu đúng là
Đáp án đúng là: D
Các phát biểu đúng là: (a), (b)
Phát biểu c sai vì HCl không làm mềm nước cứng.
Phát biểu d sai vì dùng Ca(OH)2 vừa đủ làm nước cứng tạm thời.
Câu 17:
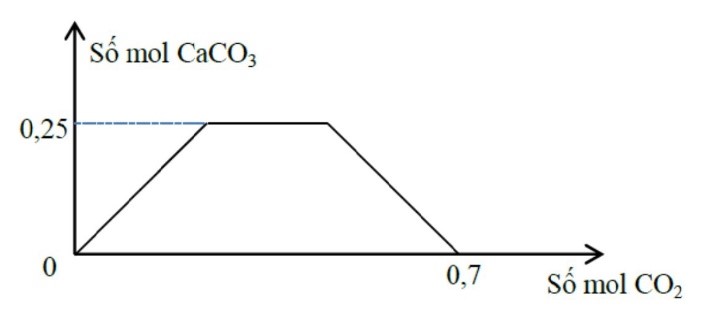
Tỉ lệ a : b tương ứng là
Đáp án đúng là: C
Khi kết tủa bị hoà tan hoàn toàn thì dung dịch chứa Ca(HCO3)2 (a mol) và NaHCO3 (b mol)
→ b = 0,2
Vậy a : b = 0,25 : 0,2 = 5:4
Câu 18:
Đáp án đúng là: B
Gọi kim loại cần tìm là M
→ M =
Vậy M là kali.
Câu 19:
Đáp án đúng là: B
Khi điện phân NaCl nóng chảy (điện cực trơ), tại anot xảy ra sự oxi hóa ion Cl-
Câu 20:
Khi cho từ từ đến dư dung dịch NH3 vào dung dịch AlCl3. Hiện tượng thu được là
Đáp án đúng là: A
3NH3 + 3H2O + AlCl3 → Al(OH)3↓ + 3NH4Cl
Câu 21:
Muối X tác dụng với dung dịch HCl có khí thoát ra, tác dụng với dung dịch NaOH có kết tủa. X là
Đáp án đúng là: A
Ca(HCO3)2 + 2HCl → CaCl2 + CO2↑ + H2O
Ca(HCO3)2 + 2NaOH → CaCO3↓ + Na2CO3 + 2H2O
Câu 22:
Đáp án đúng là: D
Dãy gồm các chất đều tác dụng được với dung dịch HCl và dung dịch NaOH là NaHCO3, K, Al2O3, Al(OH)3.
Chú ý: K tác dụng với nước có trong dung dịch NaOH.
Câu 23:
Để phản ứng vừa đủ với 5,4 gam Al cần 100 ml dung dịch NaOH x (mol/l). Giá trị của x là
Đáp án đúng là: D
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
Theo phương trình: nNaOH = nAl = 0,2 mol
→ x = 2M
Câu 24:
Thể tích dung dịch Ca(OH)2 0,01M tối thiểu để hấp thụ hết 0,02 mol khí CO2 là
Đáp án đúng là : B
Ca(OH)2 + 2CO2 → Ca(HCO3)2
Theo phương trình:
lít
Câu 25:
Đáp án đúng là: C
→ mCu = 0,02.64 = 1,28 gam
Câu 26:
Đáp án đúng là: B
Sử dụng dung dịch NaOH làm thuốc thử
+ Không có hiện tượng: Mg
+ Chất rắn tan và có khí không màu thoát ra: Al
+ Chất rắn tan và không có khí thoát ra: Al2O3
Câu 27:
Đáp án đúng là: D
Điện phân dung dịch NaCl có màng ngăn, ở catot thu được khí H2
Câu 28:
Đáp án đúng là: A
Vì cho từ từ dung dịch HCl nên phản ứng xảy ra theo thứ tự
→ H+ dư 0,04 – 0,015 = 0,025 mol
Và tổng số mol HCO3- là 0,015 + 0,02 = 0,035 mol
Câu 29:
Đáp án đúng là: A
Bảo toàn e:
→ mAl = 10,8 gam
Câu 30:
Đáp án đúng là: C
C không đúng vì Ca bị oxi hóa khi tác dụng với Cl2.
Câu 31:
Đáp án đúng là: A
2CO2 + Ca(OH)2 → Ca(HCO3)2
Phương trình ion rút gọn : CO2 + OH- → HCO3-
Câu 32:
Đáp án đúng là: D
Dung dịch Y chứa hai chất tan và hoà tan được Al nên Y chứa NaOH và NaCl dư, FeCl2 đã bị điện phân hết.
Ta có: nAl = 0,02 mol → nNaOH = 0,02 mol
Gọi số mol FeCl2 là a mol
→ mdung dịch giảm = 127a + 71.0,01 + 2.0,01 = 4,54
→ a = 0,03
Vậy X chứa FeCl2 (0,03 mol) và NaCl (0,06 mol)
Cho X tác dụng với dung dịch AgNO3
→ m = 20,46 gam
Câu 33:
Cho hỗn hợp gồm Na2O, CuO, Al2O3 có tỷ lệ mol 1:1:1 vào nước dư được chất rắn X. Dẫn H2 có dư đi qua X ở nhiệt độ cao được chất rắn Y. Y chứa
Đáp án đúng là: B
Na2O + H2O → 2NaOH
2NaOH + Al2O3 → 2NaAlO2 + H2O
→ X chứa CuO
H2 + CuO
Câu 34:
Thực hiện các thí nghiệm sau:
(a) Cho dung dịch NaOH vào dung dịch Ca(HCO3)2.
(b) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3.
(c) Đun nóng nước cứng vĩnh cửu.
(d) Cho dung dịch HCl đến dư vào dung dịch NaAlO2.
(e) Cho dung dịch Ba(OH)2 dư vào dung dịch AlCl3.
(f) Cho dung dịch NaOH vào nước cứng tạm thời.
Số thí nghiệm thu được kết tủa sau phản ứng là
Đáp án đúng là: C
Những thí nghiệm thu được kết tủa là: (a), (b), (f).
Câu 35:
Cho từ từ x mol khí CO2 vào 500 gam dung dịch hỗn hợp KOH và Ba(OH)2. Kết quả thí nghiệm được biểu diễn trên đồ thị sau:
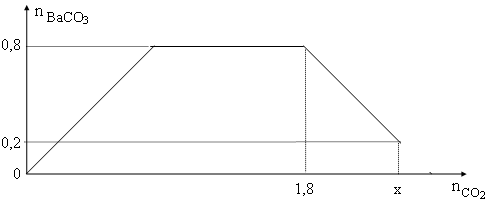
Dáp án đúng là: A
Đặt
Tại thời điểm dung dịch chứa KHCO3 và BaCO3
Mà
→ tại thời điểm còn 0,2 mol BaCO3 thì dung dịch chứa
Bảo toàn nguyên tố C
→ mdung dịch sau phản ứng =
Câu 36:
Đáp án đúng là: A
Ngâm hỗn hợp trên vào dung dịch Fe(NO3)3 thì xảy ra phản ứng
Cu + 2Fe(NO3)3 → Cu(NO3)2 + 2Fe(NO3)2
Ag không phản ứng.
Câu 37:
Đáp án đúng là: D
Với thanh (1): Vì MZn > MCu → khối lượng thanh kim loại giảm
Với thanh (2): Vì Zn không phản ứng với MgSO4 nên khối lượng thanh kim loại không đổi.
Câu 38:
Đáp án đúng là: C
A sai, Al2O3 không phản ứng với CO
B sai, CO2 + Ca(OH)2 dư CaCO3
D sai, 2NaHCO3 Na2CO3 + CO2 + H2O
Câu 39:
Đáp án đúng là: C
Mà
Vì oxi chiếm 8%
Câu 40:
Hỗn hợp X gồm 0,1 mol Na2O; 0,1 mol Ba; 0,5 mol Al. Cho X vào lượng nước dư đến khi phản ứng xảy ra hoàn toàn thì thu được V lít H2 (đktc). Giá trị của V là
Na2O + H2O → 2NaOH
0,1 0,2
Ba + 2H2O → Ba(OH)2 + H2
0,1 0,1 0,1
2Al + 2H2O + 2OH- → 2AlO2- + 3H2
0,5 0,4 0,6
→ V = 15,68 lít
